
3 个月前

3 个月前
一粒癌细胞,从原发肿瘤脱落,踏上一场穿越人体复杂环境的“长征”,最终在远端器官扎根,形成新的致命病灶。这个过程被称为肿瘤转移,是90%癌症患者死亡的直接原因。我们曾以为,这场致命迁徙的指挥官是那些飘散在体液中的化学信号,癌细胞如同嗅着气味的猎犬,循迹前行。然而,如果说这只是故事的一半呢?如果还有一种更底层、更本源的力量——如同无形的电场和水压——在为癌细胞编排着一套精准而致命的“舞步”,我们又该如何应对?
2025年12月,南京中医药大学的郭军教授团队在国际顶尖期刊《Advanced Science》上发表的一项研究,为这个问题提供了颠覆性的答案。这篇题为“渗透张力不对称性通过PDLIM7极化的微丝协同作用驱动乳腺癌细胞的趋电性迁移”的论文,如同一道闪电,照亮了肿瘤生物学的一个盲区。研究团队通过实验证明,一个微弱的外部电场,足以指挥乳腺癌细胞进行定向移动。这不仅是首次系统性地揭示了驱动癌细胞迁移的“力-电耦合”机制,更重要的是,它为郭军团队此前提出的大胆理论——“生物渗透压”——提供了坚实的实验证据。这个新理论,正悄然挑战着统治了生物和医学教科书近一个世纪的经典渗透压学说。
自19世纪末范德霍夫提出渗透压公式以来,一个核心观念深入人心:细胞内外环境处于一种精密的“等渗稳态”,渗透压的大小简单地由溶液中溶质颗粒的总数决定。在这个模型里,细胞膜被视为一张理想的半透膜,细胞就像一个被动调节内外平衡的“水袋”。然而,生命远比这个静态模型要精妙和主动得多。郭军团队敏锐地指出,活细胞的细胞膜是一个布满了精密“门控”的动态屏障,其上镶嵌着成千上万的离子通道和水通道蛋白。这些通道,尤其是那些对电压变化敏感的电压依赖性离子通道,才是真正的主宰。细胞内的游离蛋白纳米颗粒,如同微小的电容器,能通过吸附阳离子来主动调节膜电位,并与钙离子协同,上演着膜电位的“去极化”与“超极化”之舞。这意味着,细胞的渗透活动并非简单的浓度平衡,而是一个由电信号精准调控的、不同离子渗透作用相互“对抗”的动态力学系统。这,就是“生物渗透压”理论的核心。
基于这一新理论框架,郭军团队得以解剖肿瘤细胞在电场中的一举一动。借助先进的荧光共振能量转移张力探针技术,他们得以实时“看见”细胞内部微丝张力和渗透压的微妙变化,一幅清晰的作战图景徐徐展开:
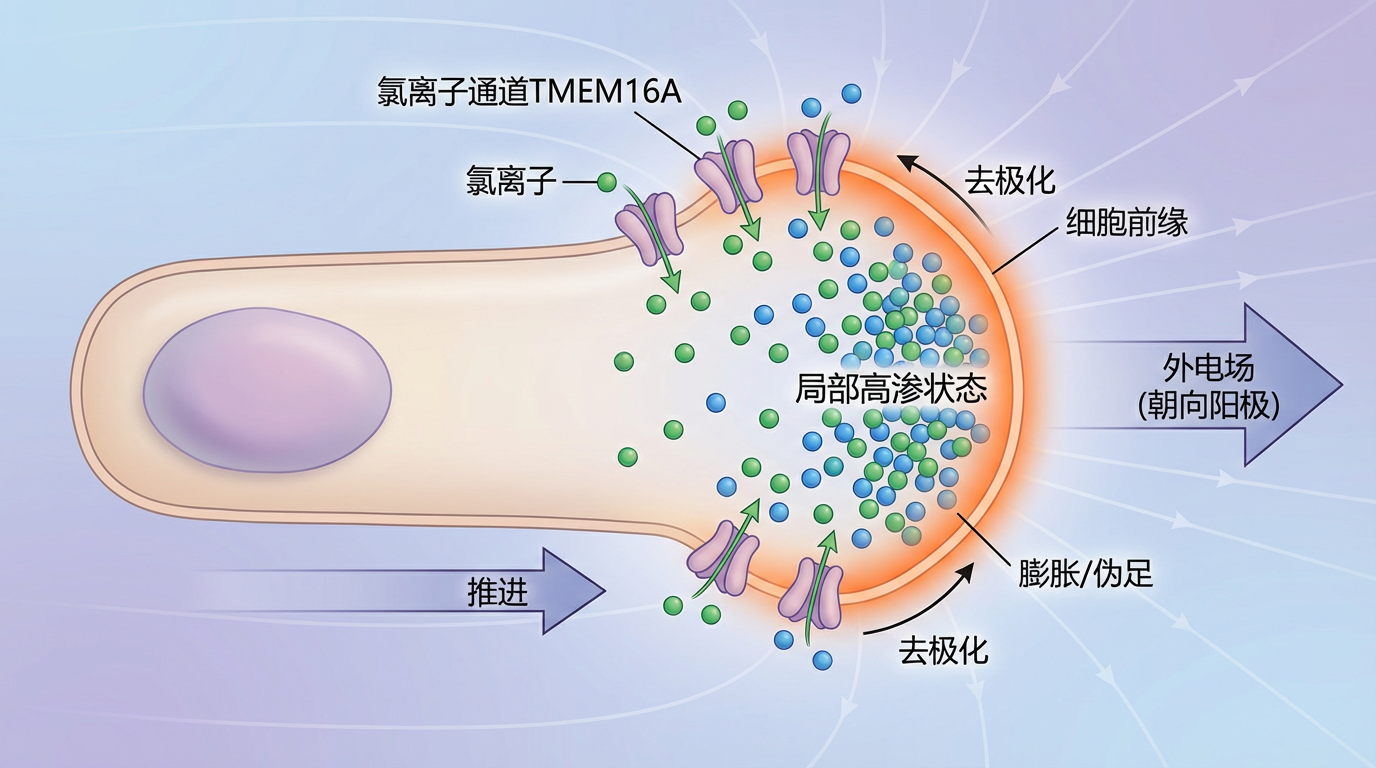
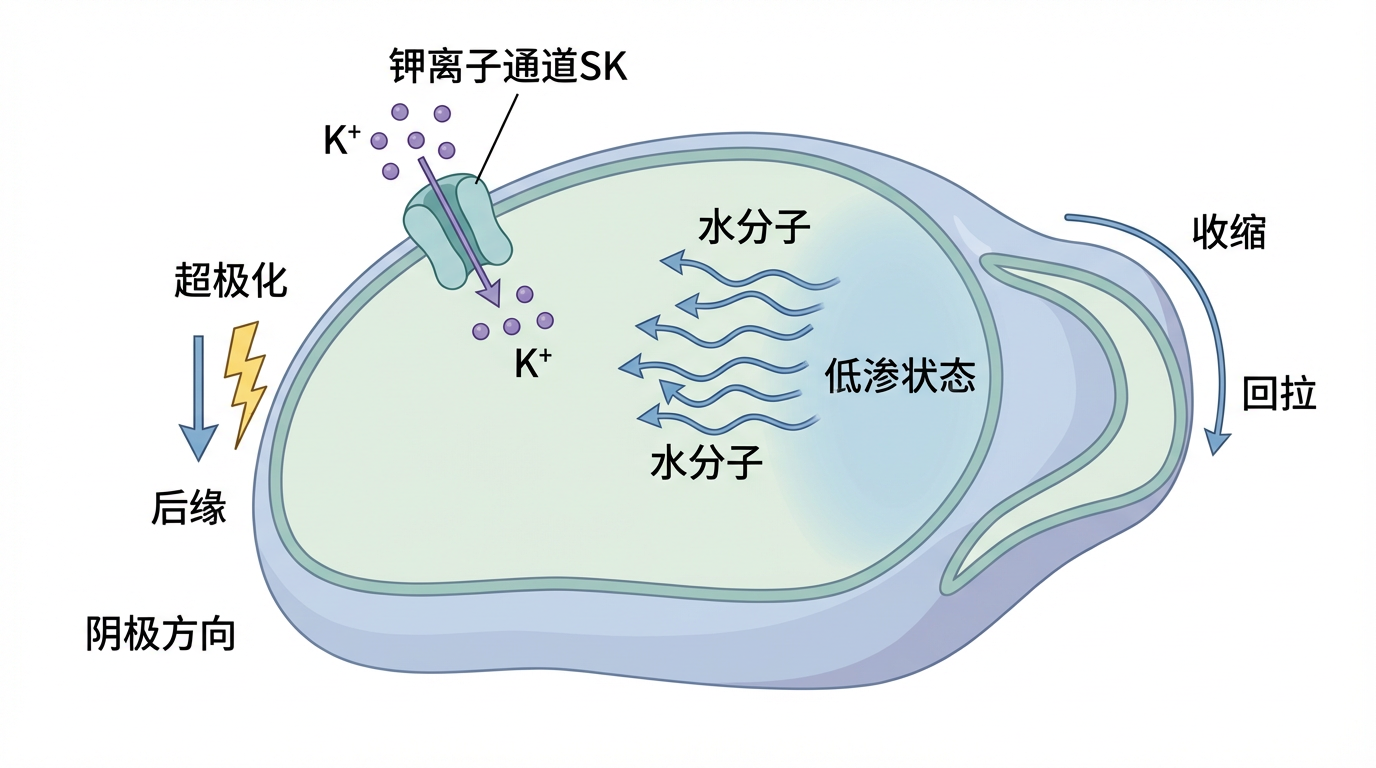
这一“前推后拉”的完美配合,形成了一部由电力驱动的微型引擎。但故事并未结束。细胞前后缘形成的渗透压差,像一块磁铁,在空间上极化招募了蛋白激酶A。该激酶随即磷酸化了微丝骨架的关键结合蛋白PDLIM7。被激活的PDLIM7与肌动蛋白的结合能力大增,在细胞前后两端形成了高度极化的内部张力网络。这个力学网络与渗透压产生的推力矢量叠加,共同构成了驱动肿瘤细胞持续、定向迁移的强大合力。至此,“电信号-离子渗透力学-细胞骨架机械响应”这一完整的调控链条被首次清晰地描绘出来。
“生物渗透压”理论的提出和验证,其意义远不止于一篇顶级论文或一个精巧的科学解释。它是一场可能从根本上改变医学实践的认知革命。
郭军团队的发现,为我们打开了一扇通往细胞生命物理本质的新窗口。它揭示了,在最微观的生命尺度上,电、力与化学信号如何交织成一曲生命的交响乐,而肿瘤,正是这首乐曲中一个致命的、失序的变奏。当新一代的医学生和研究者们,开始用“生物渗透压”的全新视角去解读教科书上的经典知识时,我们有理由相信,一场从基础医学到临床实践的深刻变革,或许才刚刚拉开序幕。癌细胞的致命“舞步”已被洞悉,而人类反击的乐章,正在谱写新的篇章。
点击充电,成为大圆镜下一个视频选题!