对抗知识焦虑,从看懂这条开始
App 下载
mRNA癌症疫苗不靠主干道,双通路激活T细胞
华盛顿大学医学院|T细胞激活|树突状细胞cDC2|树突状细胞cDC1|mRNA癌症疫苗|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
华盛顿大学医学院|T细胞激活|树突状细胞cDC2|树突状细胞cDC1|mRNA癌症疫苗|肿瘤学|医学健康
2023年全球新发癌症近2000万,90%的死亡源于实体瘤的侵袭转移——这是悬在人类头顶的冰冷数字。mRNA疫苗曾以黑马之姿终结新冠大流行,如今转向攻克癌症,但它到底如何调动免疫系统追杀癌细胞,一直是个未完全解开的谜。
过去的免疫学教科书里,1型经典树突状细胞(cDC1)是激活抗癌T细胞的唯一“金牌教官”,所有疫苗都得走它这条“主干道”。但华盛顿大学医学院的一项新研究,把这个写进教材的认知彻底推翻了。
研究人员在小鼠身上做了个极端测试:把体内负责激活T细胞的cDC1细胞全部清除,再注射mRNA癌症疫苗。按照传统认知,没了“金牌教官”,T细胞应该毫无反应,肿瘤会继续疯长。
结果却让所有人意外。
即使没有cDC1,mRNA疫苗依然激活了强烈的抗癌T细胞反应,成功清除了小鼠体内的肉瘤——这意味着,还有另一条路在支撑疫苗起效。
这条路的主角,是cDC1的“表亲”cDC2。过去大家都认为,cDC2只负责辅助性T细胞的激活,根本碰不到抗癌的CD8+ T细胞。但mRNA疫苗偏偏激活了这个“替补队员”,而且它的能力一点不差。
更关键的是,cDC1和cDC2激活的T细胞,虽然分子特征略有不同,但都能有效追杀癌细胞,还能形成长期免疫记忆——相当于给免疫系统装了双保险,一条路堵了,另一条照样能打。
cDC2到底是怎么绕过传统路径,激活T细胞的?研究人员揭开了它的“独门秘籍”:交叉装饰。
你可以把这个过程想象成一场证据传递:肿瘤细胞或组织细胞先根据mRNA的指令,生产出肿瘤特异性抗原蛋白,把它切成小片段后,挂在自己表面的MHC-I分子上——这就像把“犯罪证据”装在了自己的“身份证”上。
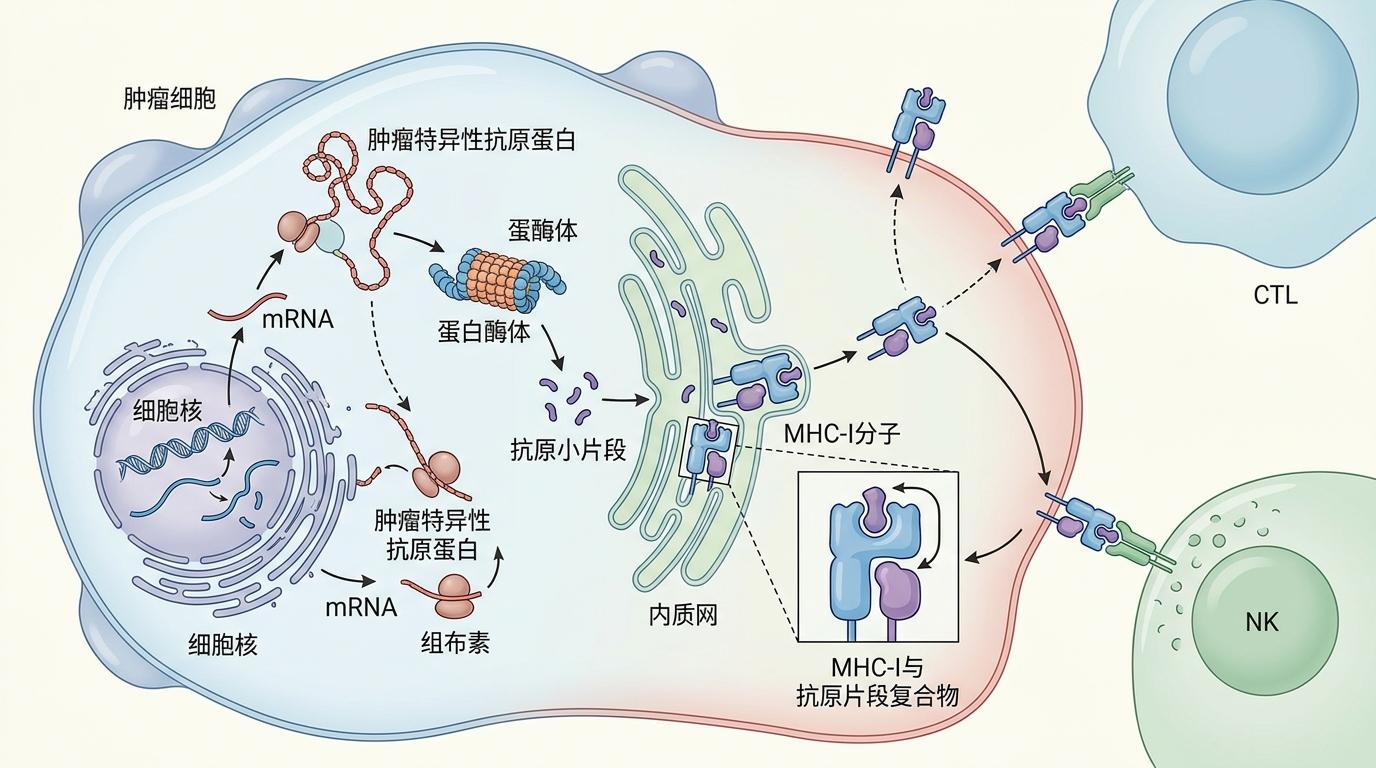
随后,这些细胞会把挂着证据的“身份证”整个“借”给cDC2。cDC2不用自己加工抗原,直接拿着现成的证据去找T细胞:“看,这就是癌细胞的标记,去消灭它们!”
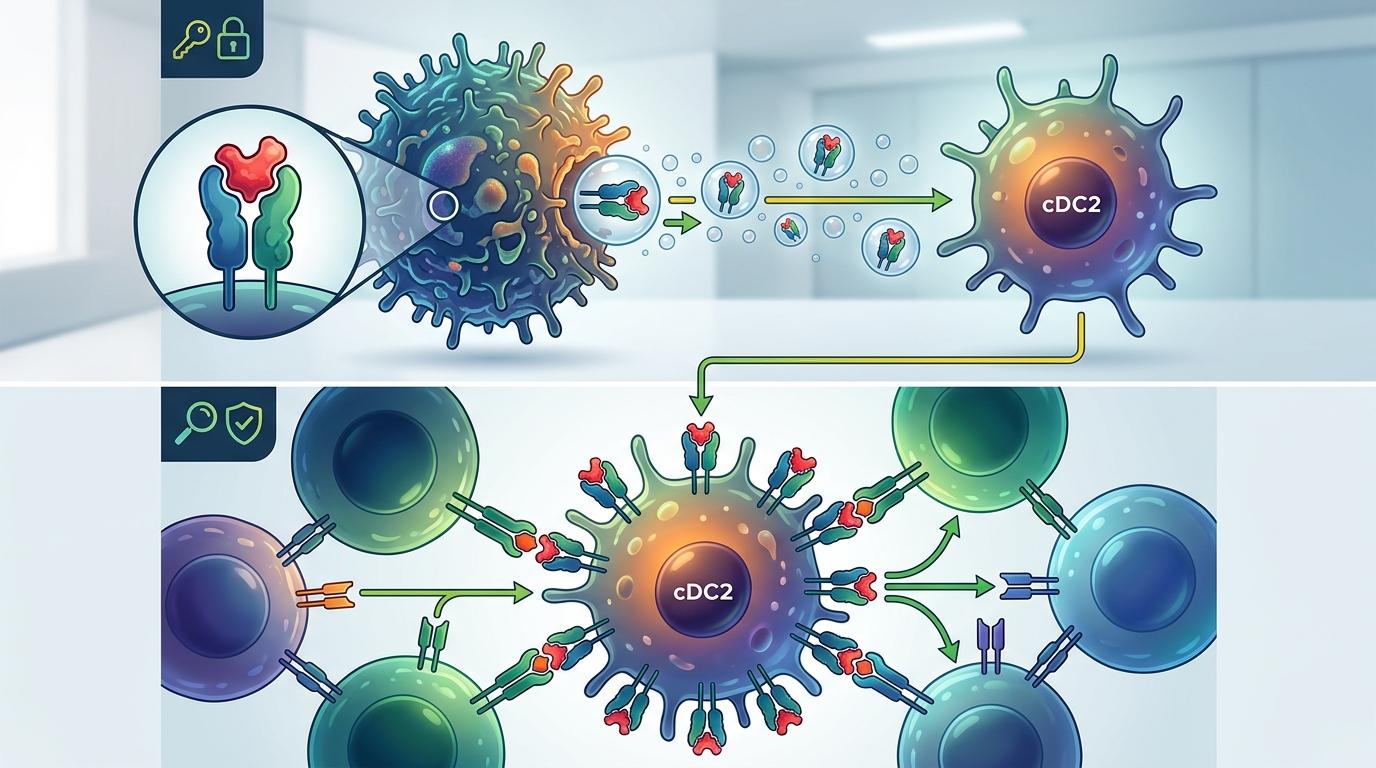
这个过程完全不依赖cDC1常用的WDFY4通路,而是靠I型干扰素信号驱动。简单说,cDC2学会了“借花献佛”,跳过了传统的抗原加工步骤,效率反而更高。
研究人员还发现,mRNA疫苗的脂质纳米颗粒(LNP)载体,在这个过程中起到了关键作用——它能同时激活cDC1和cDC2,两条通路齐头并进,这也是mRNA疫苗比传统疫苗效力更强的核心原因。
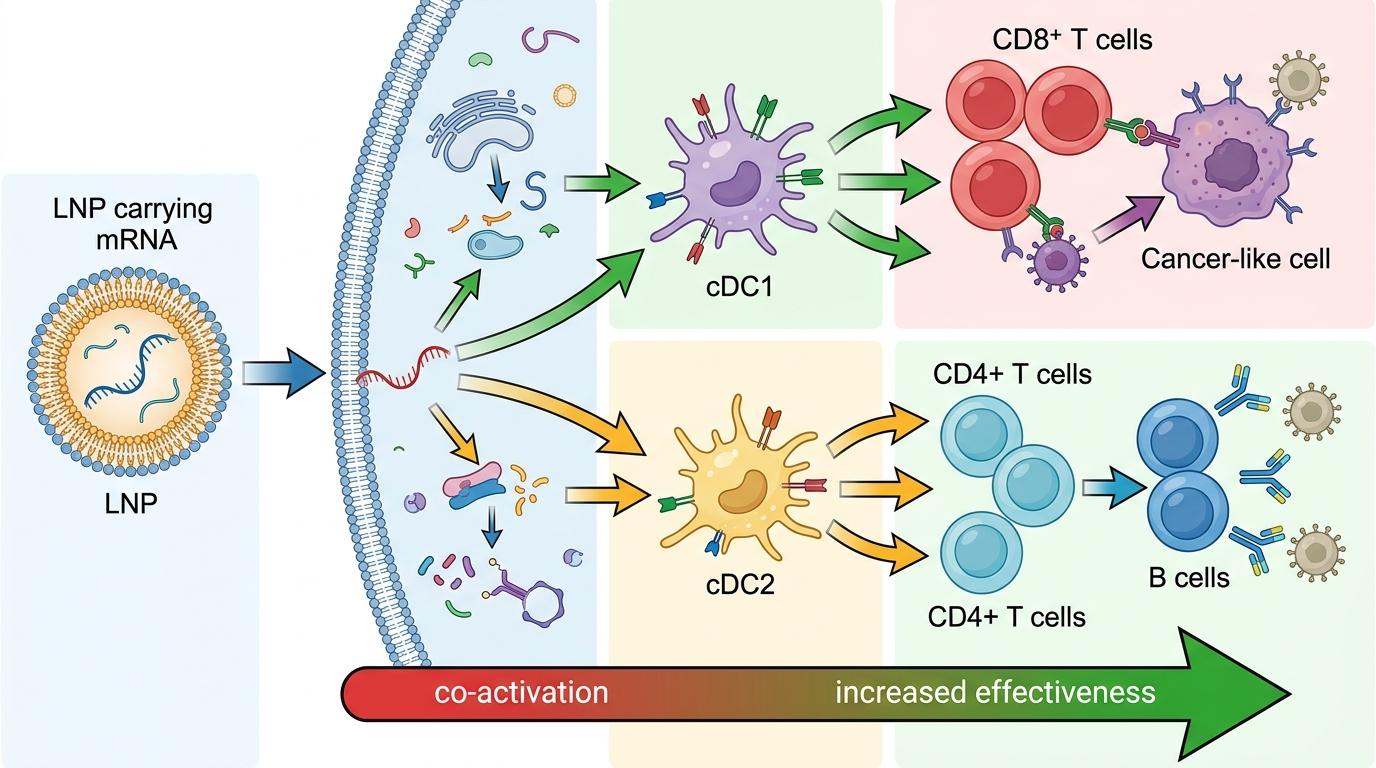
这个发现不止改写了免疫学教科书,更给癌症患者带来了实际的希望。
临床中,总有部分患者对mRNA疫苗反应不佳,过去医生找不到原因,现在终于有了答案:可能是这些患者体内cDC1细胞的数量或功能不足,但如果能激活cDC2通路,他们也能获得有效的治疗。
未来的mRNA癌症疫苗,可以不再只盯着cDC1设计,而是同时瞄准两条通路——比如通过调整LNP的配方,增强对cDC2的激活,或者直接利用交叉装饰机制,提升cDC2的抗原呈递效率。
当然,这项研究目前还停留在小鼠模型阶段,人类的免疫系统比小鼠复杂得多,cDC2在人体内的表现是否和小鼠一样,还需要更多临床试验验证。但至少,它打开了一扇新的大门:原来免疫系统的潜力,比我们想象的大得多,那些被忽视的“替补队员”,关键时刻能撑起一片天。
从新冠疫苗到癌症治疗,mRNA技术一次次打破我们的认知。它没有沿着传统疫苗的老路走,而是找到了免疫系统的“备用通道”,用双保险机制激活了抗癌的T细胞。
这让我们意识到,人类对免疫系统的了解,还只是冰山一角。那些被教科书定义为“次要角色”的细胞,可能藏着未被开发的巨大潜力。
免疫系统的备用通道,是抗癌的新希望。
对于那些在等待更有效疗法的癌症患者来说,这个发现,就是黑暗里的一道光——我们对抗癌症的武器,又多了一件。