对抗知识焦虑,从看懂这条开始
App 下载
肝脏的“B计划”:当免疫“中心法则”被打破,一个沉默器官如何筑起最后防线
浆细胞|《自然》期刊|病毒感染|B细胞|肝脏免疫|免疫学基础|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
浆细胞|《自然》期刊|病毒感染|B细胞|肝脏免疫|免疫学基础|生命科学
在免疫学的宏伟殿堂中,一条“中心法则”如同基石般支撑着我们的认知:面对病毒入侵,所有战役的指挥权都归于二级淋巴器官(SLOs)——那些遍布全身的淋巴结与脾脏。教科书描绘的画面是,抗原被押送至这些壁垒森严的“军事学院”,B细胞在此接受严苛训练,最终进化为能精准打击敌人的浆细胞,释放高效抗体。然而,生命总是在最意想不到的角落,上演颠覆常规的奇迹。如果战场本身就是一座孤岛?如果病毒狡猾到能让全身的警报系统集体失声?机体,是否就此束手就擒?
就在不久前,《自然》期刊上的一项研究为我们揭示了一个惊心动魄的“B计划”。研究人员发现,当一种病毒将战场完全局限在肝脏,导致传统免疫中心“失灵”时,肝脏竟能在战火废墟中,自发构建起一套功能完备的临时淋巴组织——诱导性肝相关淋巴组织(iHALT)。这并非简单的细胞聚集,而是一场在绝境中精密布局、就地取材的“绝地反击”。
要理解这场反击的巧妙之处,我们需先认识两位风格迥异的“入侵者”。一位是免疫学研究的“老熟人”——淋巴细胞脉络丛脑膜炎病毒(LCMV),它引发的是一场典型的全身性战役。一旦入侵,全身的免疫系统,从外周血到脾脏,都会迅速响应。数据显示,感染4周后,骨髓中的抗体分泌细胞(ASCs)数量激增16.1倍,完全符合“一方有难,八方支援”的经典模式。
另一位则是啮齿动物肝炎病毒(RHV),它与人类丙型肝炎病毒(HCV)极为相似,是个彻头彻尾的“恋肝癖”,只攻击肝脏。当RHV感染小-鼠时,一幅诡异的景象出现了:全身的免疫雷达,无论是外周血还是脾脏,都近乎静默。即便到了第4周,骨髓中的抗体分泌细胞也毫无动静。然而,在肝脏这座“孤城”之内,战况却已白热化。感染后11天,肝内抗体细胞仅微增1.3倍,但到了第4周,这个数字竟飙升了280.6倍。数据清晰地表明:这场战争的指挥部和兵工厂,并未设在远方的中央要塞,而是以前所未有的密度,直接建在了战火最前线。
科学的魅力在于大胆假设,小心求证。肝脏内激增的免疫细胞,会不会只是从脾脏等“中央军区”调派来的援军?为了排除这种可能,研究团队设计了一组堪称“釜底抽薪”的实验。
他们首先切除了小鼠的脾脏,相当于端掉了最大的一个免疫指挥部。接着,他们使用了一种名为FTY720的药物,这种药物的作用好比“封锁城门”,能阻止淋巴细胞从所有淋巴器官中流出。在应对全身性感染(LCMV)时,这套组合拳是致命的,病毒无法被清除。这再次印证了传统法则:没有中央指挥部的支援,仗没法打。
然而,当这套逻辑被应用到RHV感染时,结果令人瞠目结舌。无论是切除脾脏,还是封锁淋巴细胞,小鼠竟然都能顺利清除病毒。数据显示,用药组与未用药组之间,肝脏内的抗体分泌细胞数量几乎没有差异。这意味着,在对抗这类高度“恋肝”的病毒时,脾脏和淋巴结这些二级淋巴器官,不仅不是核心,甚至可以说是“可有可无”的。事实只有一个:肝脏,这个我们眼中的代谢与解毒工厂,在危急时刻,独立承担起了免疫兵工厂的全部职责。
既然没有外援,肝脏内部必然发生了翻天覆地的结构重塑。这种被命名为iHALT的临时建筑,在显微镜下,不像淋巴结那样拥有界限分明、井井有条的“功能分区”,它更像一个战时匆忙搭建的“游击队营地”,B细胞与T细胞交织在一起,边界模糊。
但“杂乱”绝不等于“无序”。借助空间转录组学技术,科学家绘制了iHALT的精细地图。他们发现,在这个看似混乱的细胞团块中,所有高级免疫反应的关键信号一应俱全。这里有负责抗体“武器升级”的核心酶——由Aicda基因编码的AID酶,证明B细胞正在进行体细胞超突变,现场打磨抗体,使其更具杀伤力。这里还有功能完备的“生发中心样”B细胞和滤泡辅助性T细胞(Tfh),它们是B细胞成熟分化的关键“教官”与“战友”。
更有趣的是,这场“局部动员”的时机。在全身性感染中,脾脏的生发中心在第2周就达到顶峰,速战速决。而在RHV感染中,所有戏剧性的变化都推迟到了第4-周,且完全局限在肝脏。这种“虽迟但到”的精准反击,正是iHALT的标志——它不如正规军反应神速,但它能在正规军无法触及的敌后战场,建立起坚固的根据地。
通常,完成训练的浆细胞(Plasma Cells)会离开淋巴器官,迁移到骨髓这个“养老院”中长期服役。但在iHALT中,这些细胞却选择了“就地扎营”。是什么力量将它们留在了肝脏这个充满代谢压力的地方?
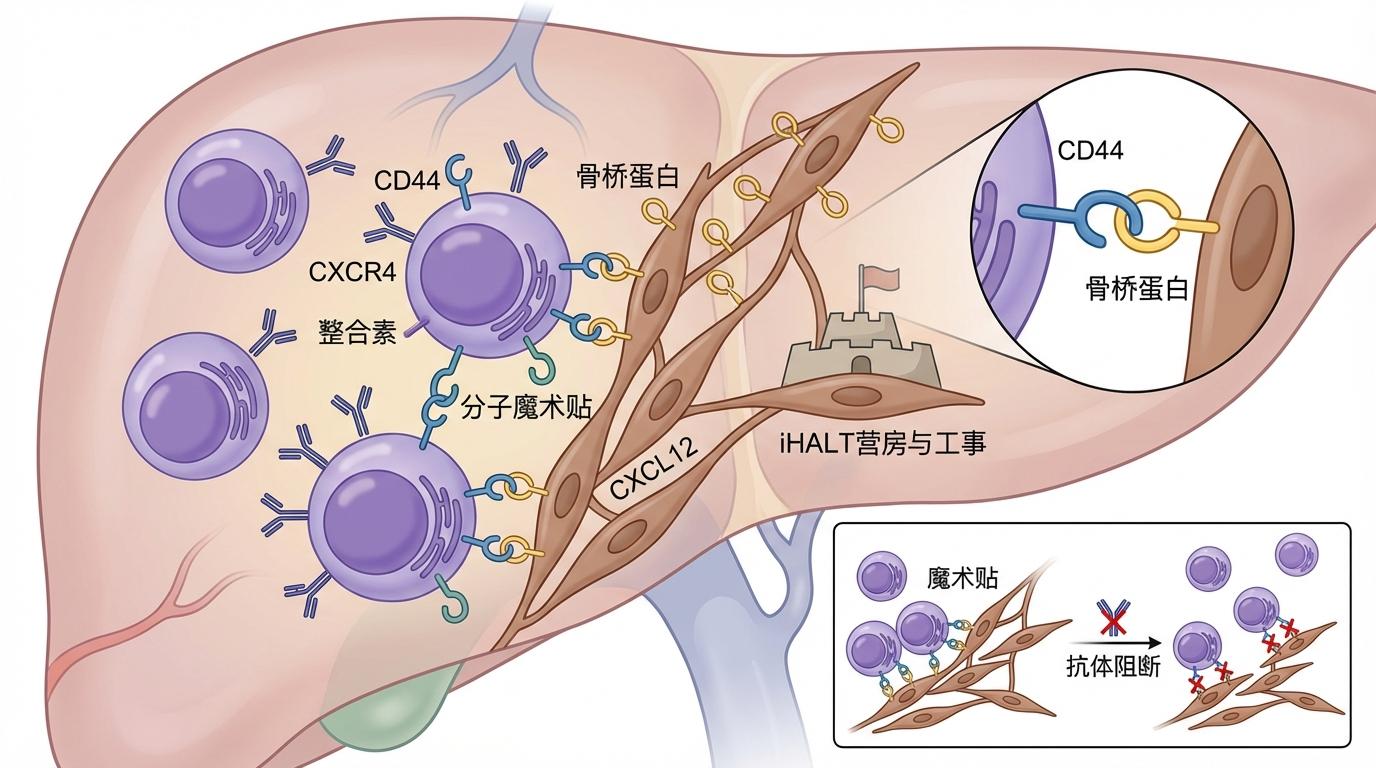
答案藏在细胞间的“分子魔术贴”里。研究发现,iHALT中的浆细胞高表达一系列“钩子”分子,如CD44、CXCR4和整合素。而在它们周围的成纤维细胞上,则恰好高表达与之对应的“毛面”分子,如骨桥蛋白和CXCL12。这些“同源锚定对”将浆细胞牢牢固定在肝脏的门静脉周围区域。当研究人员用抗体阻断这些“魔术贴”时,肝脏内的浆细胞数量显著下降。这表明,iHALT不仅生产士兵,还为他们提供了能够长期驻扎和战斗的“营房”和“工事”。
这项发现在小鼠身上的验证固然激动人心,但它是否同样存在于人类体内?利用尖端的亚细胞空间转录组技术,研究人员分析了人类肝脏样本。结果令人振奋:在健康人的肝脏中,看不到任何类似的淋巴结构。但在**丙型肝炎(HCV)**患者的肝脏中,研究人员看到了与小鼠RHV感染模型中几乎一模一样的画面。
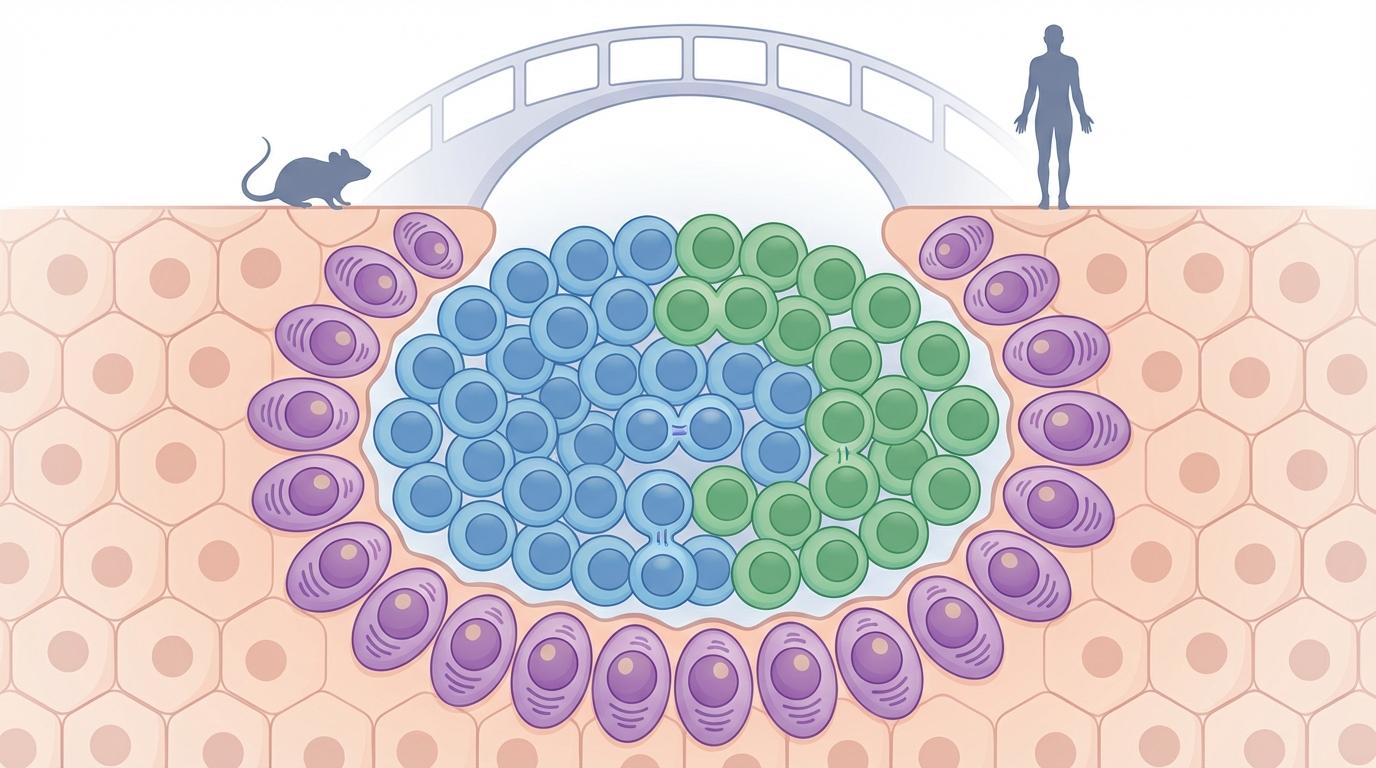
在这些患者的肝脏中,同样存在着由分裂旺盛的B细胞和T细胞构成的“生发中心样”结构,边缘同样驻扎着大量的浆细胞。这种在细胞组成、空间布局和分子信号上的高度一致性,强有力地证明了iHALT并非小鼠的专利,而是哺乳动物在面对嗜肝病毒时,共有的一种古老而保守的免疫策略。
为什么生命要进化出iHALT这样一套备用系统?从进化的视角看,这是一个充满智慧的妥协。二级淋巴器官虽然高效,但它们也是病毒的重点攻击目标。许多病毒,尤其是那些引发慢性感染的病毒,早已学会了如何抑制或逃避这些中央免疫系统的监视。
对于像HCV这样将战场严格限制在肝脏的病毒,如果机体仍固执地依赖远端的淋巴结,无异于远水解不了近渴。iHALT的出现,完美解决了这个空间难题。通过在感染灶局部建立“兵工厂”,机体实现了:
这项研究不仅改写了我们对肝脏功能的认知,更可能为慢性病毒性肝炎、自身免疫性肝病乃至肝癌的治疗开辟全新道路。我们是否可以人为诱导或增强iHALT的形成来打破免疫耐受?反之,这些驻留的免疫细胞是否也是导致肝纤维化的元凶?
当教科书上的“中心法则”在生命的复杂现实面前被打破,我们再次见证了大自然惊人的适应能力。肝脏,这个沉默的代谢器官,在免疫的废墟之上,为生命默默筑起了最后一道防线。它提醒我们,当一扇门(二级淋巴器官)被关上时,生命总会巧妙地,为自己打开一扇窗(iHALT)。