3 个月前

3 个月前
胰腺癌,因其极高的恶性度和极低的生存率,长久以来被冠以“癌中之王”的称号。在显微镜下,胰腺肿瘤呈现出一座坚不可摧的“堡垒”——致密的纤维化基质,它像护城河一样将癌细胞与外界隔绝,不仅阻碍了化疗药物的渗透,也抵挡了免疫细胞的进攻。而建造这座堡垒的“工兵”,便是一种名为**癌症相关成纤维细胞(Cancer-associated Fibroblasts, CAFs)**的细胞。
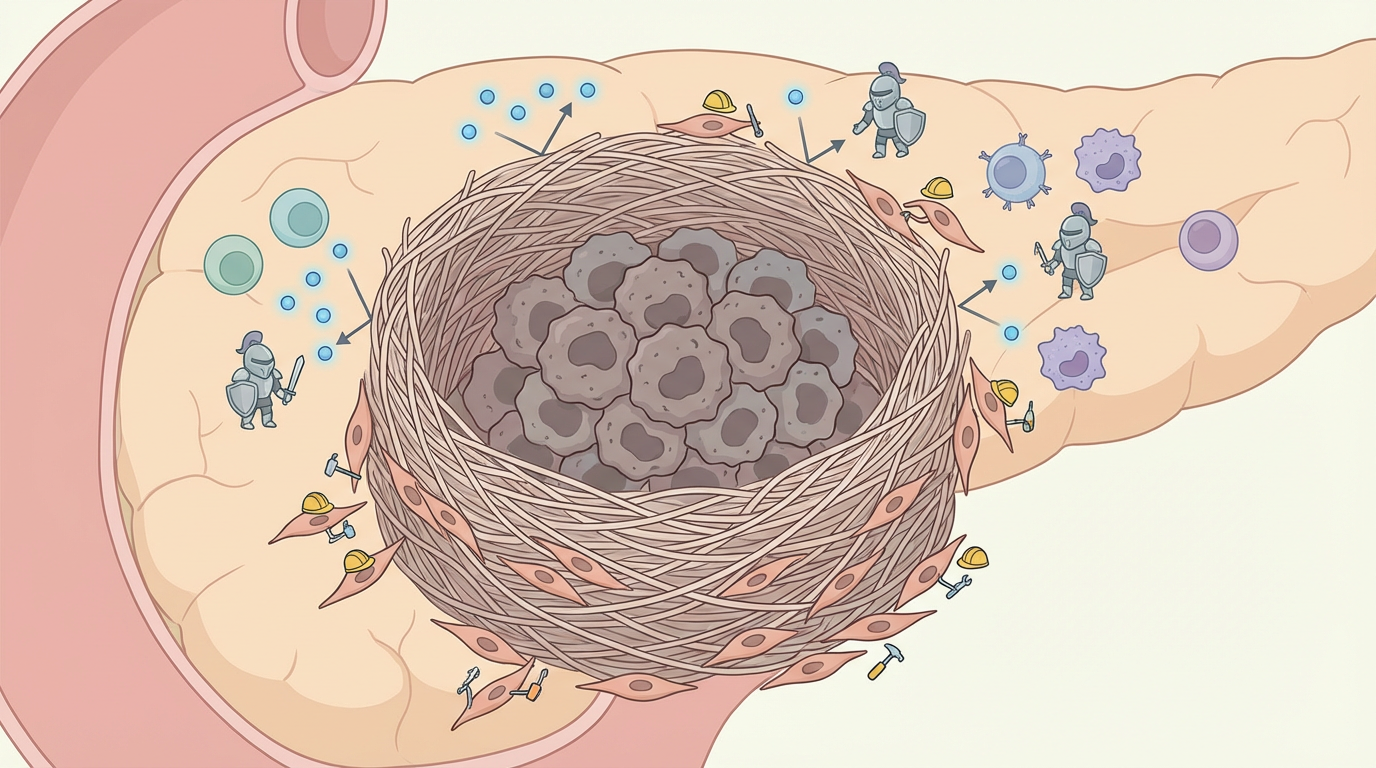
长久以来,科学家们普遍认为CAFs是肿瘤的“帮凶”,它们不遗余力地为癌细胞搭建庇护所、提供养分、甚至释放信号迷惑免疫系统。然而,一系列靶向清除CAFs的临床试验却意外失败,有时甚至加速了肿瘤的恶化。这让科学界陷入了深深的困惑:我们对这位“帮凶”的理解,是否从一开始就错了?如果这些“工兵”中,不仅有忠诚的建造者,还混入了意图不轨的“内奸”呢?
这场困惑的答案,在近期一项突破性研究中初现端倪。北京大学的杨尹默、田孝东团队与美国约翰斯·霍普金斯大学的He Jin团队合作,在国际顶尖期刊《GUT》上发表了一项重要成果。他们利用先进的单细胞多组学技术,以前所未有的精度绘制了胰腺癌中CAFs的详细图谱。
研究团队发现了一个此前未被充分认识的CAF亚群——分泌补体的CAFs(complement-secreting CAFs, csCAFs)。令人惊讶的是,肿瘤组织中csCAFs比例越高的患者,其总生存期和无复发生存期都显著更长。这一发现颠覆了CAFs全是“坏人”的传统认知,首次明确了一种与“好预后”相关的CAF亚型。
更深一步的分析揭示,csCAFs可能是一种相对“天真”的早期CAF形态,它们与促使肿瘤恶化的**炎症性CAFs(inflammatory CAFs, iCAFs)**在基因和表观遗传层面有着千丝万缕的联系,甚至可能在肿瘤进展过程中分化为iCAFs。这一发现如同一道曙光,不仅解释了CAFs功能的复杂性,更指明了一条全新的治疗路径:我们或许不必赶尽杀绝,而是可以“策反”那些坏的iCAFs,让它们变回好的csCAFs。
要理解这场发生在肿瘤微环境中的“细胞战争”,我们必须认识其中的主要参与者。CAFs远非一个均质的群体,而是一个由多个功能迥异的亚型组成的“部落”:
肌成纤维细胞样CAF (myCAF): 这是最经典的“建造者”。它们高表达α-平滑肌肌动蛋白(α-SMA),在肿瘤细胞分泌的TGF-β信号诱导下,大量生产胶原蛋白,构筑起致密的物理屏障,是导致胰腺癌基质坚硬、药物难以渗透的元凶。
炎症性CAF (iCAF): 这是阴险的“煽动者”。它们通常远离癌细胞,但通过分泌白细胞介素-6(IL-6)等大量炎症因子,招募并“腐化”免疫细胞,如诱导巨噬细胞向抑制免疫的M2型转化,营造出一个强大的免疫抑制微环境,让免疫系统对癌细胞“视而不见”。
抗原呈递CAF (apCAF): 这是一个身份模糊的“信使”。它们表面表达MHC-II类分子,理论上可以像免疫细胞一样呈递抗原、激活T细胞。然而,由于缺乏必要的共刺激信号,它们的“报告”可能反而导致T细胞功能耗竭或被误导,其真实角色仍在激烈讨论中。
分泌补体的CAF (csCAF): 这是新发现的“潜在盟友”。它们的存在与较低水平的免疫抑制信号(如TGF-β)和较少的M2型巨噬细胞相关,暗示其可能在维持一个相对有利于抗肿瘤免疫的环境中发挥作用。
这些亚型并非一成不变,它们之间存在动态转化。正是这种异质性和可塑性,构成了胰腺癌治疗的巨大挑战,也蕴含着精准干预的无限机遇。
在胰腺癌的微环境中,一场由肿瘤细胞主导,CAFs执行,并与免疫系统对抗的复杂博弈正时刻上演。
第一幕:肿瘤细胞的“指令”。 肿瘤细胞是这场博弈的“总指挥”,它们通过分泌不同的信号分子,对周围的成纤维细胞进行“编程”。例如,释放TGF-β,指令它们分化为myCAF,加固物理防线;释放IL-1,则催生iCAF,部署化学与免疫防线。
第二幕:CAFs的“执行”。 myCAF忠实地执行命令,堆砌胶原,形成“铜墙铁壁”,让前来攻击的T细胞寸步难行。iCAF则像宣传员,四处散播免疫抑制信号,招募调节性T细胞(Tregs)和髓源性抑制细胞(MDSCs)等“叛军”,共同压制英勇的CD8+ T细胞“战士”。
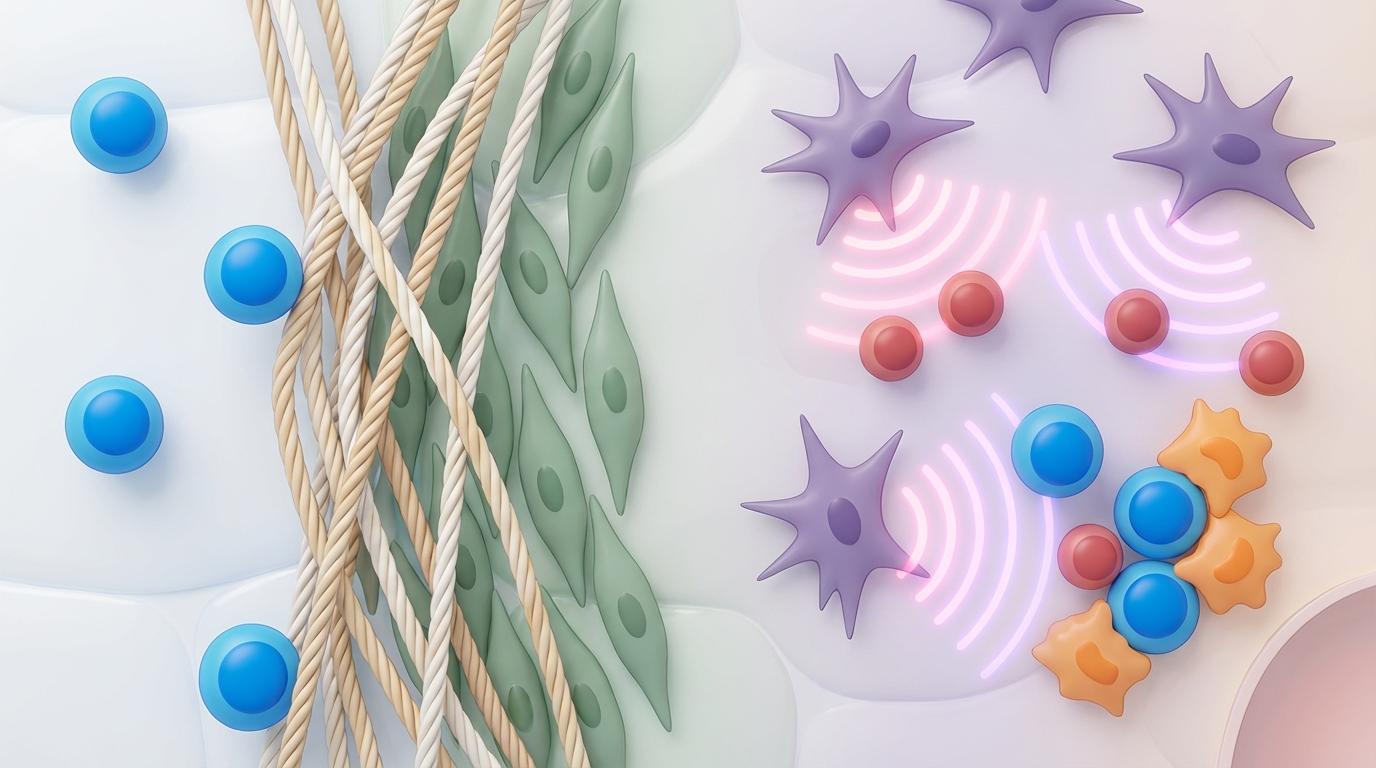
第三幕:免疫系统的“挣扎”。 在这个被精心构建的抑制性环境中,免疫系统处处受制。而csCAFs的存在,则像是在这片压抑的战场上开辟出的一小片“安全区”。在这些区域,免疫抑制信号减弱,为免疫细胞的喘息和反击提供了可能。csCAFs与T细胞之间甚至存在特定的空间互作,暗示着它们可能在悄悄地帮助免疫系统。
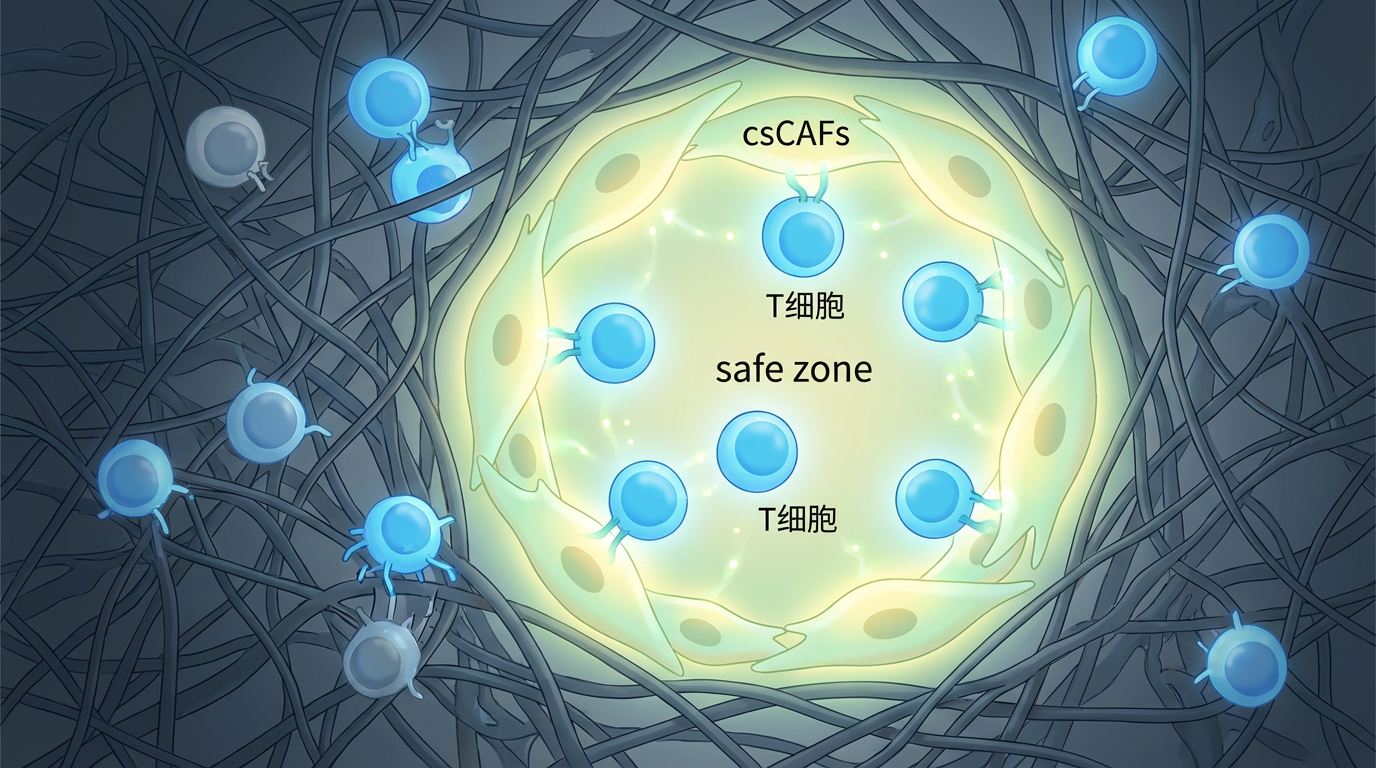
因此,胰腺癌的预后,很大程度上取决于这场博弈的平衡:是促癌的myCAF和iCAF占上风,还是抑癌的csCAFs能守住阵地?
对CAF异质性的深入理解,正引领胰腺癌治疗策略从“焦土政策”向“精准策反”转变。
过去的失败警示我们,盲目清除所有CAFs是危险的。未来的方向在于:
精准识别与靶向: 利用液体活检、多重免疫组化或成纤维细胞活化蛋白(FAP)PET-CT等先进成像技术,精确评估患者体内CAF亚型的构成。针对性地抑制myCAF的纤维化功能(如使用TGF-β抑制剂)或阻断iCAF的炎症信号(如使用IL-6抗体),而非一概而论。
功能“再编程”: GUT杂志的研究为我们描绘了最激动人心的前景——将促癌的iCAF“劝回”为具有抑癌潜力的csCAF。这需要科学家们进一步破解其转化过程中的关键调控节点,并开发出能够实现这种逆转的药物。
联合治疗新范式: 将靶向CAF亚型的疗法与现有的免疫检查点抑制剂相结合。通过瓦解CAFs构建的物理和免疫屏障,可以为免疫治疗药物和免疫细胞进入肿瘤核心创造条件,将免疫“冷”肿瘤转化为“热”肿瘤,从而显著提升疗效。
我们与“癌中之王”的战斗,正在从直接攻击癌细胞本身,扩展到一场更宏大、更精妙的“生态环境改造工程”。理解并驾驭癌相关成纤维细胞的异质性,就是我们在这场工程中,最有力的设计蓝图。前路漫长,但方向已然清晰——未来的胜利,将属于那些能够巧妙重塑肿瘤微环境,化敌为友的智慧策略。
点击充电,成为大圆镜下一个视频选题!