2 个月前

2 个月前
对抗艾滋病病毒(HIV)的科学战争,是一场持续了四十余年的漫长马拉松。全球至今仍有约3900万感染者,每年新增130万条生命被阴影笼罩,而一节能提供广泛保护的有效疫苗,始终是遥不可及的彼岸。这场斗争的核心难点,在于HIV如同一位千变万化的伪装大师。它的表面覆盖着一层致密的“聚糖盾牌”——这些糖分子像一件厚重的外衣,不仅掩盖了病毒的致命要害,还迷惑了人体的免疫系统,使其难以产生能够识别并消灭多种病毒变种的“万能钥匙”——广谱中和抗体(bNAbs)。
这层“糖衣”让传统疫苗的研发思路屡屡碰壁,通常需要7到10次序贯免疫,耗时数月甚至数年,才能勉强唤醒初步的免疫记忆。人类在这场与病毒的智力竞赛中,似乎陷入了一个无解的僵局。
然而,就在最近,美国威斯塔研究所的团队在权威期刊《Nature Immunology》上发表的一项研究,如同一道闪电划破了长夜。他们设计出一种名为WIN332的新型免疫原,在非人灵长类动物实验中,仅需单次注射,3周内便成功诱导出了针对HIV的中和活性。这一惊人的速度,将传统疫苗的启动效率提升了数倍,彻底颠覆了人们的认知。
WIN332的诞生,源于一次大胆的“反常识”设计。长期以来,科学界有一个根深蒂固的共识:HIV包膜蛋白上的一个特定聚糖位点Asn332是“不可或缺”的,抗体必须依赖它才能有效结合病毒。因此,所有的疫苗设计都小心翼翼地保留这一结构。但威斯塔研究所的科学家们发现了一个被忽视的细节:在真实世界的传播毒株中,Asn332聚糖的出现频率并不高,而且部分感染者体内能自然产生不依赖该聚糖的强大抗体。
这让他们提出了一个颠覆性的假设:或许Asn332聚糖非但不是必需品,反而是一个障碍?如果大胆地将它“拆掉”,是否能让病毒的真实面目暴露无遗,从而激活更多样、更强大的免疫反应?
基于这一革命性构想,WIN332被精心设计出来。它以一种常见的HIV毒株(BG505)的包膜蛋白为蓝本,不仅精准地删除了Asn332聚糖,还剔除了其他几个冗余的糖基,只保留了维持蛋白结构稳定所必需的最少量糖分子。这种“极简”设计,仿佛剥去了伪装大师层层的外衣。
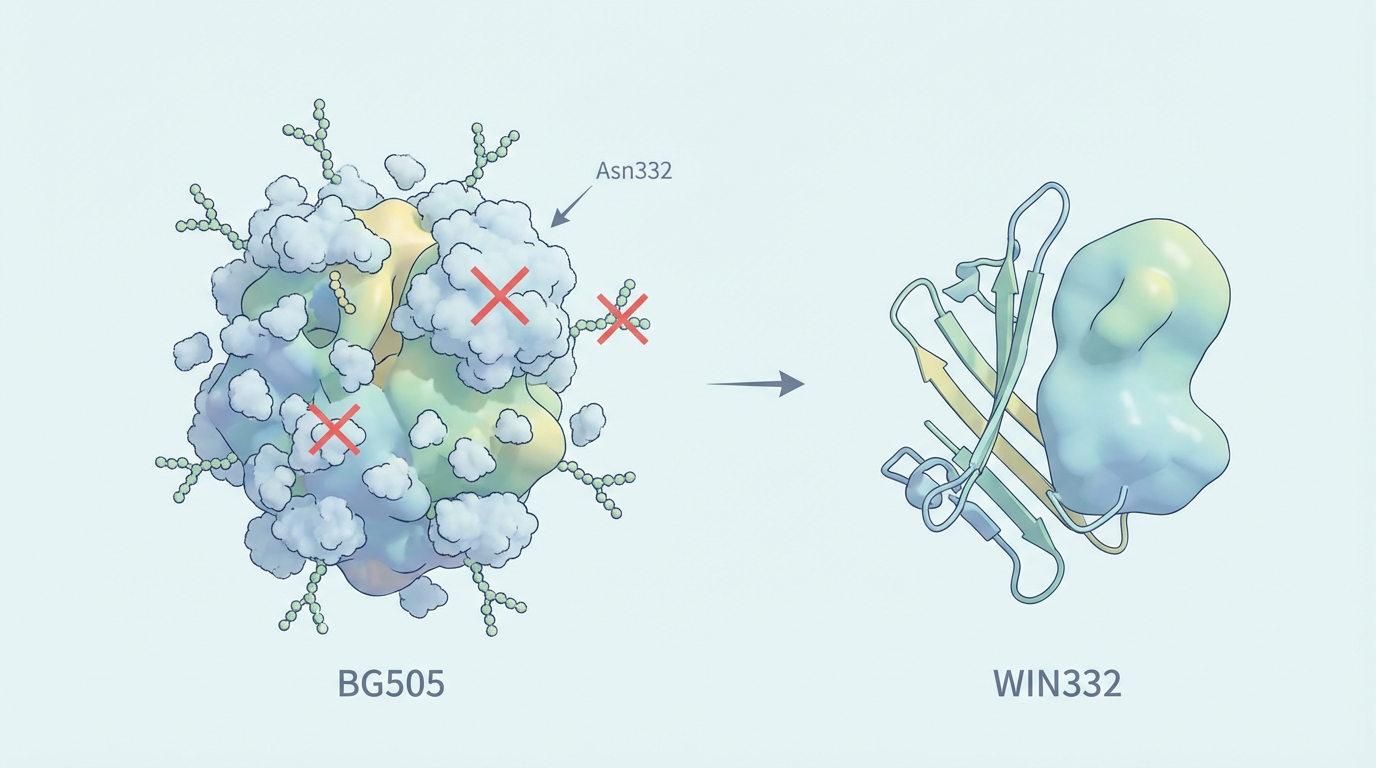
这一“拆糖”策略带来了意想不到的优势。WIN332不仅没有削弱免疫系统的识别能力,反而成了一把能打开两种锁的“万能钥匙”。它能同时激活两类广谱中和抗体的前体细胞:
这是HIV疫苗研发史上的首次。传统策略只专注于激活I型抗体,而WIN332开辟了双重战线。II型抗体的激活意义尤为重大,因为它们能有效对付那些天然缺失Asn332聚糖的传播毒株,从而极大地拓宽了疫苗的保护范围。实验数据显示,对于某些抗体前体,WIN332的结合亲和力甚至显著高于保留糖基的传统免疫原,证明“拆糖”反而提高了激活效率。
在非人灵长类动物实验中,WIN332的表现堪称惊艳。除了“单针起效”的速度优势,其诱导的免疫反应质量也颠覆了传统认知。
研究人员从实验动物体内分离出的抗体(如Ab1999和Ab1983),在基因序列和三维结构上,与人类已知的最强效广谱中和抗体(如BG18和EPTC112)高度相似。这意味着WIN332成功地在动物体内复刻了顶尖的人类免疫精英。
更重要的是,这些被激活的抗体达到中和病毒的水平,仅需经历极少量的体细胞突变(平均5.7个重链突变和2.8个轻链突变)。这与传统广谱中和抗体需要经历漫长、复杂且充满不确定性的“体内进化”(大量突变)才能成熟形成了鲜明对比。WIN332仿佛为免疫系统铺设了一条捷径,使其无需漫长的训练就能迅速形成战斗力。这正是实现“低门槛”免疫保护的关键一步。
其作用机制也呈现出巧妙的“双阶段激活”特征:
这种“先不依赖、后适应”的灵活模式,赋予了WIN332诱导的免疫反应前所未有的广谱潜力。
WIN332的突破,标志着HIV疫苗研发进入了一个新时代。它不仅有望将复杂的接种程序压缩至3针以内,大幅降低接种成本与实施难度,为全球公共卫生带来福音,其背后的“拆糖设计”理念更具有深远的科学意义。
对于乙肝、丙肝等同样依赖“聚糖盾牌”进行伪装的病毒,这一策略提供了全新的武器。通过精准地为病毒“卸妆”,科学家们或许能解锁更多前所未见的免疫通路,开发出更广谱、更高效的疫苗。
目前,WIN332已引起全球卫生机构的高度关注,其团队正在积极筹备人体临床试验。尽管从动物实验到临床应用仍有漫长的道路要走,但毫无疑问,这把“拆糖钥匙”已经为持续了四十年的科学马拉松注入了强劲的加速剂。人类终结艾滋病的梦想,从未像今天这样清晰和触手可及。
点击催更,成为大圆镜下一个视频选题!