对抗知识焦虑,从看懂这条开始
App 下载
耐药肝癌会派“无人机”,提前给肺“铺路”
复旦大学钦伦秀团队|信号无人机|细胞外囊泡|肺转移|耐药肝癌|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
复旦大学钦伦秀团队|信号无人机|细胞外囊泡|肺转移|耐药肝癌|肿瘤学|医学健康
晚期肝癌患者最害怕的不是肿瘤长大,而是它偷偷“跑”了。全球每年超75万人因肝癌离世,其中近半数患者倒在转移——尤其是肺转移。医生们曾以为,耐药的肝癌细胞是“打不死的小强”,靠自身硬实力闯到肺部。但复旦大学钦伦秀团队的最新研究彻底推翻了这个认知:耐药肝癌根本不是“硬闯”,而是提前派出了无数纳米级的“信号无人机”,远程把肺部改造成适合自己定居的“殖民地”。更关键的是,我们或许能用一款老药,直接掐断这条“铺路”的信号链。
这些被称为“细胞外囊泡”的纳米颗粒,是细胞分泌的直径仅几十到几百纳米的小泡——比头发丝细一千倍。它们像癌细胞释放的“漂流瓶”,顺着血液循环飘向全身,但耐药肝癌细胞的囊泡有精准的“导航系统”:表面富集的整合素ITGβ4,能精准识别肺部组织里的层粘连蛋白,一到肺就“锚定”下来。
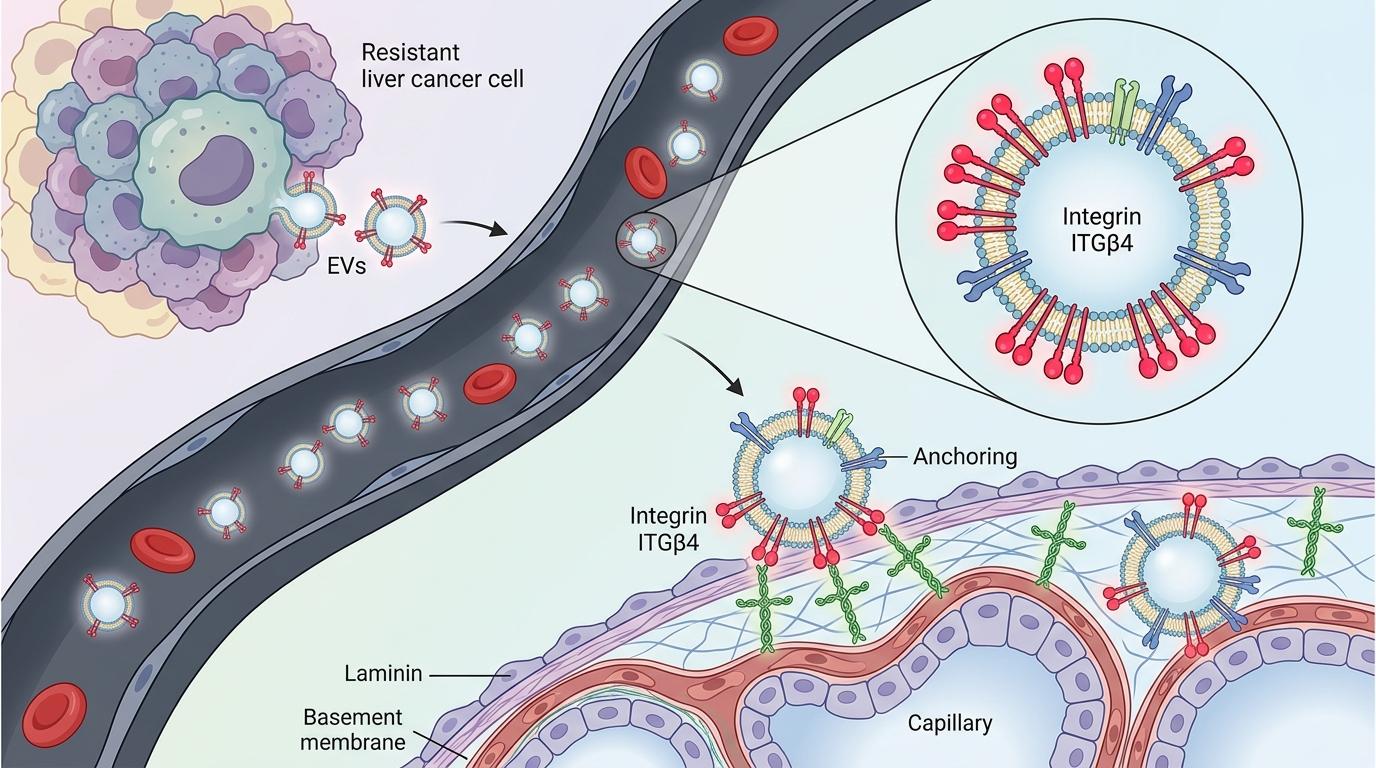
当这些囊泡被肺部的成纤维细胞“吞”下,真正的改造就开始了。囊泡携带的信号会激活成纤维细胞里的PI3K-AKT-p65通路,让原本安静的成纤维细胞变成“基建工人”,疯狂分泌促炎因子和促血管生成因子——相当于在肺里提前搭好“水电煤”,还铺上了“地毯”,就等耐药肝癌细胞过来“入住”。
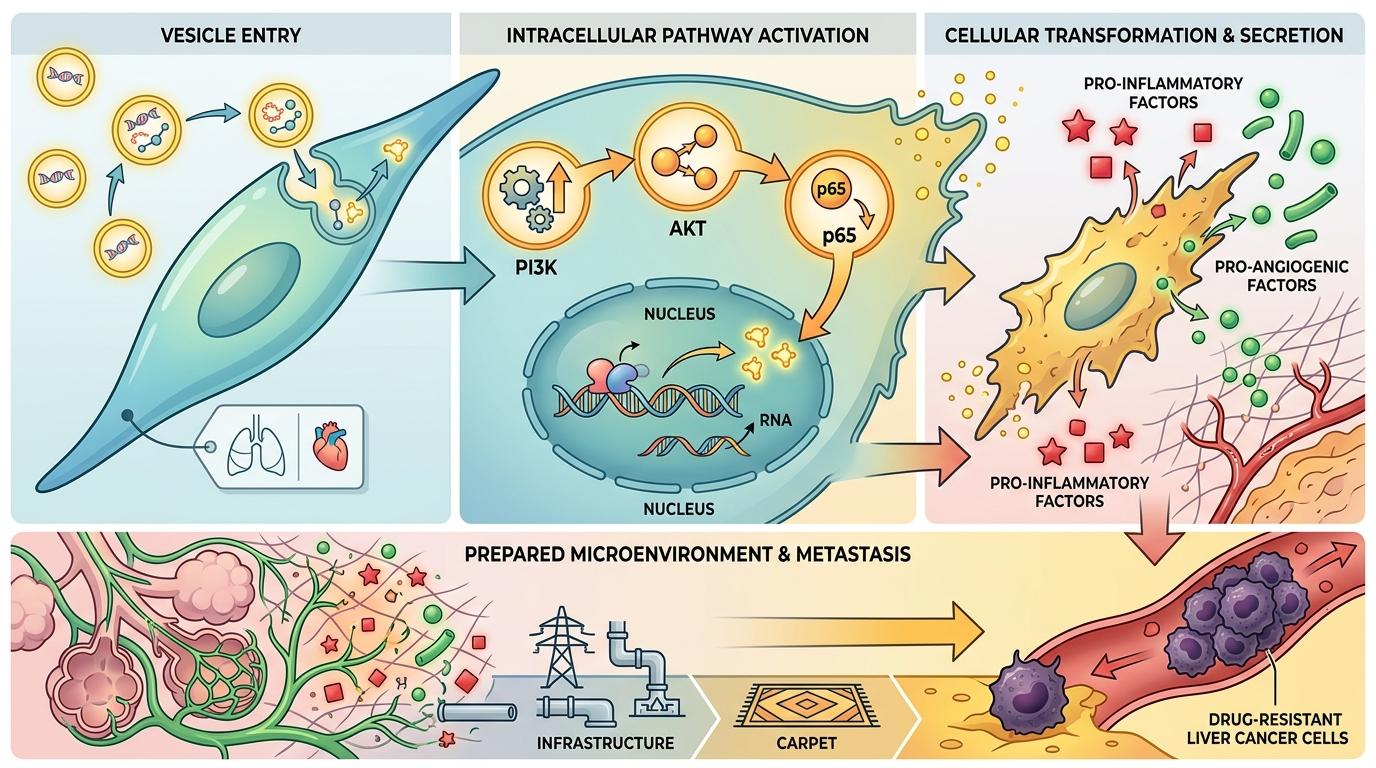
临床数据更证实了这个机制的残酷:对仑伐替尼耐药的肝癌患者,血液里这种带ITGβ4的囊泡数量,是敏感患者的3倍以上,而他们发生肺转移的风险,足足高了4.7倍。
为什么耐药肝癌细胞会释放这么多囊泡?研究团队追查到了源头:一条叫mTOR的信号通路在耐药细胞里异常激活了。
你可以把mTOR看成细胞里的“资源调度官”,它一旦过度激活,就会叫停细胞里的“垃圾回收站”——多囊泡体的自噬降解功能。原本该被细胞自己消化的囊泡,只能被一股脑地“吐”到细胞外。而雷帕霉素,这款已经在临床用了几十年的老药,恰好是mTOR的“抑制剂”。
实验数据直白得惊人:给耐药肝癌细胞用上雷帕霉素,mTOR通路被阻断,细胞的“垃圾回收站”重新开工,囊泡分泌量直接下降了60%;在小鼠模型里,仑伐替尼联合雷帕霉素的方案,让肺转移灶的数量减少了70%,小鼠的生存期延长了近一倍。
更重要的是,这个方案绕过了“开发新药”的漫长周期——两种都是已经获批的临床药物,意味着最快几年就能进入临床应用,给晚期患者带来实打实地希望。
当然,这个方案也不是万能的。研究团队在论文里明确提到,联合用药只能“抑制”转移,而不是彻底“消灭”耐药细胞——毕竟肝癌的耐药机制不止这一条,比如复旦大学樊嘉团队同期发现的神经生长因子通路,也是耐药的关键推手。
更现实的问题是,雷帕霉素本身有免疫抑制的副作用,长期使用可能增加感染风险。如何精准控制剂量,在“阻断囊泡分泌”和“保留免疫功能”之间找到平衡,是接下来临床研究要解决的核心难题。
但不可否认的是,这个研究给了我们一个全新的思路:对付癌症,不仅要“打敌人”,还要“拆后路”——与其等癌细胞转移后再被动治疗,不如提前切断它“铺路”的信号。
从“癌细胞靠硬实力转移”到“癌细胞靠信号铺路”,这个认知的转变,其实是人类对抗癌症的一个缩影:我们终于不再只盯着肿瘤本身,而是开始拆解它的“社交网络”——它如何和周围细胞对话,如何远程操控其他器官,如何给自己“创造生存条件”。
打蛇打七寸,抗癌断后路。未来的癌症治疗,或许不再是单一的“杀敌”,而是精准的“破局”——打断癌细胞的信号,破坏它的后勤,让它无处可去,无家可归。对晚期肝癌患者来说,这不是遥不可及的未来,而是触手可及的希望。