对抗知识焦虑,从看懂这条开始
App 下载
靶向纳米酶突破:类风湿关节炎治疗迎新范式?
破骨细胞|巨噬细胞|纳米酶|类风湿关节炎|自身免疫疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
破骨细胞|巨噬细胞|纳米酶|类风湿关节炎|自身免疫疾病|医学健康
对全球数千万类风湿关节炎(RA)患者而言,他们的身体就是一座持续交火的战场。免疫系统失控,将自身的关节滑膜误认为“敌人”,发起无休止的攻击。结果是剧烈的疼痛、关节肿胀变形,以及逐渐丧失的活动能力。这场战争悄无声息,却足以摧毁一个人的生活。
长久以来,医生们手握的“武器”——传统免疫抑制剂和生物制剂,虽能压制战火,却像无差别轰炸,在攻击“敌军”的同时,也对全身造成了附带伤害,引发严重的副作用。更关键的是,这些药物只能减缓破坏,却无法精准拆除驱动战争的核心引擎——失控的巨噬细胞与破骨细胞。一个更精准、更智能的“特种部队”亟待登场。
近日,这场战争迎来了新的转机。2026年1月5日,同济大学吴鹏、Huo Minfeng团队联合上海交通大学Xu Sudan团队在国际顶尖期刊 《Advanced Science》 上发表了一项突破性研究,揭示了一种名为 “自组装杨梅素-精氨酸偶联纳米酶(MANZs)” 的新型疗法,它如同一支装备了高精度导航系统的纳米特种兵,为类风湿关节炎的精准治疗带来了全新的范式与希望。
这项研究的核心成果在于,他们设计出一种无需任何外源载体、由天然分子自发组装而成的“智能药物”,能够精准识别并潜入战争的“指挥部”——促炎的M1型巨噬细胞,从内部瓦解其破坏力,并“策反”其成为和平的修复者。
要理解这一突破的意义,我们必须深入RA的病理战场。这个微环境有三大特征:
传统药物无法精准区分敌我,导致“杀敌一千,自损八百”。而一些早期的纳米载体策略,又因载药量低、潜在毒性以及缺乏有效的导航系统而难以走向临床。
同济大学的科学家们选择了一条回归自然、大道至简的路径。他们将两种天然存在的分子巧妙地结合在一起:
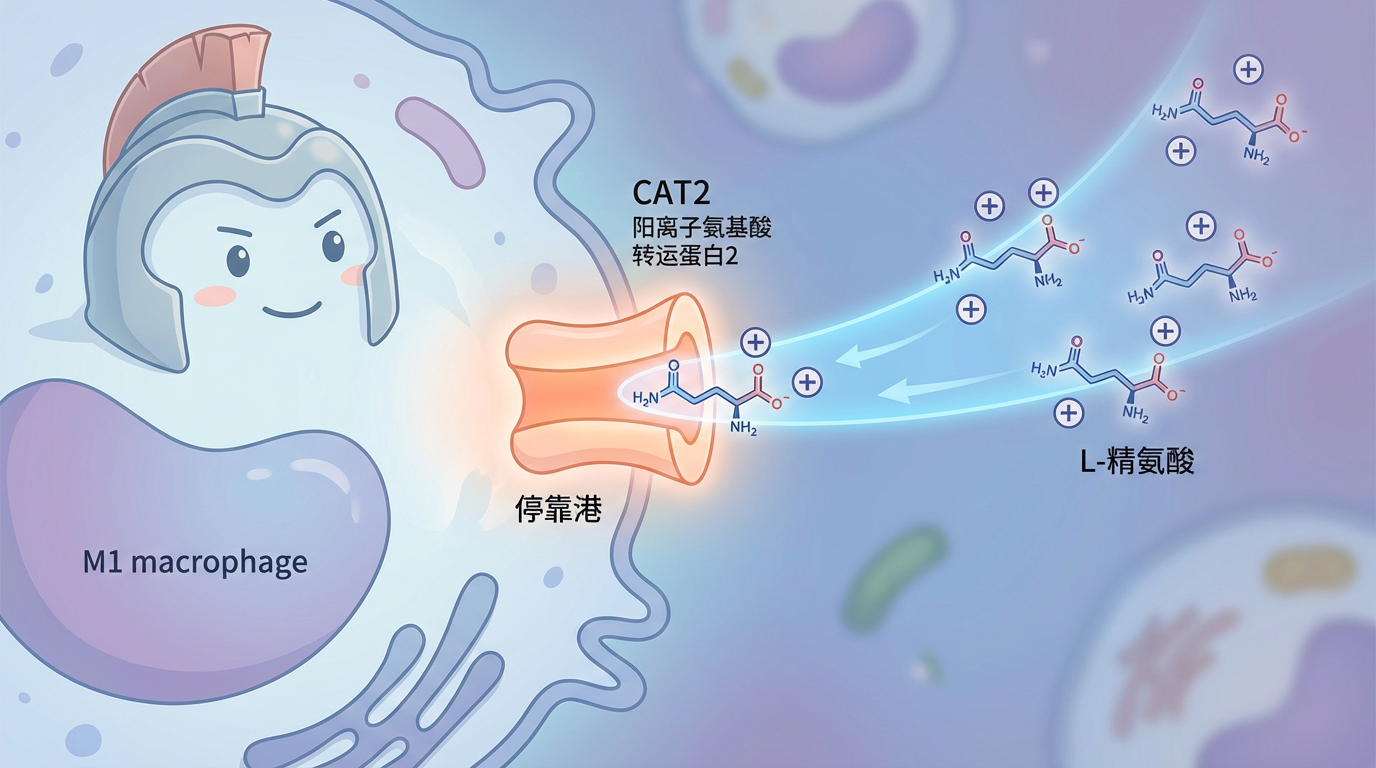
通过一步简单的化学反应(曼尼希反应),科学家将这两者共价连接,随后,这些分子依靠彼此间的引力(非共价相互作用)自发地聚集、组装成纳米颗粒——MANZs。这种设计摒弃了任何人工合成的载体,不仅生物相容性极高,也大大提升了“弹药”的装载效率。
一旦被注射到体内,这支纳米特种部队便开始了它们的“斩首”与“修复”行动。依托L-精氨酸的精准导航,MANZs大量富集在发炎的关节部位,并被M1型巨噬细胞通过CAT2通道“请君入瓮”。进入细胞内部后,MANZs立即上演了一场精彩的“三重奏”:
第一重:清除“化学武器”。杨梅素强大的抗氧化能力开始发挥作用,迅速清除细胞内外的活性氧(ROS),从根源上缓解了驱动炎症的氧化应激。
第二重:“策反”敌军。MANZs通过调控信号通路,将狂热的“主战派”M1型巨噬细胞“再教育”为温和的“维和派”M2型巨噬细胞。这些被转化的细胞不再释放炎症因子,反而开始分泌抗炎物质,促进组织修复。
第三重:叫停“拆迁队”。通过抑制关键的PI3K-Akt和TNF信号通路,MANZs直接切断了M1巨噬细胞向破骨细胞传递的“攻击指令”,有效阻止了骨侵蚀的发生。
在最能模拟人类RA病程的胶原诱导性关节炎(CIA)小鼠模型中,MANZs展现了惊人的疗效。接受治疗的小鼠,其关节肿胀显著减轻,滑膜炎症得到有效控制,更重要的是,通过Micro-CT扫描可以清晰地看到,它们的骨侵蚀被成功遏制。
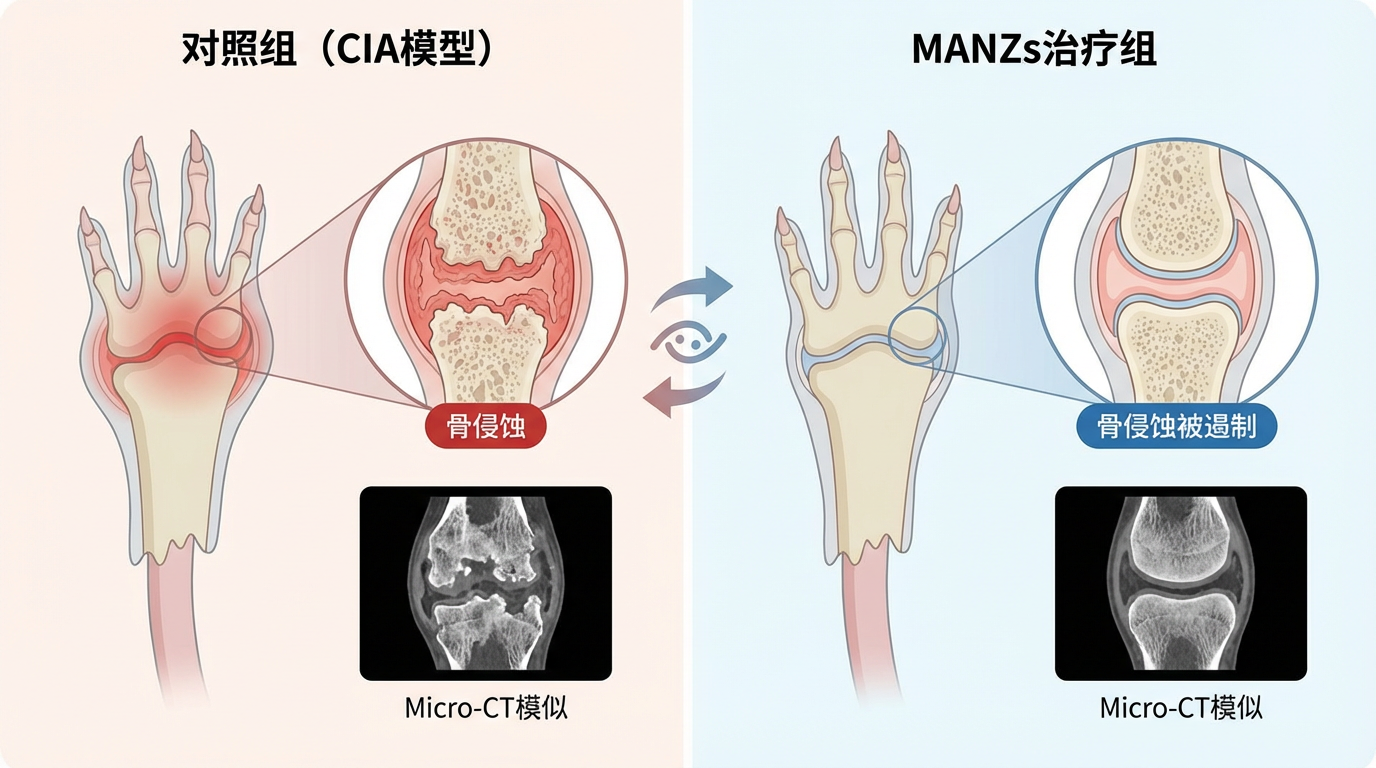
整个治疗过程中,小鼠并未表现出任何全身性的毒副作用,这证明了MANZs疗法的高度安全性与靶向性。它只在需要的地方开火,而不伤及无辜。
这项工作不仅仅是发表了一篇高水平论文,它更像是在黑暗中点亮了一盏明灯。它通过将天然分子巧妙整合,构建了一个无载体、高生物相容性、多功能协同的靶向治疗平台。与CAR-T等复杂且昂贵的细胞疗法相比,MANZs的设计理念更为简约、普适,展现出巨大的临床转化潜力。
当然,从实验室走向真正的临床应用,MANZs仍有很长的路要走,包括大规模生产的工艺优化、长期的安全性评估以及人体临床试验的验证。但无论如何,这项研究已经为攻克类风湿关节炎这座堡垒,提供了一种全新的、极具潜力的作战蓝图。它让我们相信,在不远的未来,人类或许终将赢得这场与自身免疫系统的“无声战争”。