对抗知识焦虑,从看懂这条开始
App 下载
肌动蛋白丝拧出超螺旋,解码细胞受力信号
力学信号传导|Alushin团队|细胞力学|超螺旋结构|肌动蛋白丝|分子细胞生物学|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
力学信号传导|Alushin团队|细胞力学|超螺旋结构|肌动蛋白丝|分子细胞生物学|生命科学
当你的心脏每一次收缩,当胚胎细胞慢慢拉扯出器官的轮廓,当癌细胞挤过坚硬的组织缝隙——这些生命动作的背后,都藏着同一个未解的谜题:细胞是怎么“感知”到力的?过去科学家只知道,有些蛋白质像“传感器”,能在受力时激活信号,但力到底如何在分子层面留下可被读取的痕迹,始终是个黑箱。直到2026年4月,洛克菲勒大学的Alushin团队在《Nature》上捅破了这层窗户纸:他们第一次“看见”,细胞里的肌动蛋白丝会在受力时拧出独特的“超螺旋”,而这,就是细胞能读懂的“力学密码”。
你可以把肌动蛋白丝想象成一根串着微小珠子的细弹簧——平时它是规整的螺旋,支撑着细胞的形状,就像帐篷的骨架。而肌球蛋白,就是在这根弹簧上“行走”的小马达,它会不断拉扯弹簧的两端,产生皮牛顿级的微小力量——这个量级有多小?相当于一根头发丝重量的十亿分之一。
但真实的机制比这更精确。
为了捕捉受力瞬间的变化,研究团队把冷冻荧光显微镜和冷冻电镜拧成了一套“组合拳”:先用荧光标记找到细胞里受力最集中的黏着斑区域,再用冷冻电镜把这些区域的分子结构“拍”成亚纳米级的高清快照。结果让所有人意外:原本笔直的肌动蛋白丝,在肌球蛋白的异步拉扯下,竟然拧出了左旋的“超螺旋”——每一圈螺旋的扭曲幅度只有几纳米,却足以改变整条丝的分子界面。
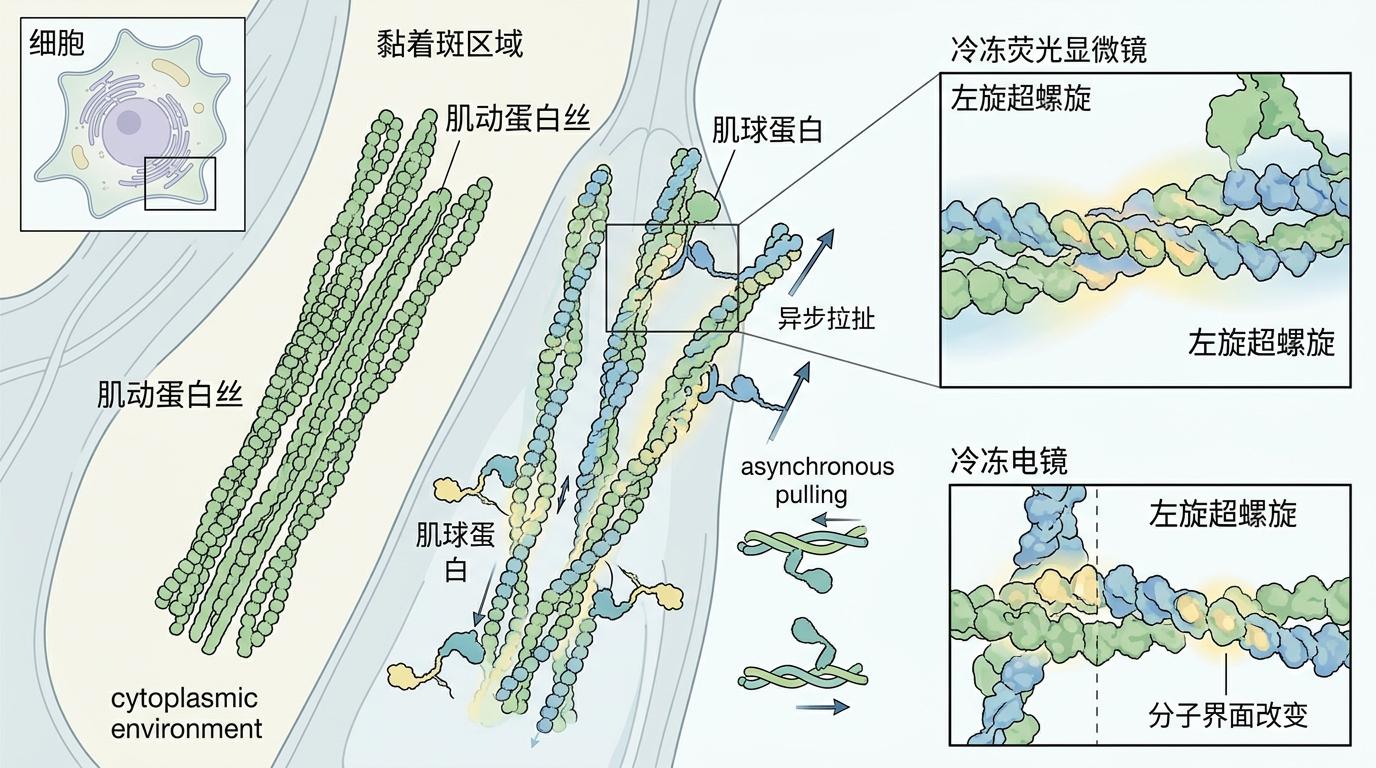
分子动力学模拟进一步证实,这种变形不是随机的:肌球蛋白就像一群不同步拉绳子的人,有的拉得快有的拉得慢,不均匀的力道让肌动蛋白丝的双链发生不对称扭曲,最终稳定成超螺旋结构。
超螺旋变形本身就是信号,但细胞得有能读懂它的“解码器”——α-连环蛋白就是这把钥匙。
你可以把α-连环蛋白想象成一个沿着肌动蛋白丝“走迷宫”的小人,它的脚只能卡在特定形状的凹槽里。当肌动蛋白丝处于松弛状态时,分子界面的间距太窄,它走得磕磕绊绊,很快就会掉下来;但当丝被拧成超螺旋,局部的分子界面被拉宽,刚好能卡住它的“脚”,它就能稳稳地沿着丝“行走”,同时激活下游的生化信号。
但真实的机制比这更巧妙。
三维结构分析显示,α-连环蛋白的结合不是单向的:它在识别超螺旋的同时,还会反过来“校正”肌动蛋白丝的扭曲——就像给拧变形的弹簧套上一个固定环,既稳定了信号的传递,又避免了丝被过度拉扯断裂。这种动态的相互调控,形成了一个“力-变形-信号-稳定”的闭环:力越大,超螺旋越明显,α-连环蛋白结合得越牢固,信号也就越强。
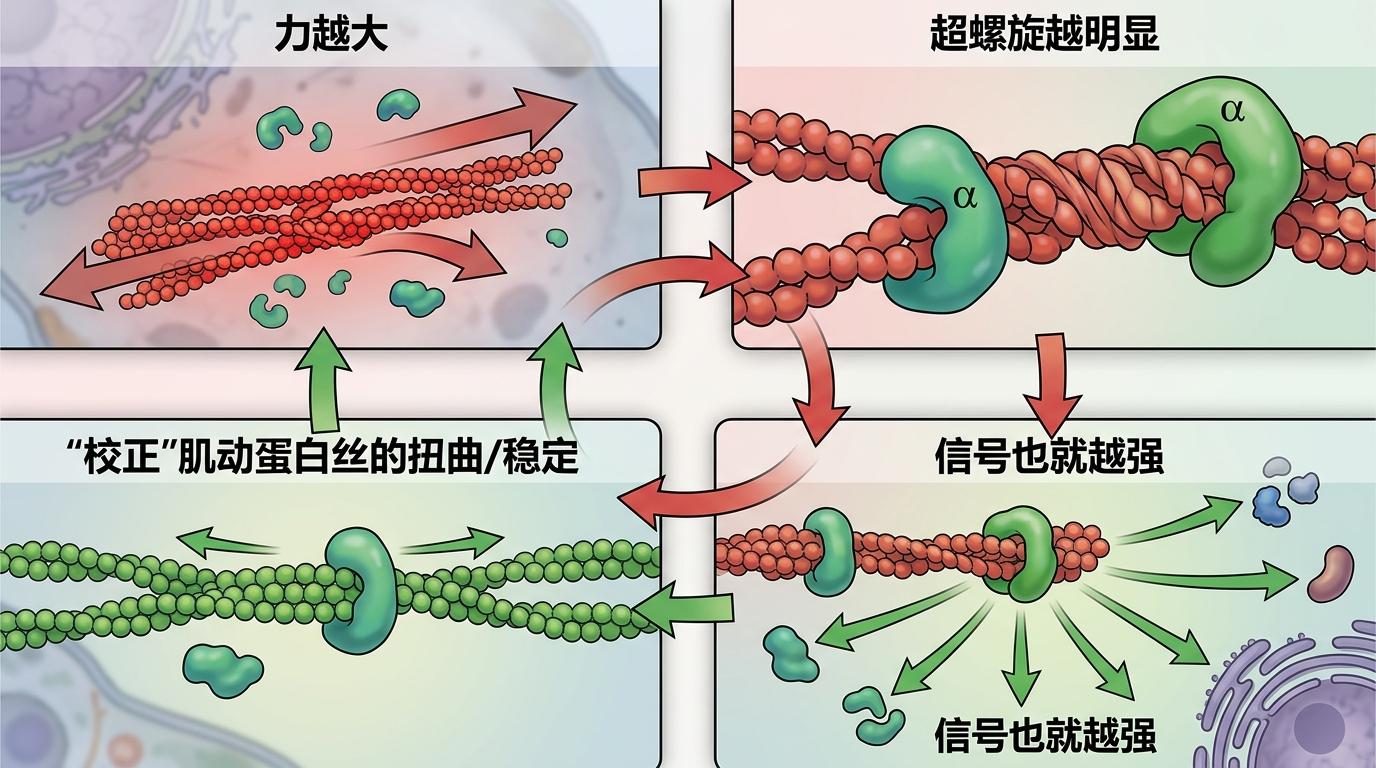
研究团队还做了一组对比实验:当他们用药物抑制肌球蛋白的活性,肌动蛋白丝恢复笔直,α-连环蛋白立刻从丝上脱落,下游信号也随之消失——这直接坐实了超螺旋作为力学信号的核心作用。
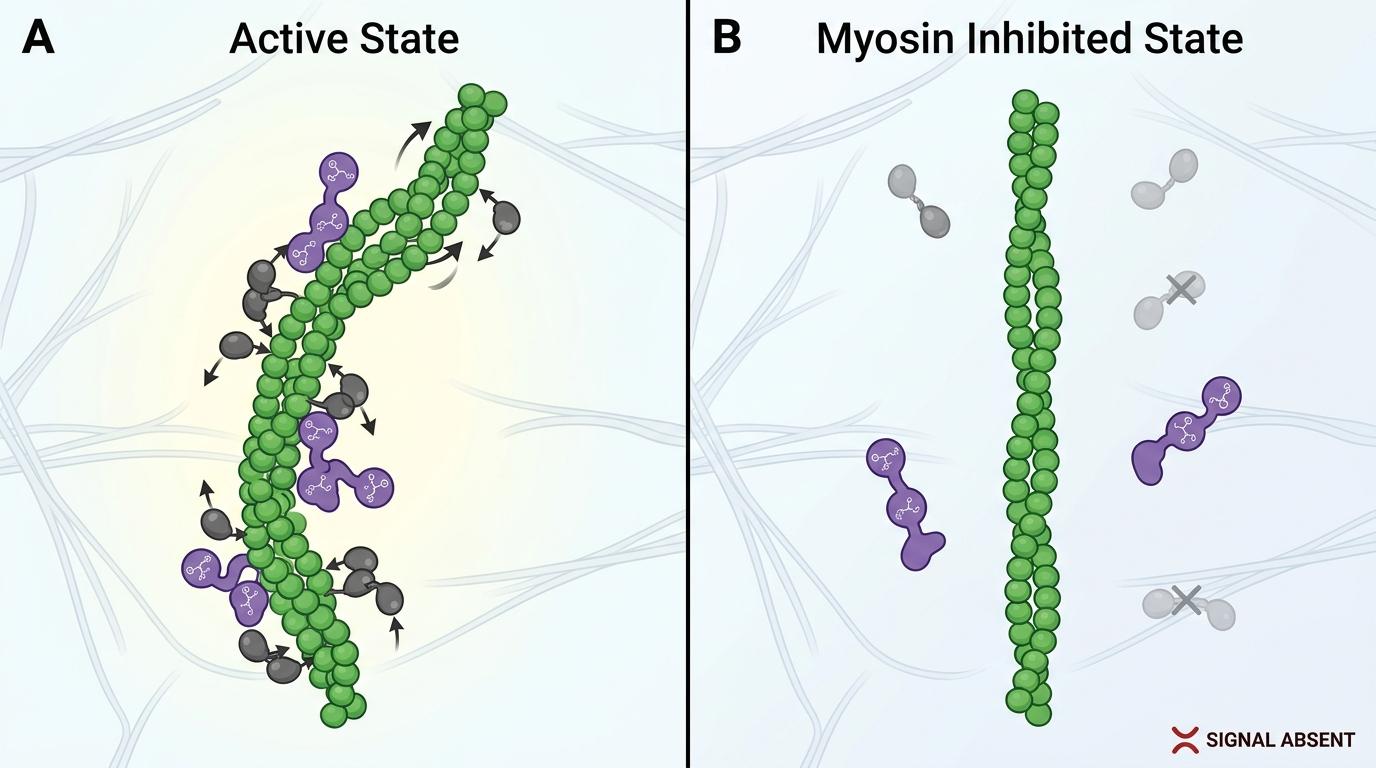
这项发现最有价值的地方,是它打破了人们对“机械信号转导”的固有认知:过去我们以为只有特定的“力学传感器”蛋白能感知力,现在才知道,细胞骨架本身就是一个动态的信号平台——它的结构变形就是信号,不需要额外的“传感器”来转换。
但它也有局限:目前的研究都是在体外重构系统和培养细胞中完成的,体内的环境要复杂得多——细胞里还有微管、中间纤维等其他骨架成分,它们会不会影响肌动蛋白丝的变形?不同组织的肌动蛋白丝受力状态差异巨大,超螺旋的变形规律会不会不一样?这些问题都还没有答案。
不过它的应用前景已经清晰可见:当机械信号失调时,很多疾病就会找上门——比如心肌细胞的肌动蛋白丝无法正常感知收缩力,会导致心力衰竭;纤维化组织里的肌动蛋白丝过度扭曲,会让组织越来越硬;肿瘤细胞的肌动蛋白丝能适应更坚硬的环境,帮助它们侵袭周围组织。如果能靶向α-连环蛋白与超螺旋的结合界面,就有可能精准纠正这些力学信号的失衡,为这些难治性疾病提供全新的治疗靶点。
我们总说生命是“化学的”,但这项研究让我们看到,生命也是“力学的”——从细胞的迁移到器官的发育,从心跳的节奏到肿瘤的侵袭,每一个生命过程都在和力对话。
力刻下结构,结构传递信号,信号决定命运——这就是细胞读懂“生命之力”的逻辑。未来,当我们能精准调控这根丝的扭曲,或许就能真正掌握生命的“力学开关”,让细胞按照我们期望的方式生长、修复、工作。而此刻,我们只是刚刚听懂了生命说的第一句“力学语言”。