
5 天前

5 天前
你体内每一个细胞的线粒体里,都藏着一串看不见的“珍珠项链”——这不是比喻,是瑞士洛桑联邦理工学院团队刚刚在活细胞里捕捉到的真实画面。过去一百年里,科学家只当这是细胞应激的异常表现,直到现在才发现:这串“珍珠”是线粒体用来精准分配DNA的秘密机制。它不用任何复杂的蛋白机器,只靠膜的物理特性,就解决了困扰学界几十年的难题:线粒体DNA怎么才能均匀分给每个子细胞?
线粒体是细胞的能量工厂,自带一套独立的DNA——也就是mtDNA,它负责编码13个维持能量生产的关键蛋白。这些DNA被打包成一个个直径约100纳米的“拟核”,像散在线粒体基质里的小汤圆。过去科学家一直以为,拟核的均匀分布全靠线粒体的融合和分裂,但敲除相关蛋白后,拟核居然还能保持规律排列。这说明,一定存在另一种更基础的机制。
直到Suliana Manley团队用超分辨率显微镜盯着活细胞看了无数小时,才把目光锁定在那个被忽视了百年的现象上:线粒体串珠化。当细胞内钙浓度升高,原本细长的线粒体管状结构会突然收缩,变成一串间隔均匀的“珍珠”——每个“珍珠”的中心恰好嵌着一个拟核。
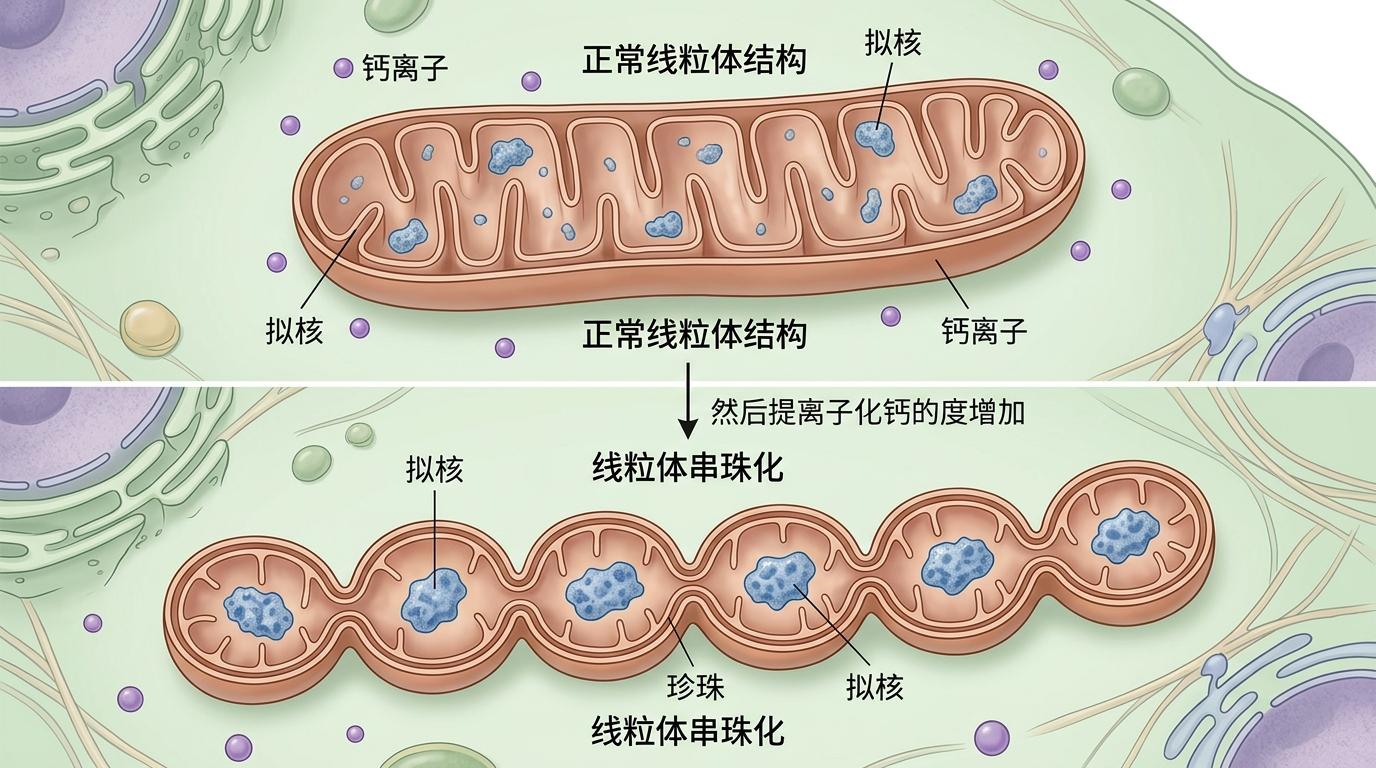
这个过程像极了物理课上的瑞利- Plateau不稳定性:就像水流过细管会变成均匀的水滴,线粒体膜的弹性和表面张力失衡时,自然会形成规则的串珠状。
串珠化不是随机发生的。团队发现,钙内流是触发这一过程的关键开关——当钙离子通过线粒体膜上的通道涌入基质,会改变膜的渗透压和张力,直接诱导线粒体形态转变。而线粒体内膜上的嵴结构,就像串珠的“定型器”:嵴的密度越高,串珠化的频率越低,形成的“珍珠”间距也越稳定。
他们做了一组对比实验:敲除负责维持嵴结构的Mic10蛋白后,线粒体的串珠化频率飙升了3倍,拟核的间距也变得杂乱无章;而用药物阻断钙内流,串珠化几乎完全停止,拟核开始聚集成团。
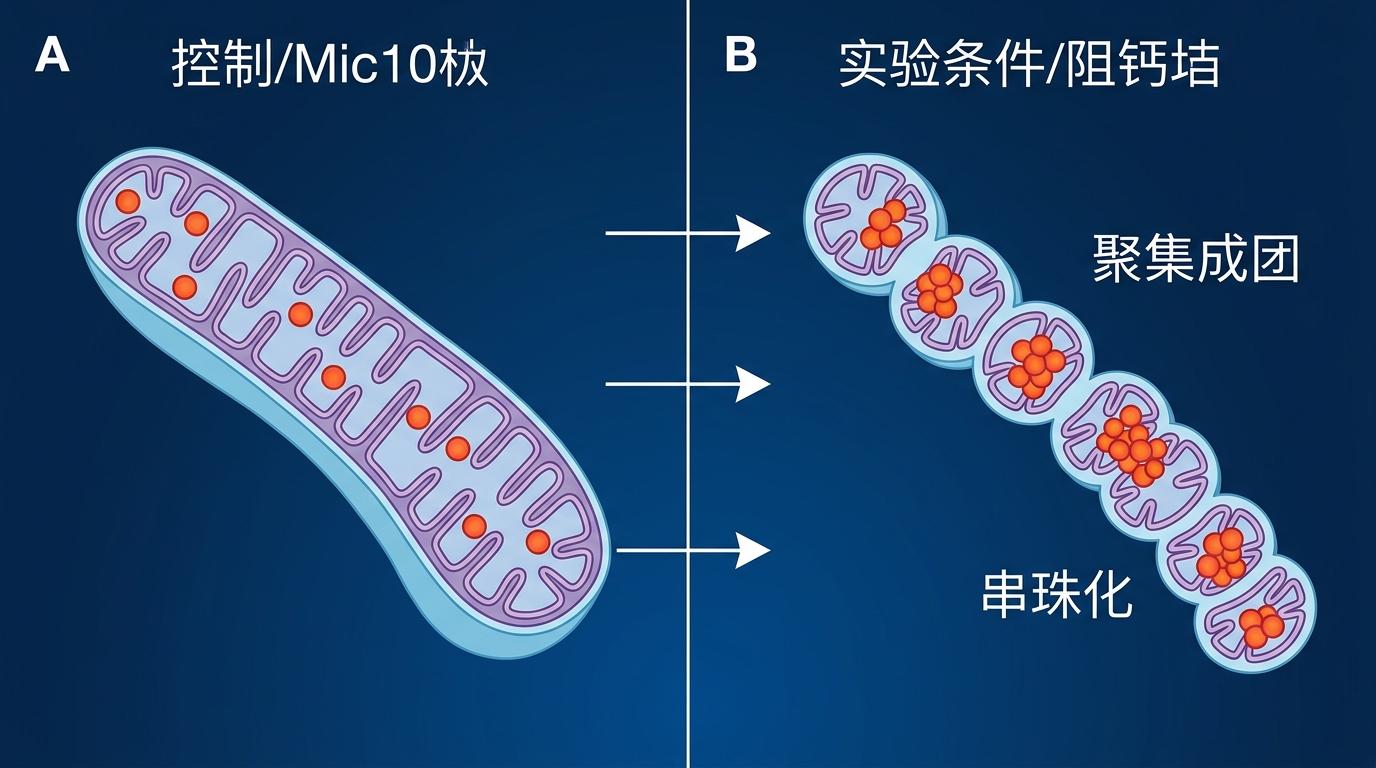
更关键的是,这个过程是可逆的。当钙浓度回落,串珠会重新变回管状线粒体,但拟核已经被精准地分散到了整个网络里——就像有人用尺子量过一样,每个拟核之间的误差不超过100纳米。
串珠化的意义远不止“让DNA排好队”。当拟核均匀分布时,线粒体的基因表达会更均衡,能量生产也更稳定;一旦这个机制失效,拟核聚集在一起,就会导致mtDNA拷贝数失衡,进而引发能量代谢障碍。
团队在实验中观察到,当钙内流失调或者嵴结构被破坏时,细胞内的拟核会大量聚集,mtDNA的遗传稳定性急剧下降——这正是线粒体肌病、帕金森病等神经退行性疾病的典型特征。换句话说,串珠化的异常,可能是这些疾病的早期诱因之一。
不过目前的研究还存在局限:团队只在哺乳动物细胞和酵母中验证了这一机制,它是否存在于所有真核生物中?不同细胞类型里的串珠化调控是否有差异?这些问题还需要更多实验来回答。
过去我们总以为,生命的精密调控全靠复杂的蛋白和信号通路,却忘了最基础的物理规律也在悄悄发挥作用。线粒体用一串“珍珠”告诉我们:生命的智慧,有时候就藏在膜的张力和弹性里。
“物理规律,是生命最古老的调控密码。”这或许是这项研究最动人的启示——当我们在分子世界里寻找答案时,不妨抬头看看那些更基础的法则,它们可能早已在细胞里运行了几十亿年。未来,或许我们能通过调控串珠化过程,为线粒体疾病找到新的治疗方向,但此刻,先为这串藏在细胞里的“珍珠”惊叹就够了。
点击充电,成为大圆镜下一个视频选题!