对抗知识焦虑,从看懂这条开始
App 下载
激酶“幽灵”状态首度捕获,颠覆癌症药物设计?
T细胞激活|细胞信号传导|磷酸化位点|蛋白激酶|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
T细胞激活|细胞信号传导|磷酸化位点|蛋白激酶|肿瘤学|医学健康
在每一个细胞内部,都有一场永不停歇、以微秒计的芭蕾舞。生命活动,从细胞迁移到免疫反应,都依赖于信号的精确传递。这场舞蹈的核心指挥家,是一类被称为蛋白激酶的蛋白质。它们如同细胞世界的信使与开关,通过将能量分子ATP上的磷酸基团“贴”到底物蛋白上,瞬间改变其功能,从而发出指令。
然而,这个过程隐藏着一个近乎悖论的难题。对于许多关键任务,如T细胞激活或伤口愈合时的细胞迁移,激酶不能只“贴”一次标签就离开。它需要像一台高速冲压机,在紧紧抓住同一块“钢板”(底物蛋白)的同时,连续在其表面冲压出多个“印记”(磷酸化位点)。这种被称为**“连续性磷酸化”**(processive phosphorylation)的机制,要求激酶在完成一次催化后,以惊人速度排出反应废物——ADP分子,并立即装填新的ATP“燃料”,准备下一次冲压。问题是,一个紧紧抓住钢板的机器,如何能同时以闪电般的速度排出内部废料?这个矛盾长期困扰着生物学家。
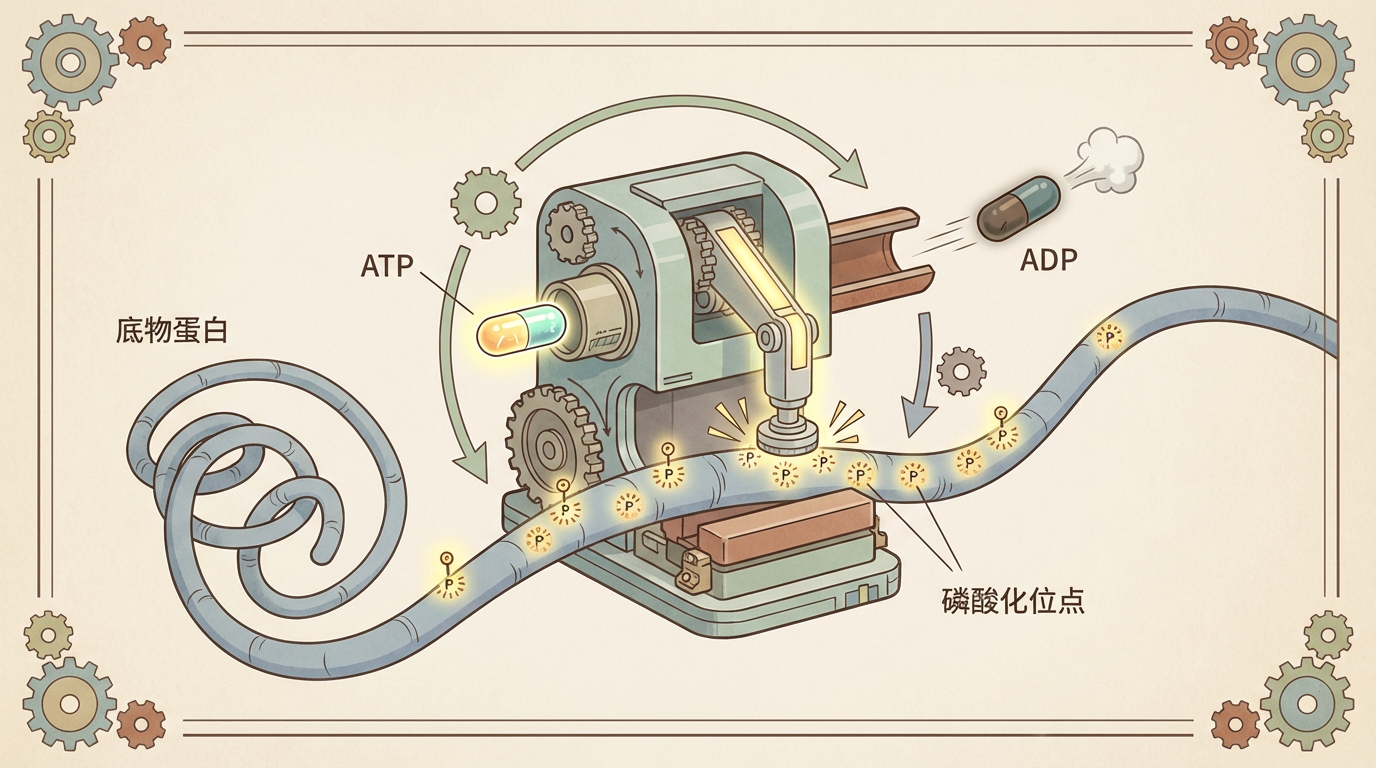
直到最近,一扇通往全新分子世界的大门被悄然推开。科学家们捕捉到了一个此前从未被观察到的“幽灵”状态,它如同一部机器中转瞬即逝的齿轮,完美解决了这个悖论,也为我们理解生命调控的精度和未来的药物设计,带来了颠覆性的启示。
近日,圣裘德儿童研究医院(St. Jude Children’s Research Hospital)结构生物学系主任Charalampos Babis Kalodimos博士领导的团队,在顶尖期刊**《Science》上发表了一项突破性研究。他们首次直接观察并解析了Src激酶家族中一种寿命极短的“隐藏中间态”**(hidden intermediate state)。
这项研究的核心发现是:
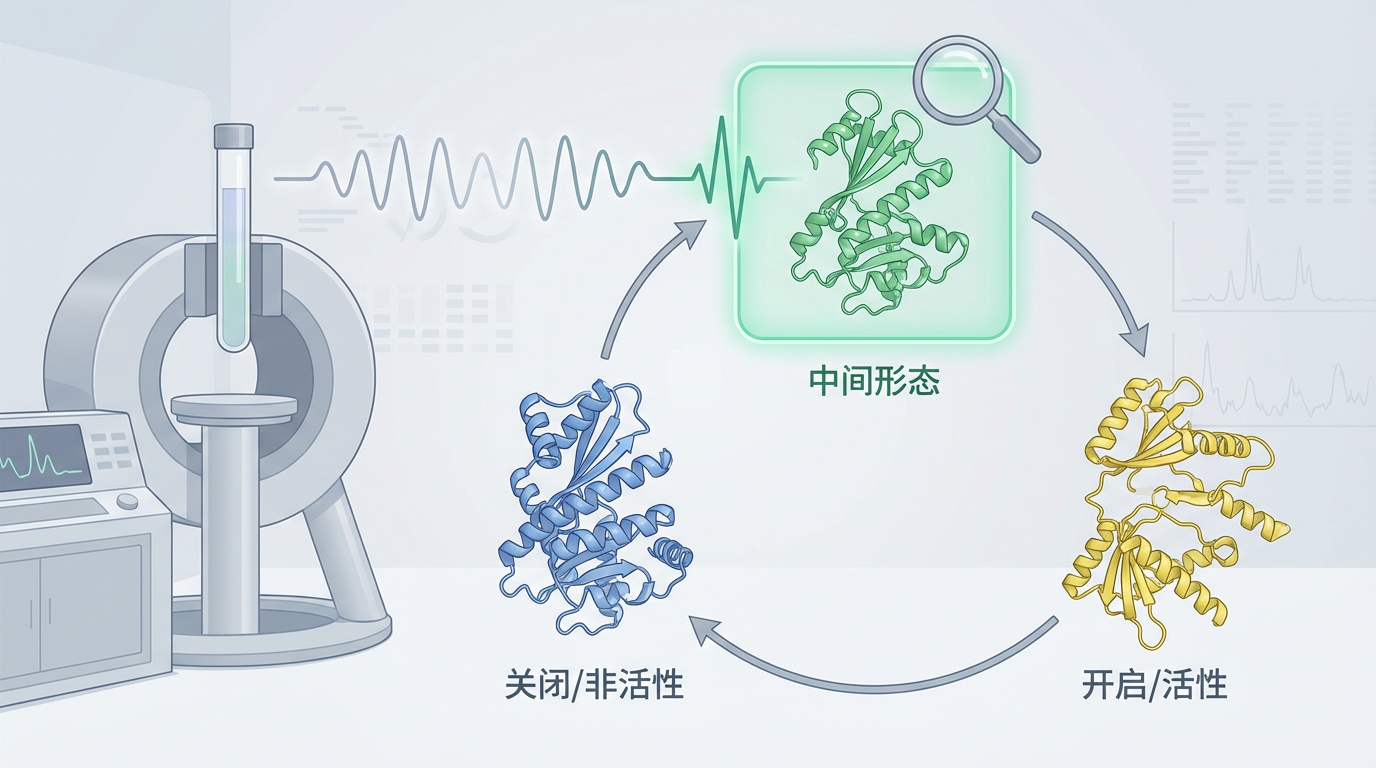
这项由崔一昕博士担任独立第一作者的研究,如同一部超高速摄像机,记录下了分子机器内部最核心的运作秘密。它雄辩地证明,生命的精确调控,不仅依赖于我们能看到的稳定结构,更依赖于这些难以捕捉的、转瞬即逝的动态过程。
长期以来,我们对蛋白质的理解主要依赖于X射线晶体学等技术,它们能拍出蛋白质清晰的“定妆照”,展示其稳定的三维结构。这帮助我们识别了激酶的“开启”和“关闭”两种主要状态,也催生了第一代靶向药物。然而,这些静态照片无法解释激酶如何实现高速的连续催化。
Kalodimos博士的团队另辟蹊径,他们所使用的核磁共振(NMR)技术,更像一部能够捕捉分子运动的“电影摄影机”。通过追踪激酶上百个原子在皮秒至毫秒时间尺度上的微小振动与构象变化,他们最终拼凑出了一个包含“开启态”、“关闭态”和这个全新“中间态”的三态动态平衡模型。
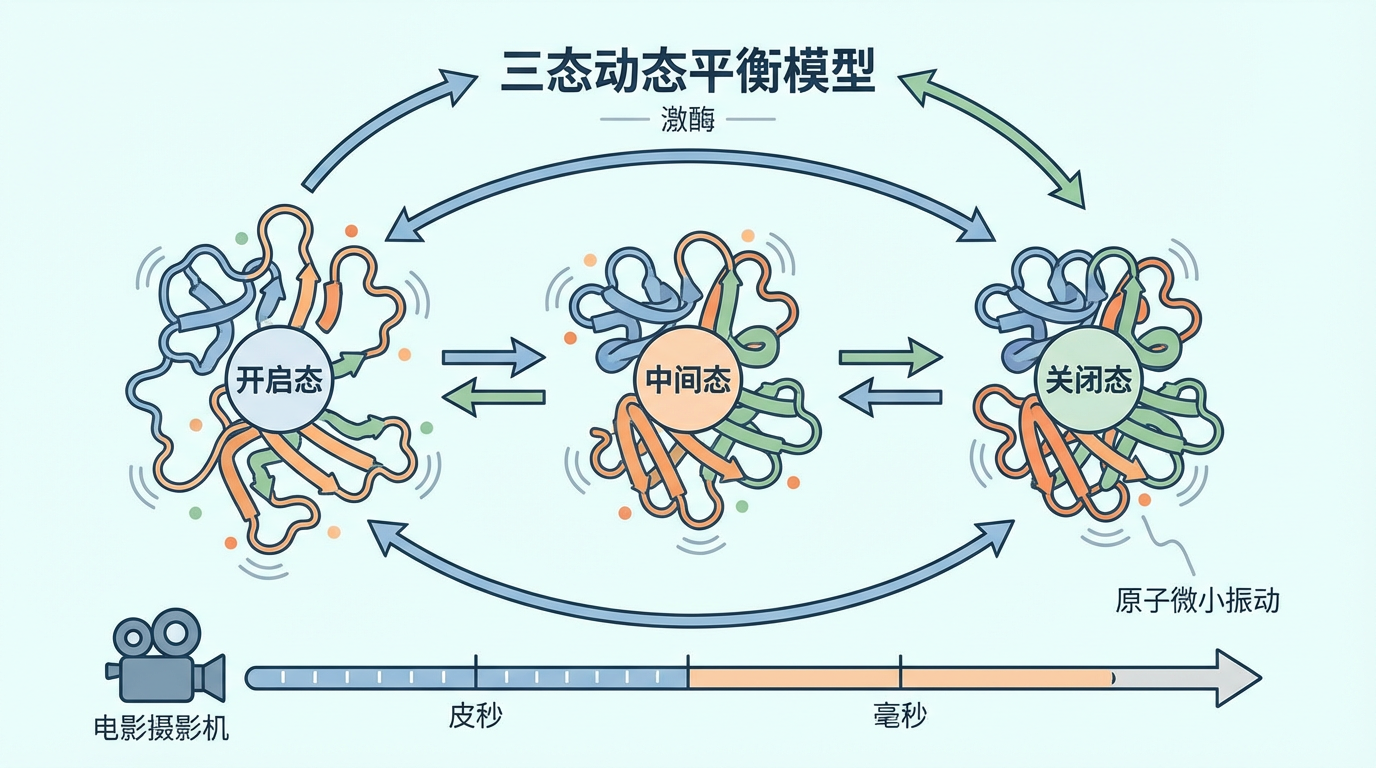
这项工作不仅是一次科学发现,更是一次技术驱动的认知飞跃。它告诉我们,要真正理解生命的运作,就必须从观察静态的“零件”转向研究动态的“机器”。Kalodimos团队正致力于利用NMR、冷冻电镜(Cryo-EM)等前沿结构生物学手段,系统地绘制人类激酶组的动态图谱,以期揭示更多关于癌症和药物抗性的深层机制。
这一发现的意义远远超出了基础生物学领域,它为药物研发和疾病治疗打开了一扇全新的大门。
目前,全球每年投入数百亿美元研发的激酶抑制剂,绝大多数靶向的是激酶稳定存在的“开启”或“关闭”状态。这就像试图通过卡住汽车的点火开关或直接拔掉电池来让它熄火。这种方法虽然有效,但往往因为激酶家族成员结构相似而导致“误伤”(脱靶效应),引发副作用。此外,癌细胞也常常通过突变开关结构来产生耐药性。
而“隐藏中间态”的发现,提供了一个前所未有的精准靶点。这个状态的构象是独特的,且只在激酶高速运转时短暂出现。这意味着,如果能设计出一种只结合这个中间态的小分子药物,就可以实现前所未有的特异性。这相当于不再是粗暴地切断电源,而是像一位高明的机械师,精确地在机器高速运转的特定瞬间,插入一根销钉,使其安全停机,且不影响其他正常机器。
这一思路在以下领域具有巨大的应用潜力:
正如Kalodimos博士所言,目前我们对激酶构象景观的认识仍然非常有限,这项工作只是揭开了冰山一角。Src家族的这一“生存绝技”在亿万年的进化中被高度保守,暗示着类似的隐藏状态可能广泛存在于人类500多种激酶乃至其他蛋白质家族中。
我们正处在一个结构生物学新时代的黎明。随着技术的不断进步,我们将有能力观察到越来越多曾经“不可见”的分子事件。每一个新发现的短暂状态,都可能是一个潜在的药物靶点,一种调控生命过程的新方法。
从一个转瞬即逝的分子构象,到对细胞行为的精确调控,再到颠覆性的疾病治疗策略,这项研究完美地展示了基础科学的强大力量。它提醒我们,在生命最微观的尺度之下,隐藏着最高效、最精妙的设计。而人类的智慧,正在一步步学会阅读并运用这本来自大自然的“设计手册”,为攻克顽疾带来新的希望。