内容由AI生成,思考得你完成
App 下载
内容由AI生成,思考得你完成
App 下载
你可能不知道,每3秒全球就有一起骨质疏松性骨折发生——50岁以上女性里,每3个就有1个会遭遇这种“无声的骨折”。我们总把骨质疏松当成“骨头变脆”的老化问题,却忽略了它本质是一场骨骼里的攻防战:破骨细胞像过度活跃的拆迁队,啃食骨质的速度远超成骨细胞的修复速度。
苏州大学的研究团队最近挖到了这场战争里的关键“指挥官”——Gαi1/3蛋白。它就像破骨细胞的加速按钮,一旦失控,骨质流失会被直接拉满。更意外的是,抑制它的效果,居然和目前一线治疗药物地舒单抗几乎一样。这到底是怎么做到的?
要理解Gαi1/3的作用,得先搞懂骨骼里的核心调控通路——RANKL信号轴。你可以把它看成破骨细胞的“启动指令”:成骨细胞和免疫细胞分泌的RANKL,就像一把钥匙,插进破骨细胞前体表面的RANK受体锁孔里,激活下游的TRAF6蛋白,随后一系列信号通路被打通,最终催生能啃食骨质的成熟破骨细胞。
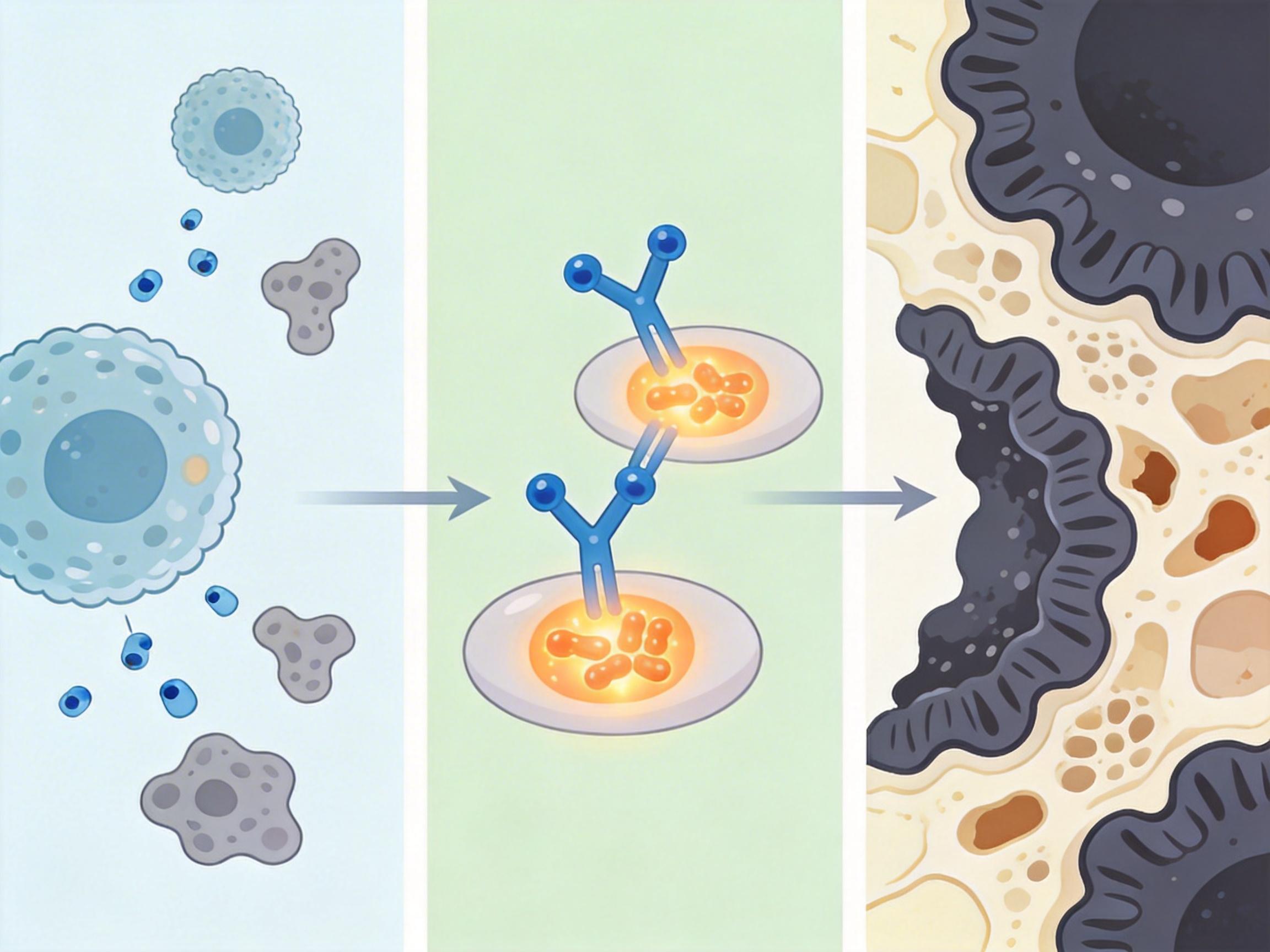
过去大家都以为,RANK和TRAF6的结合是这套系统的核心。但苏州大学的研究发现,Gαi1/3才是藏在背后的“隐形搭扣”——它的第173位天冬氨酸,是RANK和TRAF6能牢牢粘在一起的关键。没有这个位点,钥匙就算插进锁孔,也转不动齿轮。
研究团队做了一组对比实验:把小鼠破骨前体细胞里的Gαi1/3敲除,就算用RANKL强力诱导,破骨细胞的形成能力也直接下降了60%;反过来,给细胞过表达Gαi1/3,破骨细胞的分化速度和骨吸收能力翻了一倍还多。
更关键的临床证据是:骨质疏松患者和卵巢切除后的骨质疏松小鼠骨髓里,Gαi1/3的水平比健康个体高了近3倍——这意味着,它就是骨质流失的“信号灯”。
既然Gαi1/3是破骨细胞的“加速按钮”,那按住它会发生什么?
团队给卵巢切除的骨质疏松小鼠用了Gαi1/3抑制剂,结果和注射地舒单抗的小鼠几乎一模一样:骨小梁的厚度增加了28%,骨体积分数提升了32%,原本被啃得千疮百孔的骨结构,重新变得致密。
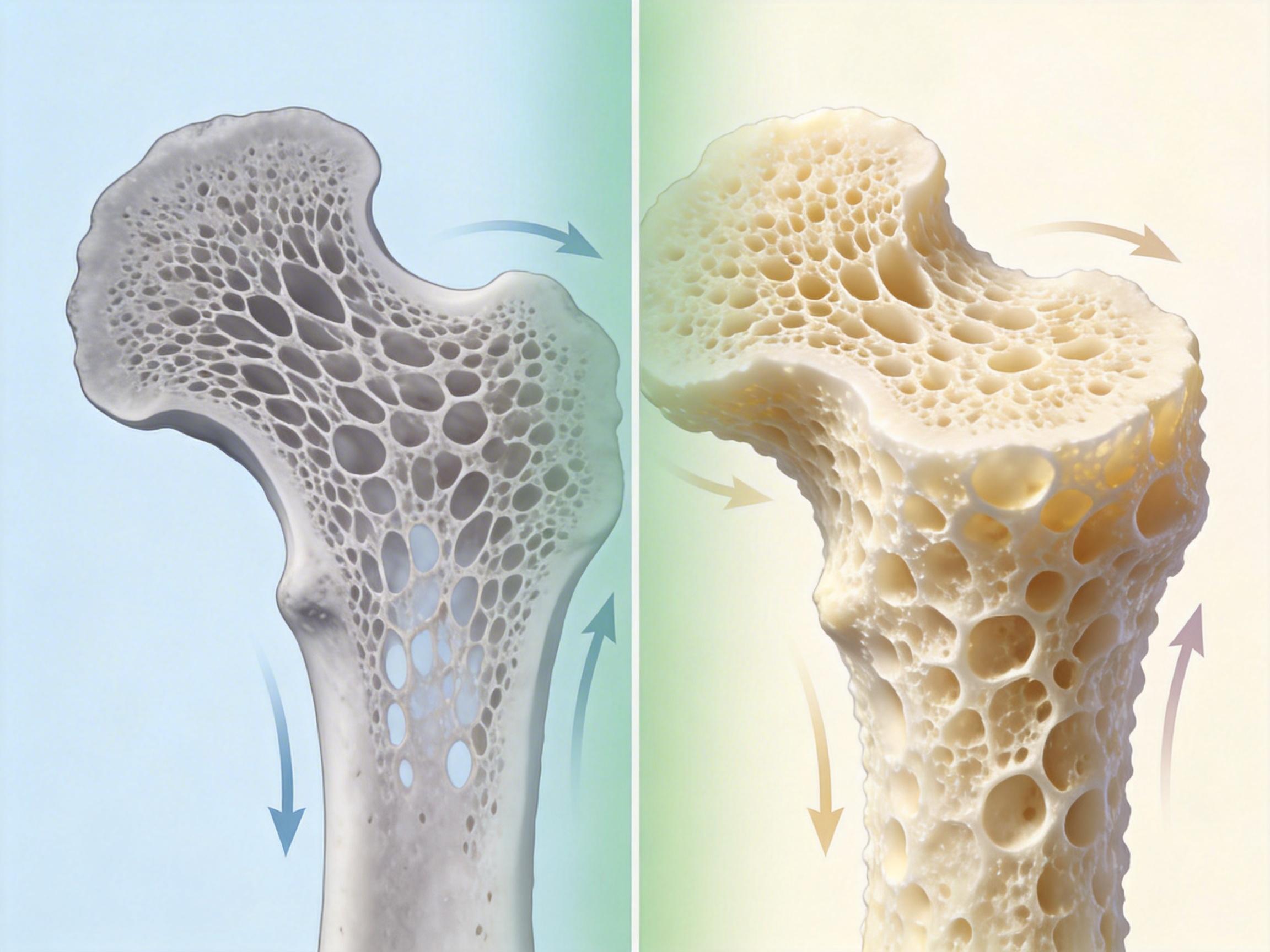
有意思的是,当他们把小鼠的Gαi1/3敲除后再用地舒单抗,药物的保护作用直接打了对折——这说明,地舒单抗的疗效,很大程度上依赖Gαi1/3的存在。换而言之,Gαi1/3是RANKL通路里的“必经关卡”,不管是用抗体阻断RANKL,还是直接抑制Gαi1/3,最终都是掐断了破骨细胞的“动力源”。
我认为,这是研究最有价值的地方:它不仅找到了新靶点,还把现有药物的作用机制补全了。过去我们只知道地舒单抗能“锁死”RANKL,现在才明白,它最终是通过Gαi1/3这个节点,阻止了破骨细胞的过度激活。这为未来开发更精准、副作用更小的药物,铺了一条清晰的路。
Gαi1/3的另一个特殊之处,在于它是骨骼和免疫系统的“交叉点”。它本来就是免疫细胞里的信号分子,调控着巨噬细胞的极化和炎症反应——而破骨细胞,恰恰是从单核/巨噬细胞分化来的。
这就解释了为什么绝经后女性容易得骨质疏松:雌激素缺乏不仅直接影响骨骼,还会激活免疫系统,让免疫细胞分泌更多RANKL,同时上调Gαi1/3的表达,相当于给破骨细胞踩了双重油门。
研究团队还发现,Gαi1/3缺失的小鼠,骨髓里的炎症因子水平直接下降了40%。这意味着,抑制Gαi1/3不仅能阻止骨质流失,还能同时调节骨骼微环境的炎症状态——这是现有药物不具备的额外优势。毕竟,很多骨质疏松患者同时伴随慢性炎症,单一靶点能解决两个问题,在临床上的价值不言而喻。
当我们把骨质疏松当成“老化问题”时,能做的只有补钙、晒太阳,或者用药物强行抑制破骨细胞。但Gαi1/3的发现,让我们看到了更精准的可能:找到骨质流失的“核心开关”,从根源上调节骨骼的攻防平衡。
未来的骨质疏松治疗,或许不再是“一刀切”地抑制骨吸收,而是通过调控Gαi1/3这样的节点,让破骨细胞和成骨细胞重新回到平衡状态。毕竟,健康的骨骼从来不是“不被破坏”,而是破坏和修复的动态平衡——这也是所有生命系统的底层逻辑:
骨之稳态,在于平衡而非静止。
骨之稳态,在于平衡而非静止。