
1 个月前

1 个月前
你可能没听说过铁死亡——一种由铁元素失控引发的细胞“氧化自杀”,却是免疫系统清除癌细胞的秘密武器。但肺腺癌偏偏能绕开这道生死关:只有约20%的患者能在免疫治疗中获得持久应答,剩下的癌细胞总能悄悄躲避免疫系统的追杀。
2026年3月,中国医学科学院肿瘤医院高树庚、刘芝华团队的研究,终于揪出了这场逃逸的“主谋”:一种名叫BZW1的蛋白。它像个潜伏在细胞里的“铁管家”,死死按住铁死亡的开关,帮癌细胞在免疫系统的眼皮底下活下去。为什么它能有这么大的能量?这得从铁死亡的底层逻辑说起。
我们可以把铁死亡想象成一场厨房火灾:细胞里的铁离子是易燃的柴火,脂质过氧化是火苗,一旦火势失控,细胞就会被烧得“灰飞烟灭”。而免疫系统恰恰是这场火灾的“点火人”——当CD8+T细胞识别出癌细胞,就会分泌干扰素-γ,拆毁癌细胞的“防火设备”,逼着它启动铁死亡。
但癌细胞进化出了一套“灭火系统”:铁蛋白。这种由FTH1蛋白组成的“铁罐子”,能把游离的铁离子牢牢锁起来,让脂质过氧化没了燃料。而负责销毁“铁罐子”的,是一种叫NCOA4的“拆罐工”——它会把铁蛋白运到溶酶体里拆解,释放出铁离子。
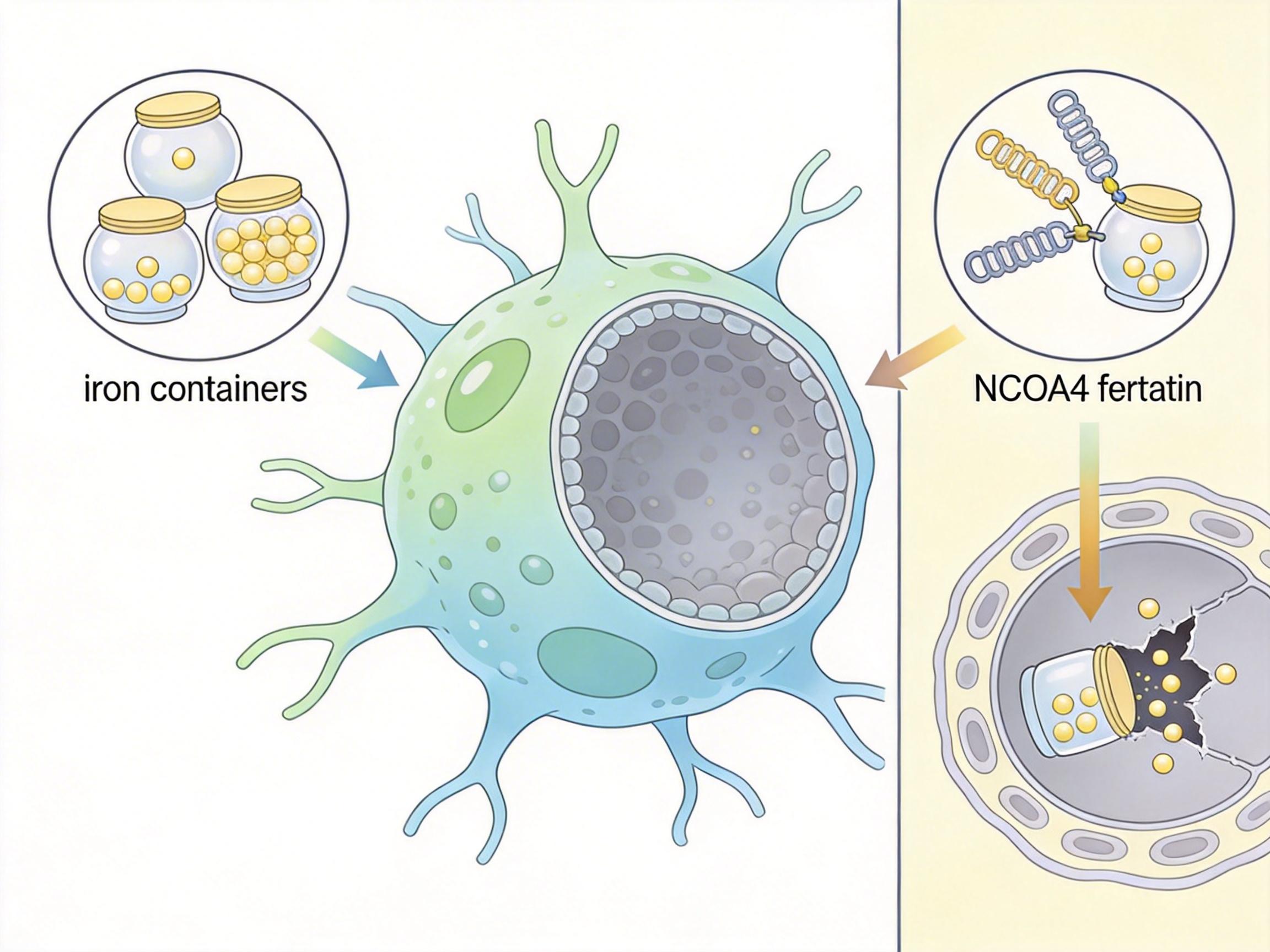
BZW1的坏心思就藏在这里。它有两招:一是直接把“拆罐工”NCOA4偷偷降解,让铁蛋白没人敢碰;二是自己抢着和NCOA4结合,硬生生把它和铁蛋白拆开。这样一来,铁离子被死死锁在“罐子”里,脂质过氧化烧不起来,铁死亡自然也就启动不了。
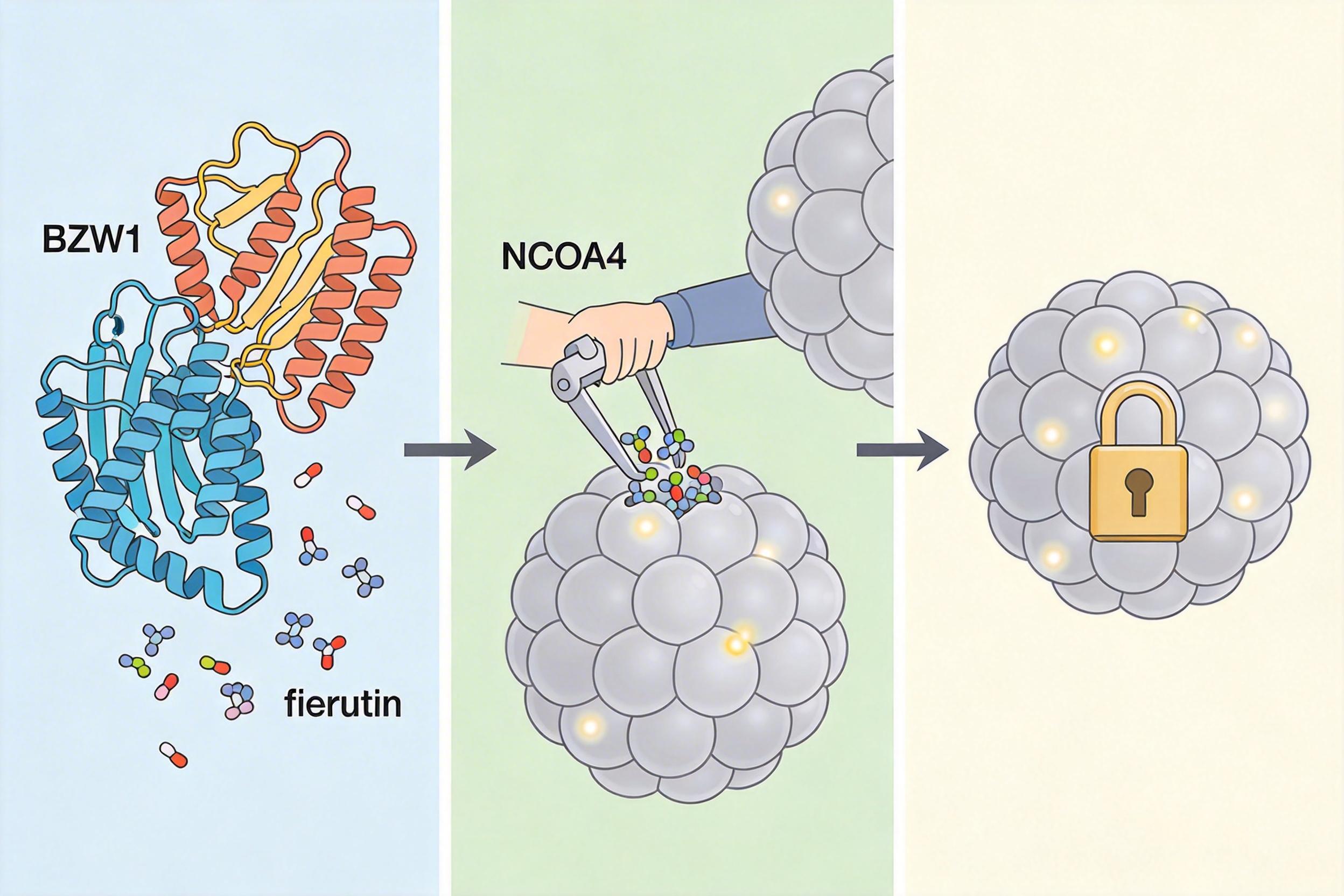
简单说,BZW1就是癌细胞的“防火总指挥”,一边拆“点火器”,一边加“灭火器”,把免疫系统的绝杀技给废了。
BZW1的危害远不止阻止铁死亡。当癌细胞逃过了这道“氧化死刑”,整个肿瘤的生存环境都会跟着变。
铁死亡其实是一种“免疫原性死亡”——细胞在死亡时会释放大量“警报信号”,吸引免疫细胞过来清理战场,同时激活更多T细胞。但BZW1按住了铁死亡的开关,这些警报信号就没了,免疫系统根本不知道这里有癌细胞。
更糟的是,BZW1还会帮癌细胞搭建“免疫隔离带”:它会减少肿瘤里CD8+T细胞的数量,就算有少量T细胞闯进来,也会被它搞得失去活性。原本应该是免疫细胞“围剿”癌细胞的战场,变成了癌细胞的“安全屋”。
研究团队在小鼠模型里验证了这个逻辑:当他们敲低BZW1的表达,癌细胞里的铁蛋白开始被大量降解,游离铁离子飙升,脂质过氧化瞬间失控,铁死亡被重新激活。更关键的是,肿瘤里的CD8+T细胞数量一下子多了3倍,干扰素-γ的分泌量翻了一番,原本“冷得像冰”的肿瘤微环境,瞬间变成了“热战场”。
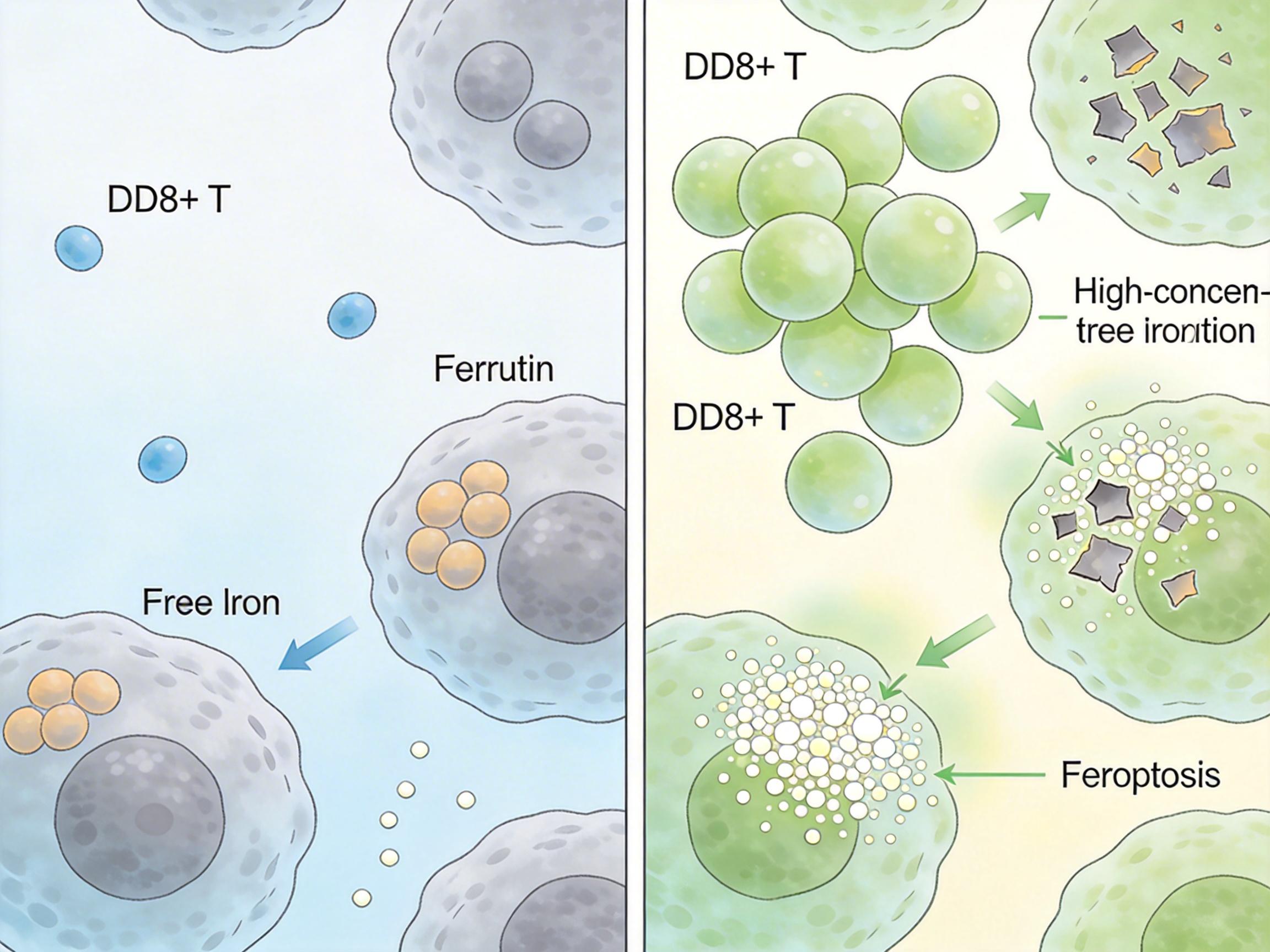
而当他们把BZW1抑制剂和抗PD-1免疫药联合使用时,肿瘤的生长速度被抑制了70%以上——这意味着,BZW1不仅是逃逸的“主谋”,更是破解免疫耐药的“钥匙”。
当然,BZW1靶点的研究还没到完美的地步。目前的实验都还停留在细胞和动物模型阶段,要真正用到临床上,还需要解决几个关键问题:
首先是特异性。BZW1在正常细胞里也有表达,只是在癌细胞里过量了。怎么才能精准打击癌细胞里的BZW1,而不影响正常细胞的功能?这需要更精准的小分子抑制剂,或者靶向递送技术。
其次是肿瘤异质性。研究显示,BZW1在肺腺癌、胰腺癌、胃癌等多种肿瘤里都有高表达,但不同肿瘤里的调控机制可能略有不同。比如在胰腺癌里,BZW1还会促进糖酵解,帮癌细胞适应缺氧环境。这意味着,针对不同肿瘤,BZW1的治疗策略可能需要调整。
还有临床转化的问题。目前还没有针对BZW1的上市药物,从实验室到病床,至少还需要3-5年的时间。但好消息是,研究团队已经找到了几个有潜力的小分子化合物,正在进行后续的优化和筛选。
过去我们总说,肺癌是“沉默的杀手”,但现在我们发现,它其实是“狡猾的逃犯”——它不是打不过免疫系统,而是学会了“钻空子”。BZW1的发现,就像在逃犯身上安装了一个“定位器”,让我们终于能看清它的逃跑路线。
未来的癌症治疗,可能不再是单一的“免疫攻击”,而是“精准打击+免疫围剿”的组合拳:先打掉癌细胞的“逃生通道”,再让免疫系统彻底清理战场。
锁死铁死亡,就锁死了癌细胞的生路。这句话不仅是对BZW1研究的总结,更是对未来癌症治疗的期待——我们不需要“杀死”所有癌细胞,只要断了它们的“后路”,免疫系统自然会完成剩下的任务。
点击充电,成为大圆镜下一个视频选题!