
9 天前

9 天前
当一个人突发心梗,医生能做的最快干预是打通堵塞的血管,但坏死的心肌细胞再也活不过来——它们会触发一场“缺血-炎症-纤维化”的连锁反应,最终把心脏拖向心力衰竭。这是全球每年1790万心血管死亡病例背后的共同剧本。
直到2026年4月,西南交大赵安莎、符金娟团队拿出了一份新的剧本:他们把中药葛根里的多糖,变成了一块能“跟着心脏跳”的补片。这块补片不仅能像脚手架一样撑住变薄的心室壁,还能导电、给药、自己修复破损,甚至能像树蛙脚趾牢牢粘住湿滑的树叶那样,贴在跳动的心脏上不脱落。它到底是怎么做到的?
你可以把这块名为GPS@AuNPs的补片,看成是一个微型的“心脏修复工厂”,每一层设计都精准对应心梗后的病理链条。
首先是“自修复的骨架”:研究者把葛根多糖氧化后,和明胶通过一种叫**动态希夫碱交联**的化学反应连在一起——简单说就是用一种“可拆可装”的分子键搭了个网状结构,就像用可降解的魔术贴拼出一张弹力网,扯破了还能自己粘回去。这个网络的弹性模量刚好卡在30-50kPa之间,和心肌组织的软硬度完全匹配,不会因为心脏跳得太猛就扯碎,也不会硬得磨伤心肌。
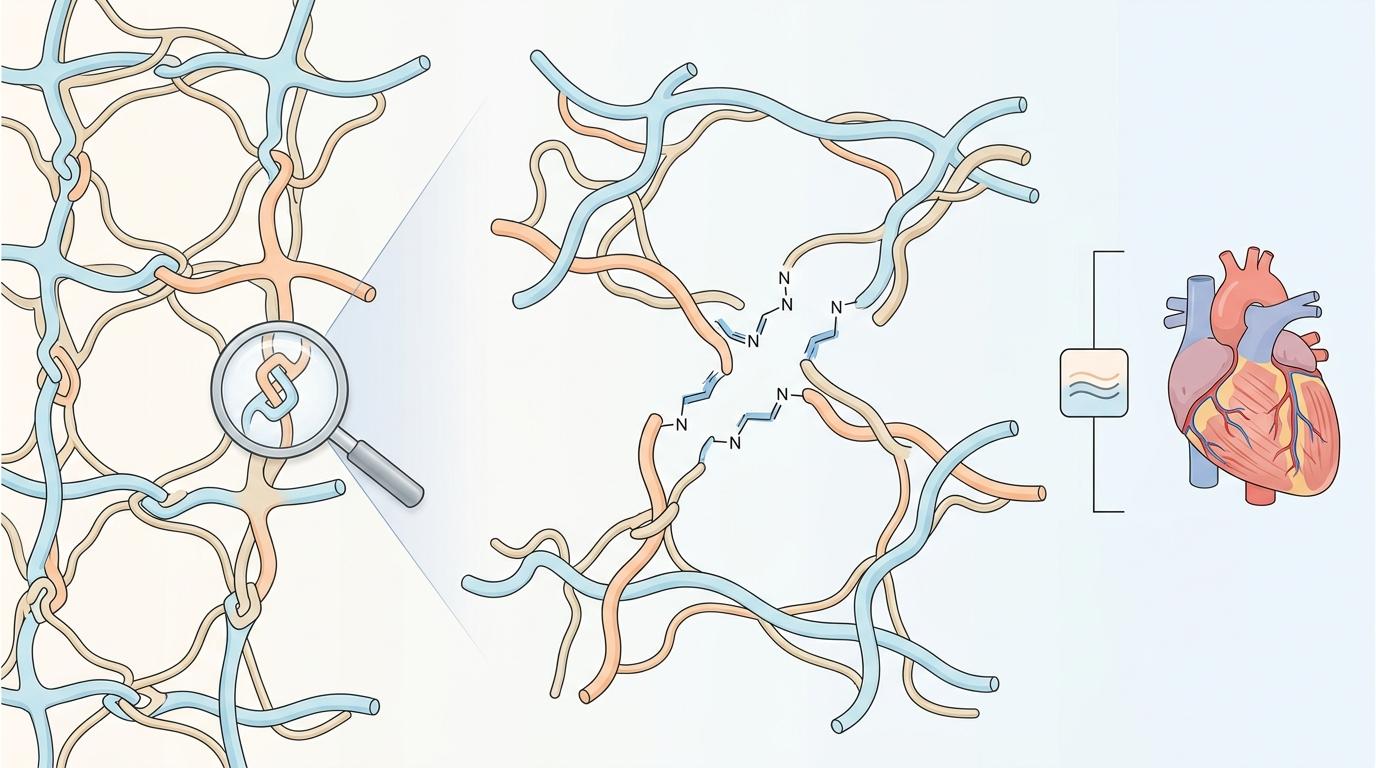
然后是“导电的神经”:他们在这个网里掺了半胱胺修饰的金纳米颗粒——这些直径只有几十纳米的小金粒,既能和多糖网的分子键结合加固结构,又能连成一条条微小的导电通路,让心脏的电信号能顺着补片传过去,避免坏死心肌导致的“电传导断裂”。
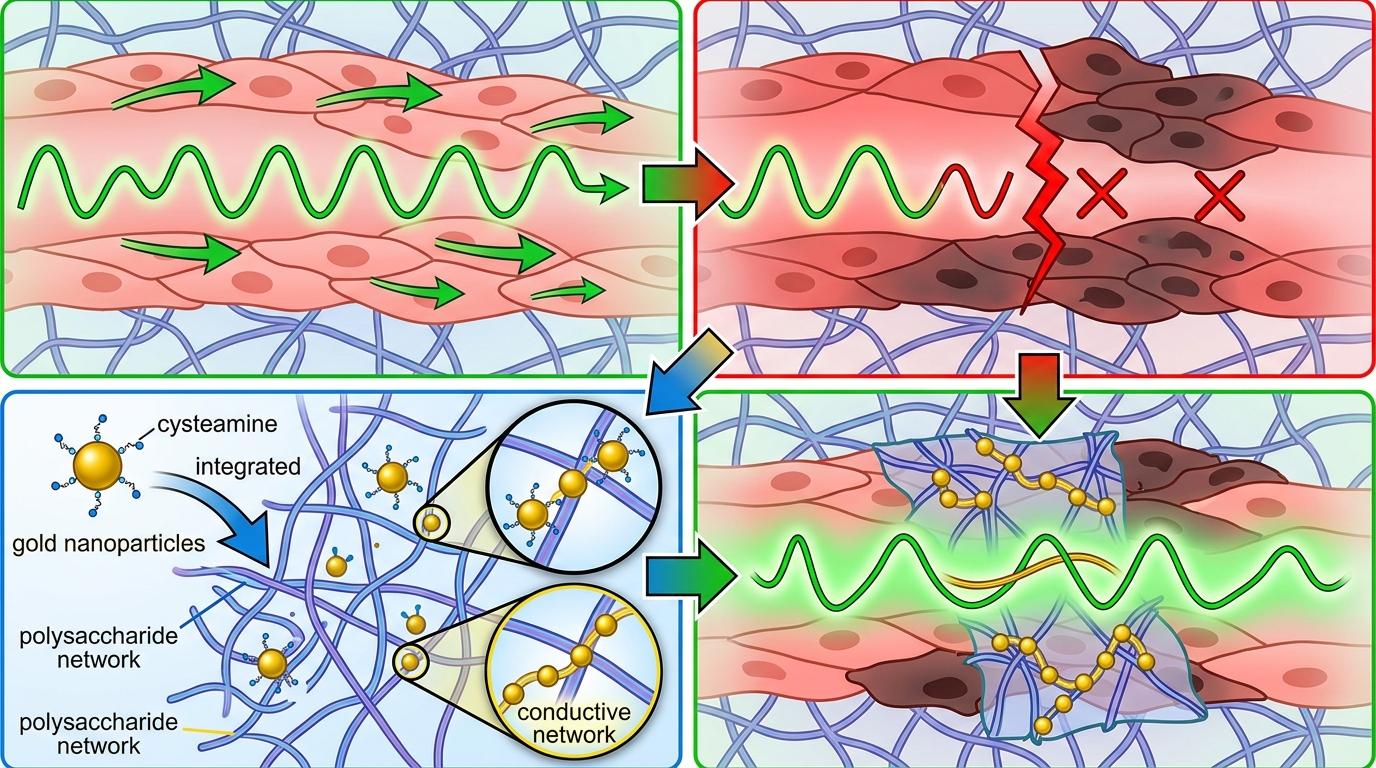
最后是“粘得牢的脚”:用3D打印在补片表面刻出仿树蛙足趾的微结构,就像给补片贴了无数个微型吸盘,能在湿滑跳动的心外膜上牢牢固定,不会移位脱落,还能避免心内粘连的二次损伤。
这不是葛根第一次用于心血管治疗——它的提取物葛根素早就被用来舒张血管,但这次的突破,是把葛根从“吃药”变成了“用材料”。
传统的中药多糖只是作为药物分子被吸收,而这块补片里的氧化葛根多糖,既是搭建骨架的材料,又是天然的药物载体:它本身的β-1,4糖苷键结构和血管基底膜相似,能模拟细胞外环境促进内皮细胞再生;它还能带着葛根里的异黄酮成分,缓慢释放到梗死区域,起到抗炎、抗氧化的作用。相当于把“药”和“支架”合二为一,实现了“药理-器件一体化”。
动物实验已经验证了效果:植入补片的心梗模型大鼠,左心室射血分数提升了15%-20%,心肌纤维化面积减少了30%以上;补片在体内会慢慢降解,最终变成无毒的代谢产物排出体外,完全不需要二次手术取出。
更重要的是,它解决了现有心肌补片的两大痛点:一是力学性能跟不上心脏跳动的节奏,二是导电和生物功能不能兼顾。而这块补片通过材料、纳米、仿生的三重结合,实现了力学、电学、生物学性能的同步优化。
当然,从实验室到病床,还有几道坎要跨。
首先是个体差异的问题:不同患者的梗死面积、心肌硬度、免疫状态都不一样,补片的降解速率、药物释放速度需要能个性化调整。目前的3D打印技术虽然能实现定制,但大规模生产的成本和效率还需要优化。
其次是长期安全性:金纳米颗粒在体内的长期代谢路径、对免疫系统的潜在影响,还需要更长期的动物实验和临床数据验证——尽管现有研究显示它的生物相容性良好,但纳米材料在人体内的“长期居留”始终是个需要谨慎对待的问题。
最后是监管和标准化:这种“中药+纳米+仿生”的跨界产品,既不是传统的药物,也不是普通的医疗器械,需要建立新的评价标准和监管路径。比如它的药物释放动力学、力学性能稳定性,都需要符合医疗器械和药物的双重要求。
当我们谈论中药现代化时,很多人想到的是提取有效成分做成西药,但西南交大的团队给出了另一种可能:把中药本身变成一种功能性材料,让它在体内发挥“材料支架+药物缓释+生物调控”的多重作用。
“从分子到器件,从给药到介入”——这不仅是葛根的跨界,也是传统中药和现代材料科学的一次握手。它让我们看到,那些在本草纲目里记载了千年的植物,或许能在纳米尺度上,给现代医学带来新的惊喜。而这场从中药到心脏补片的革命,最终受益的,是全球数以千万计的心血管疾病患者。
点击充电,成为大圆镜下一个视频选题!