
12 天前

12 天前
胶质母细胞瘤是人类大脑中最凶狠的“入侵者”——患者确诊后的平均生存期仅15个月,现有治疗几乎无法阻挡它的进展。过去十年,科学家们一直在肿瘤细胞的基因里寻找突破口,却始终没摸到那根最关键的“开关”。直到2026年3月,华中科技大学、武汉大学与中科院武汉磁共振中心的联合团队,在《科学·进展》上揭开了一个藏在昼夜节律里的秘密:我们体内调控睡眠作息的CLOCK蛋白,居然会在脑癌细胞里“叛变”,催生一种从未被发现的组蛋白修饰,直接给肿瘤的生长“开绿灯”。这种新型修饰到底是怎么运作的?它为何会成为脑癌的帮凶?
要理解这个发现,得先搞懂组蛋白是什么——你可以把它想象成DNA的“贴身保镖”,长长的DNA链缠绕在组蛋白上,形成紧密的染色质结构。组蛋白上的赖氨酸残基就像一个个“密码位”,不同的化学修饰会改变染色质的松紧度,决定哪些基因能被“读取”表达,哪些会被“锁死”沉默。
过去我们只知道乙酰化、甲基化等几种常见“密码”,而这次团队发现的,是一种全新的组蛋白修饰:H3K37戊二酰化(H3K37glut)。简单来说,就是CLOCK蛋白利用细胞内的戊二酰辅酶A,在组蛋白H3的第37位赖氨酸上“贴”了一个戊二酰基团。
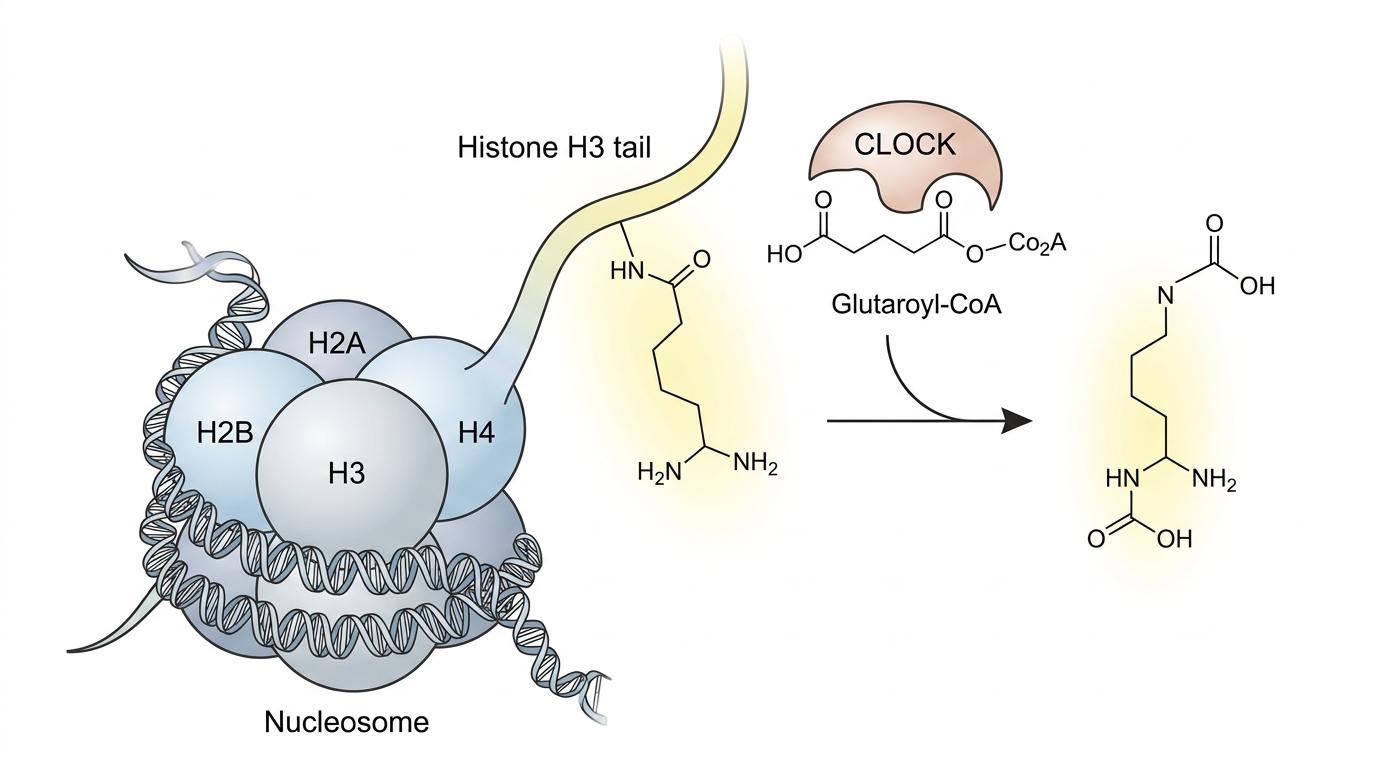
这个看似微小的变化,却引发了连锁反应:戊二酰基团带着负电荷,会被旁边H3第39位组氨酸、第40位精氨酸的正电荷“拉住”,然后像一片小盖子一样,盖在第38位脯氨酸的环状结构上。这个特殊的构象,直接挡住了另一个关键蛋白SETD2的结合位点。
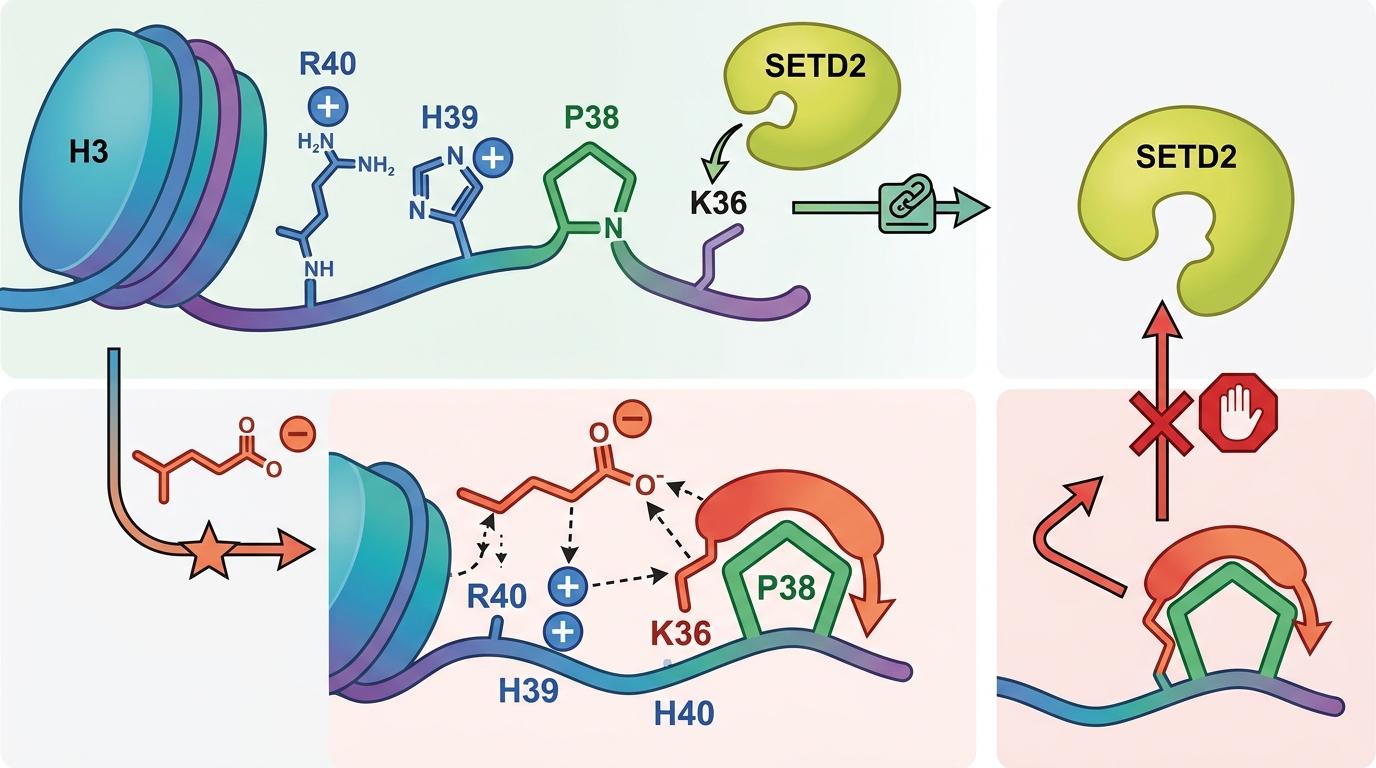
SETD2是细胞里的“抑癌守门员”,它的工作是给组蛋白H3的第36位赖氨酸加上三个甲基,也就是H3K36三甲基化(H3K36me3)。这种修饰会让染色质维持在“有序状态”,调控DNA修复、基因转录等关键通路,防止细胞乱分裂。
但当CLOCK催生的H3K37glut把SETD2的路挡住后,一切都乱了:
团队在临床样本里验证了这个机制:胶质母细胞瘤患者的肿瘤组织中,CLOCK蛋白和H3K37glut的含量都比正常脑组织高得多,而H3K36me3的水平则显著降低。更关键的是,H3K37glut含量越高,肿瘤进展越快,患者的生存期就越短——最高和最低含量的患者,生存期能差出一倍以上。
有意思的是,这个过程和CLOCK原本的昼夜节律功能完全无关,它就像一个被“策反”的卧底,用自己的酶活性干起了帮凶的勾当。
这个发现还解开了另一个谜题:为什么肿瘤细胞的代谢总是乱的?
戊二酰辅酶A不是凭空出现的,它是细胞代谢的中间产物,来自氨基酸分解和脂肪酸氧化。肿瘤细胞为了快速增殖,会疯狂调整代谢通路,戊二酰辅酶A的含量会随之升高——这正好给CLOCK提供了“作案原料”。换句话说,肿瘤的代谢重编程,其实在给这个致癌修饰“供能”。
这也解释了为什么CLOCK会在肿瘤里失控:当细胞代谢紊乱时,原本调控昼夜节律的CLOCK,会转而利用代谢产物催化新型组蛋白修饰,把代谢信号转化为致癌的表观遗传信号。这种“代谢-表观遗传”的联动,可能是肿瘤细胞适应恶劣环境、快速增殖的核心机制之一。
当然,这个研究还有不少未解的问题:比如目前还没找到能去除H3K37glut的去修饰酶,也不清楚CLOCK在其他癌症里会不会有类似的“叛变”行为。但至少它给我们指出了一个新方向:靶向CLOCK的戊二酰转移酶活性,或者阻断戊二酰辅酶A的供应,可能成为胶质母细胞瘤的新疗法。
当我们把目光聚焦在肿瘤的基因突变时,却忽略了那些原本“各司其职”的蛋白,可能在代谢紊乱的环境里悄然“变节”。CLOCK从昼夜节律的调控者,变成胶质母细胞瘤的帮凶,这个发现不仅拓展了组蛋白修饰的“密码本”,更让我们看到肿瘤细胞的狡猾之处——它会利用我们自身的生理机制,为自己的生长铺路。
代谢乱则表观乱,表观乱则癌症生。这或许是这个研究留给我们最深刻的启示:对抗癌症,不仅要盯着肿瘤本身,还要关注那些被肿瘤打乱的身体平衡。毕竟,癌细胞从来都不是孤军奋战,它是利用我们自己的身体,长出的“异己”。
点击充电,成为大圆镜下一个视频选题!