对抗知识焦虑,从看懂这条开始
App 下载
给抗癌T细胞换把锁,从根源堵上误伤漏洞
免疫治疗|受体乱配对|湖南大学刘光娜团队|T细胞受体|TCR-T细胞疗法|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
免疫治疗|受体乱配对|湖南大学刘光娜团队|T细胞受体|TCR-T细胞疗法|肿瘤学|医学健康
想象一下:你给战士们配发了能精准识别敌人的专属密钥,可一上战场,这些密钥却和战士们自带的旧钥匙乱配对,拼出了四把新钥匙——只有一把能打敌人,另外三把可能转头就对准了自己人。这就是TCR-T细胞疗法多年来卡在临床推广前的死结:抗癌T细胞里的外源受体,总会和细胞自带的受体乱配对,既削弱战斗力,又埋下误伤自身的隐患。2026年春天,湖南大学刘光娜团队的一项研究,给这个死结找到了全新的解法——不是修修补补,而是直接给T细胞换了套不会乱开的锁。
T细胞受体(TCR)是T细胞识别肿瘤的核心,它由α和β两条链像钥匙和锁扣一样精准配对而成。当医生把能识别肿瘤的外源TCR基因导入患者T细胞时,外来的α、β链会和细胞原本就有的α、β链混在一起,最终可能拼出四种组合:只有一种是能精准抗癌的“正确钥匙”,另外三种要么是没功能的废品,要么是从未经过人体免疫筛选的“野钥匙”——它们可能识别正常组织,引发致命的自身免疫反应。
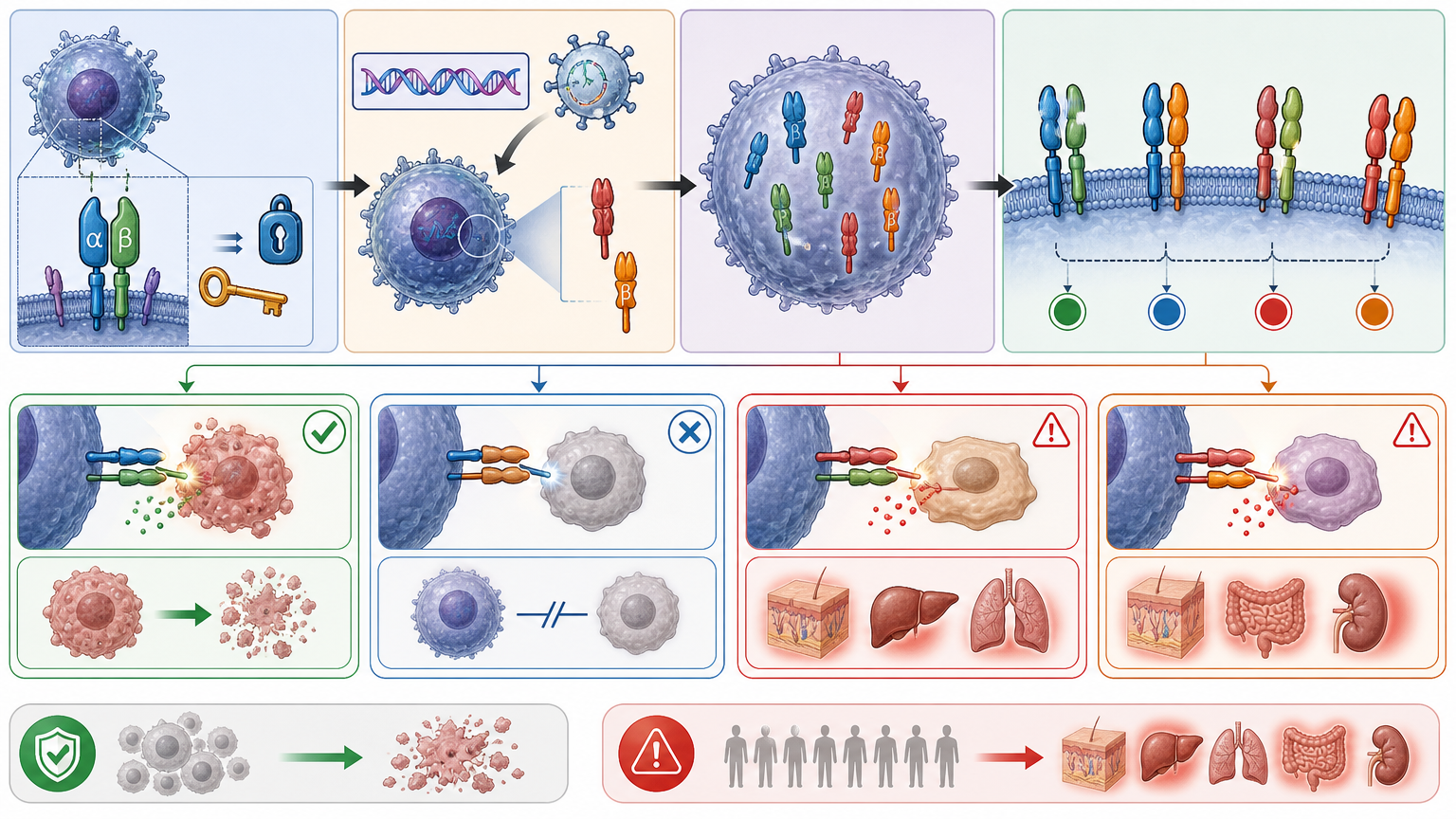
传统的解决思路要么是“换零件”:用小鼠的TCR恒定区替换人类的,靠物种差异减少错配,但小鼠蛋白会引发人体免疫排斥;要么是“加固旧锁”:在人类TCR的天然位点加额外二硫键,可天然位点本身就是错配的重灾区,加固效果有限,还不通用。这些方法都像在给漏雨的房子贴胶带,堵不住根本的漏洞。
刘光娜团队的思路彻底跳开了“修补”的惯性:既然天然的配对位点既是核心又是麻烦,那不如直接换掉这套配对逻辑。
他们先做了个验证:如果直接删掉天然二硫键的关键氨基酸,错配确实几乎消失了,但TCR的结构也垮了,完全失去了激活T细胞的功能。这说明不能硬拆,得换个地方重新搭建。
通过结构计算预测,他们在TCR恒定区的全新位置筛选出了能形成二硫键的位点——相当于在钥匙和锁扣的新位置打了个孔,重新装了个智能扣。实验验证显示,这些人工二硫键像定制的榫卯,只让外来的α、β链精准扣合,和细胞自带的链完全“合不上槽”。
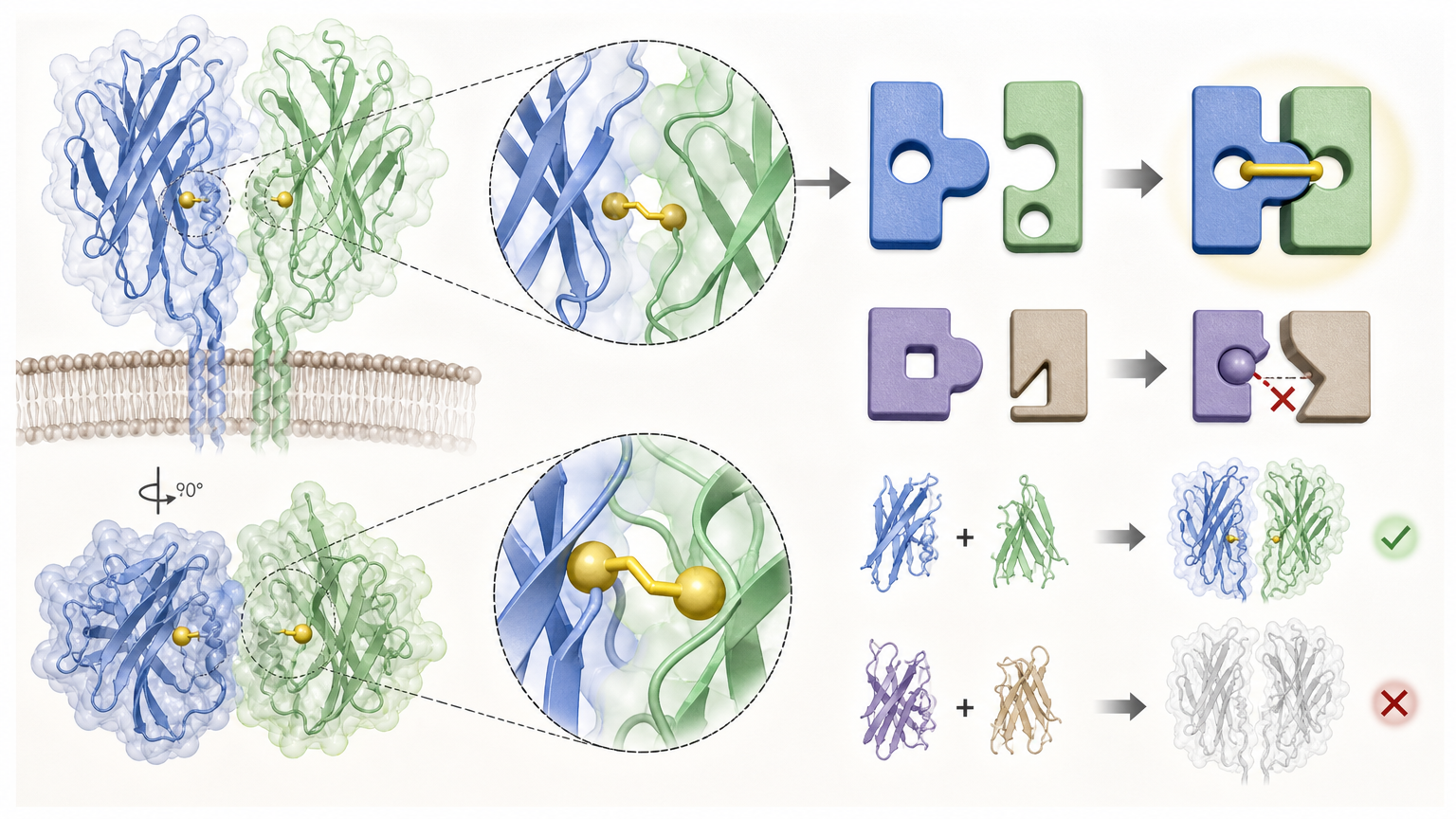
测试数据更直观:和野生型人类TCR比,这种新TCR在细胞表面的表达量显著提升,错配率降到了极低水平;它激活T细胞、杀伤肿瘤的能力,能和当前效果最好的鼠源TCR媲美,却完全用的是人类序列,没有免疫排斥风险。
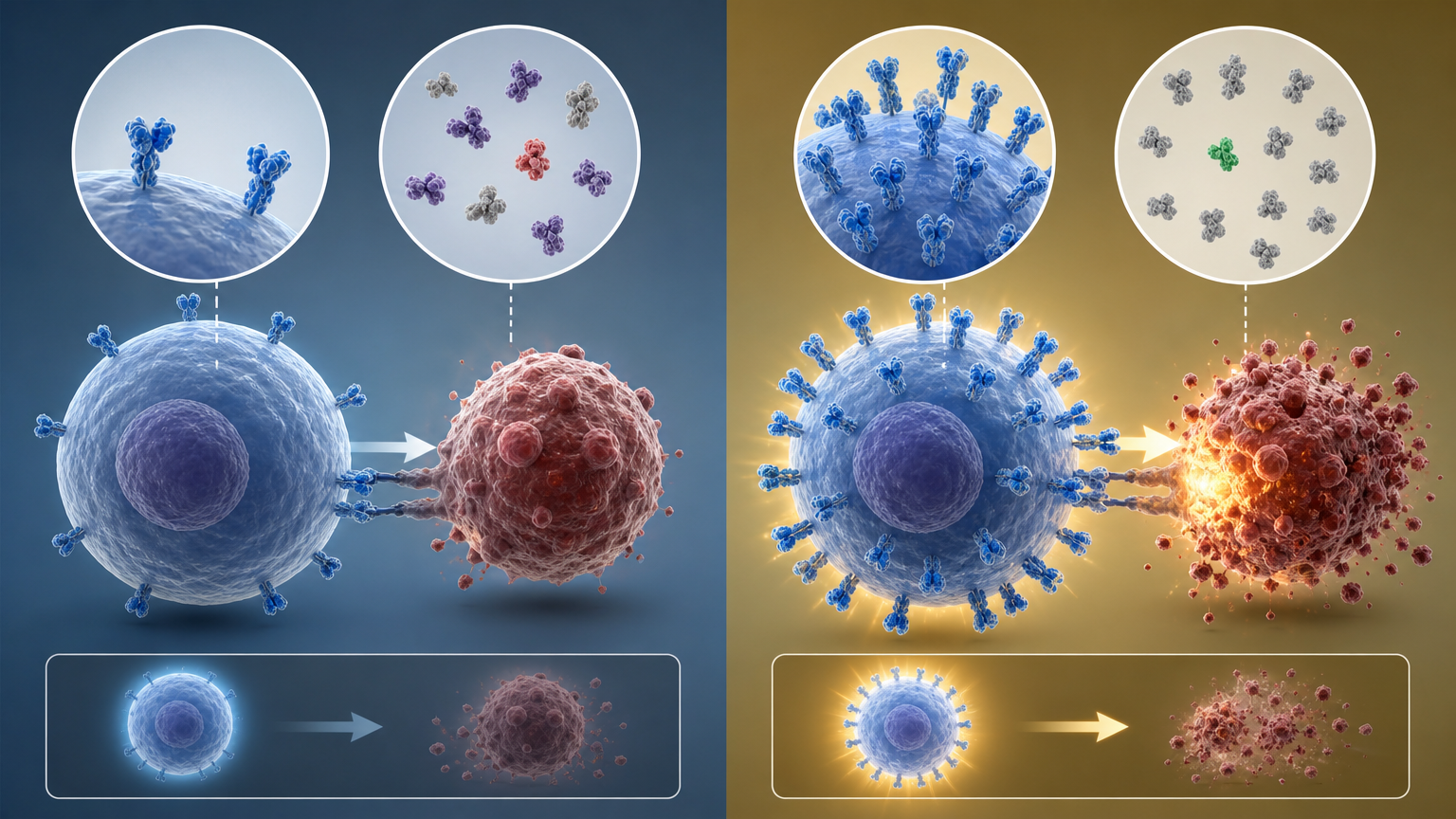
更重要的是,这套“人工二硫键”设计不是只能用在某一种TCR上。研究团队验证了它能适配多种不同的抗癌TCR,甚至有潜力推广到STAR-T等其他基于TCR的合成受体疗法上——相当于这套智能锁的接口是通用的,能给各种不同的抗癌钥匙配套。
当然,它也不是完美的终极方案:目前的实验还停留在临床前阶段,长期植入人体后的稳定性、对T细胞寿命的影响,还需要更多数据验证;而且当前的设计只能把β链的错配几乎消除,α链还有少量残留错配,背后的机制还需要进一步拆解。但不可否认的是,它给TCR-T疗法的安全问题提供了一条从根源解决的路径,而不是一直在错误的地方修修补补。
从100多年前人类发现T细胞的存在,到今天能精准改造它的核心受体,癌症免疫治疗的每一步,都在和“精准”与“安全”赛跑。过去我们总在想怎么让T细胞更能打,却常常忽略了它会不会“走火”。
刘光娜团队的这套“智能锁”,本质上是给抗癌T细胞加了一道身份验证:只有正确的配对才能激活,从根源上切断了误伤自身的可能。精准的前提,是先把“自己人”和“敌人”分清楚。未来,当这套技术走进临床,那些原本因为安全隐患被搁置的抗癌TCR,或许就能真正成为肿瘤患者手里的可靠武器。