对抗知识焦虑,从看懂这条开始
App 下载
北大团队找到调控衰老的关键RNA分子
Nature Aging|细胞衰老|长非编码RNA|北京大学韩敬东团队|分子细胞生物学|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
Nature Aging|细胞衰老|长非编码RNA|北京大学韩敬东团队|分子细胞生物学|生命科学
当你对着镜子发现第一条细纹时,你的身体里已经有上亿细胞悄悄“老”了——它们停止分裂、积累损伤,还会向周围释放炎症信号,像一群赖在组织里的“捣蛋鬼”,加速器官老化和疾病到来。科学家们一直在找能管住这些“捣蛋鬼”的开关,却总在蛋白质和基因的迷宫里打转。直到2026年3月,北京大学韩敬东团队在《Nature Aging》上发布的研究,把目光投向了之前被忽略的“暗物质”——长非编码RNA(lncRNA),还真揪出了一个能直接调控细胞衰老的关键分子。
为什么这些不起眼的RNA能决定细胞的生死?这得从衰老的根源说起。
要找到调控衰老的lncRNA,首先得解决一个难题:人类基因组里有超过10万条lncRNA,大部分功能未知,像一片没被探索过的原始森林。传统研究一次只能盯着一两条,效率太低。韩敬东团队用上了当下最前沿的“单细胞多组学扰动筛选”——你可以把它想象成给细胞群做“批量精准手术”:先用CRISPR–dCas9–KRAB系统,把32条和衰老相关的高丰度lncRNA挨个“静音”,再用单细胞RNA测序和染色质可及性分析,同时观察每个细胞的基因表达和染色质状态变化。
这就像给每个细胞装了个“黑匣子”,能精准记录下“关掉某条lncRNA”后,细胞里发生的连锁反应。比如有的细胞会立刻启动衰老程序,有的则会出现DNA损伤积累,这些细微的变化,在传统的群体分析里根本看不到。
最终,他们锁定了一条叫HOTAIRM1的lncRNA——它就像细胞里的“修复队长”,一旦被“静音”,细胞的DNA修复效率会骤降,损伤越积越多,很快就会陷入衰老状态。
HOTAIRM1到底是怎么干活的?研究人员用显微镜追踪它的位置,发现一旦细胞出现DNA双链断裂,HOTAIRM1会第一时间跑到断裂位点,像个“黏合剂”一样,把修复蛋白BANF1和p53拉到一起,形成稳定的修复复合物。没有它,这些修复蛋白就像没头苍蝇,找不到损伤位点,DNA断口只能一直敞着。
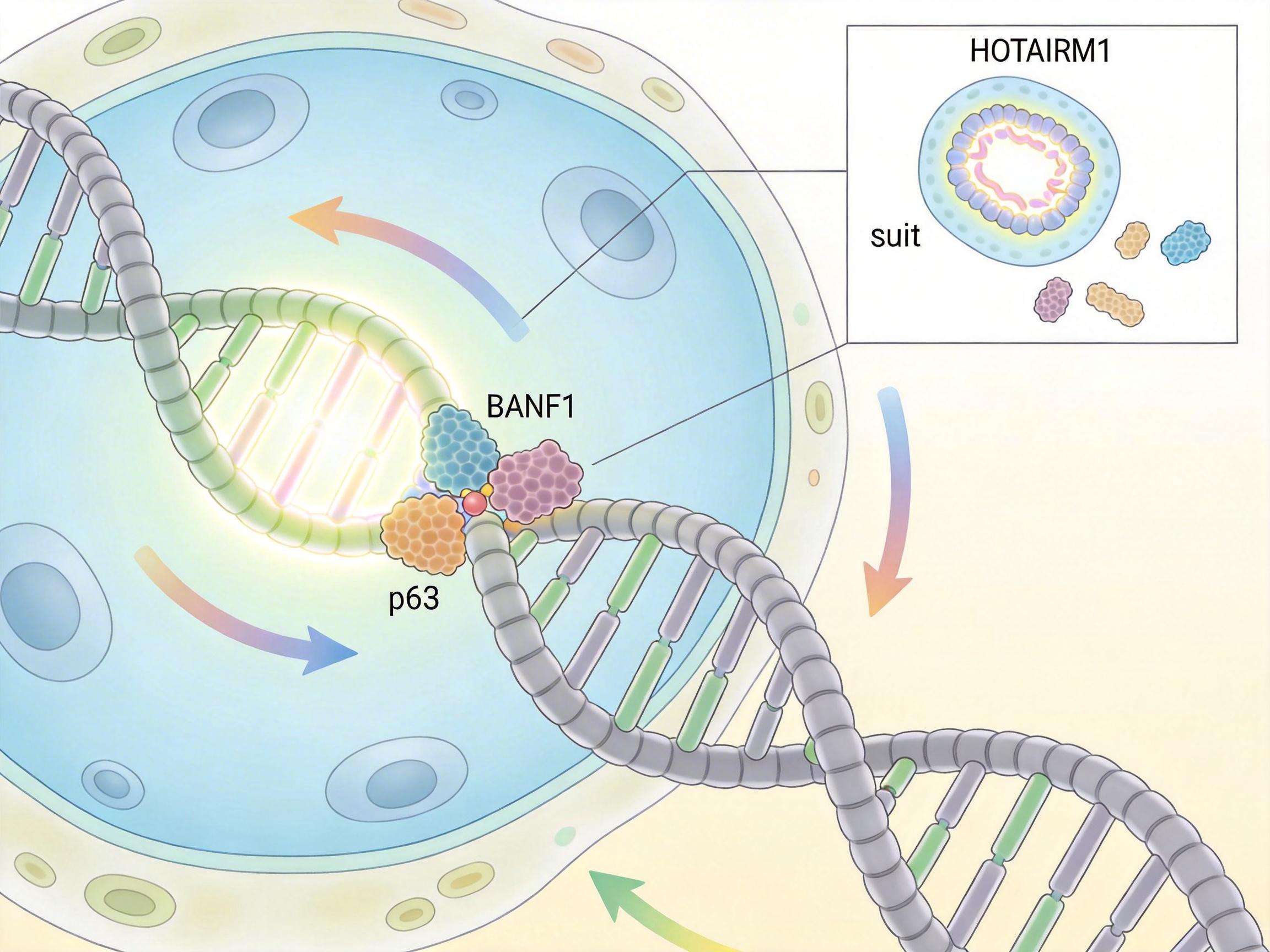
为了验证它的抗衰老能力,研究人员在老年小鼠的肺组织里过表达HOTAIRM1——结果让人惊喜:原本布满纤维化疤痕的肺组织,居然长出了新的细胞,纤维化程度明显减轻,细胞增殖的标记物Ki67也大幅增加。这意味着,这条小小的RNA,真的能让老化的组织重新焕发生机。
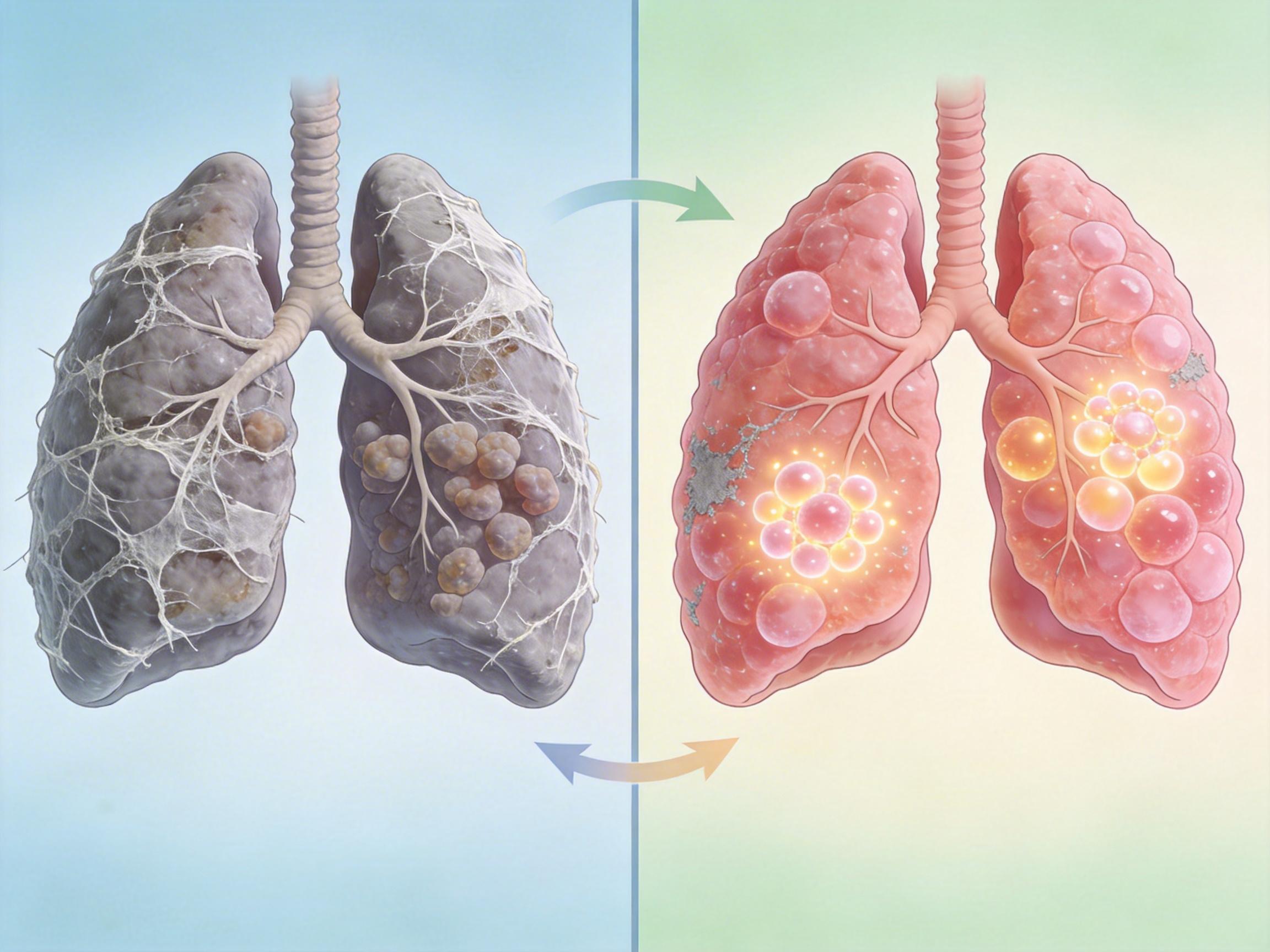
不过,这项研究也有局限:目前只在小鼠肺组织里验证了效果,在其他器官里是否有效还不确定;而且lncRNA的序列保守性很低,人类和小鼠的HOTAIRM1虽然功能相似,但直接把小鼠的序列用到人身上,可能会有问题。
HOTAIRM1的发现,不仅刷新了我们对衰老调控的认知,还打开了RNA治疗的新赛道。过去RNA治疗主要集中在mRNA疫苗和siRNA药物上,lncRNA因为功能复杂、递送困难,一直是冷门领域。但这次研究证明,只要找对靶点,lncRNA能直接调控细胞的核心功能,甚至逆转组织老化。
不过,要把实验室里的发现变成临床药物,还有好几道坎要过:首先是递送问题,怎么把lncRNA精准送到目标组织,同时避免被体内的酶降解;其次是脱靶风险,万一影响了其他正常RNA的功能,可能会引发新的问题;最后是成本,RNA药物的生产工艺复杂,价格一直居高不下。
但市场已经在蠢蠢欲动——全球lncRNA治疗市场预计到2033年能达到58亿美元,不少药企已经开始布局。北大团队的这项研究,相当于给这个赛道点亮了一盏灯,让更多人看到了lncRNA抗衰老的潜力。
当我们谈论衰老时,总习惯把它当成一个不可逆转的过程——就像时间的流逝,谁也挡不住。但HOTAIRM1的发现告诉我们,衰老其实是细胞里一系列分子事件的总和,只要找对了那个关键开关,我们就能延缓甚至逆转这个过程。
“衰老不是终点,而是可以调控的程序。”这句话听起来像科幻小说,但现在已经有了现实的依据。未来,也许我们不用再对着细纹叹气,只要打一针靶向HOTAIRM1的RNA药物,就能让老化的组织重新年轻。当然,这一天还很远,但至少我们已经迈出了关键的一步——从“被动接受衰老”,到“主动调控衰老”。