对抗知识焦虑,从看懂这条开始
App 下载
短RNA拉住乱跑的TDP-43,渐冻症有了新解法
詹姆斯·肖特团队|宾夕法尼亚大学|运动神经元|短RNA分子|TDP-43蛋白|神经退行性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
詹姆斯·肖特团队|宾夕法尼亚大学|运动神经元|短RNA分子|TDP-43蛋白|神经退行性疾病|医学健康
想象这样一个场景:你的大脑里,有个叫TDP-43的「办公室主任」,本该待在细胞核里管RNA文件,某天突然擅离职守跑到细胞质,还拉着同事们抱团成块——这就是97%的渐冻症(ALS)患者脑子里正在发生的事。这些蛋白块会堵死神经元的「工作通道」,让运动神经元慢慢坏死,直到患者连呼吸的力气都没有。
过去几十年,科学家要么想把这些蛋白块拆碎,要么想把乱跑的主任赶回办公室,但都没摸到核心的开关。直到宾夕法尼亚大学的詹姆斯·肖特团队,在《科学》杂志上抛出了一个完全不同的答案:不用硬拆也不用硬拽,给它找个「专属秘书」就行。
你可以把TDP-43想象成一个有两个工作岗位的员工:前面的「RNA识别区」是它的办公桌,负责对接各种RNA文件;后面的「朊样结构域」是它的「摸鱼开关」,一旦没人管就会拉着同事抱团摸鱼。
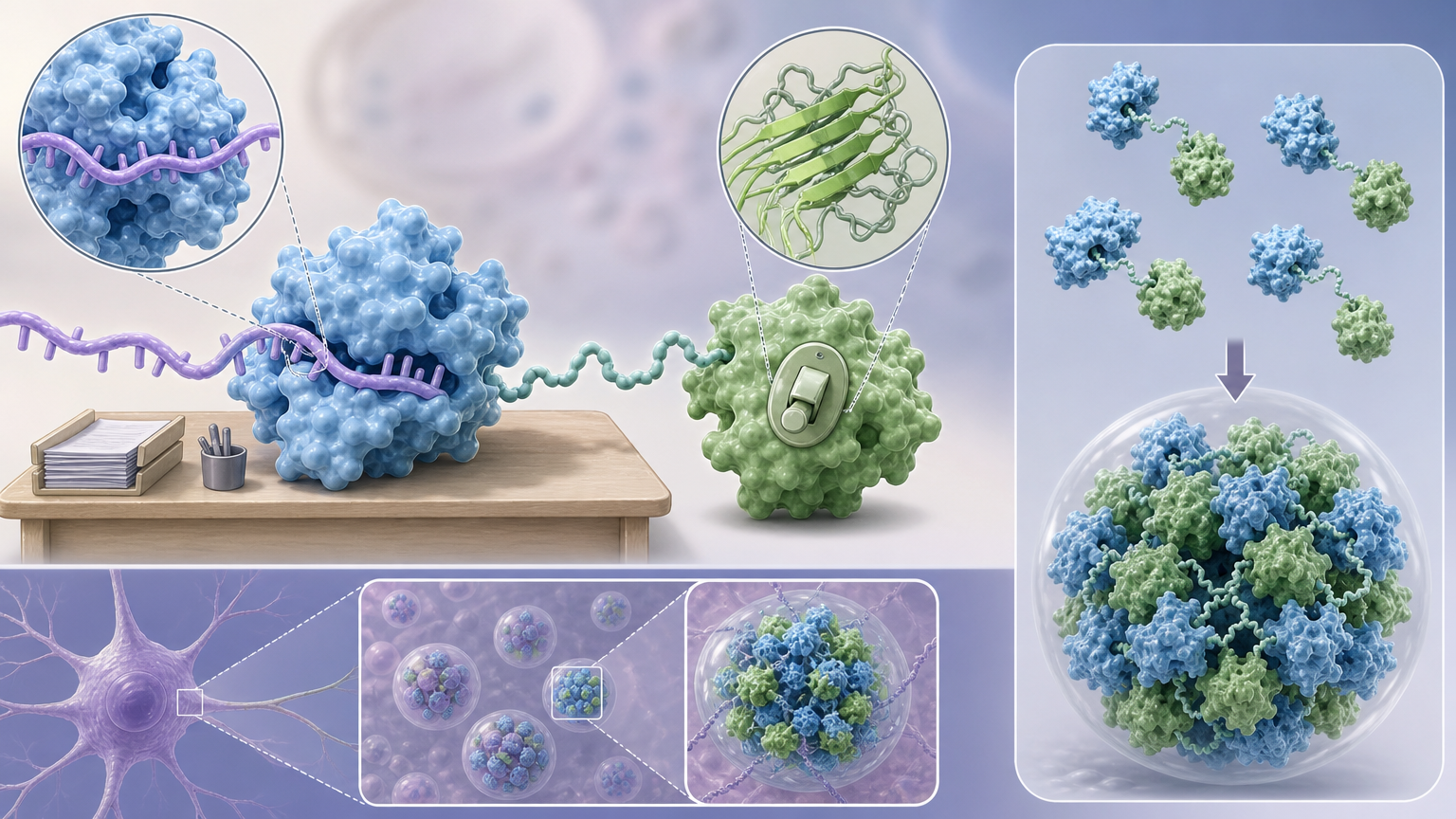
肖特团队找到的「秘书」是两段短RNA——Clip34和Malat1_start。它们既不是来抢TDP-43的工作,也不是来批评它的,而是精准地坐在它的「办公桌」上,轻轻稳住它的姿势。就像给一个坐歪了的人扶正椅背,TDP-43被稳住的同时,背后那个想抱团的「摸鱼开关」突然就失灵了。
但真实的机制比这更精确: 短RNA结合TDP-43的RNA识别基序后,会通过别构效应破坏朊样结构域里的一段保守螺旋——那正是TDP-43抱团的核心抓手。它没有改变TDP-43的本职工作,只是让它没法再「拉帮结派」。
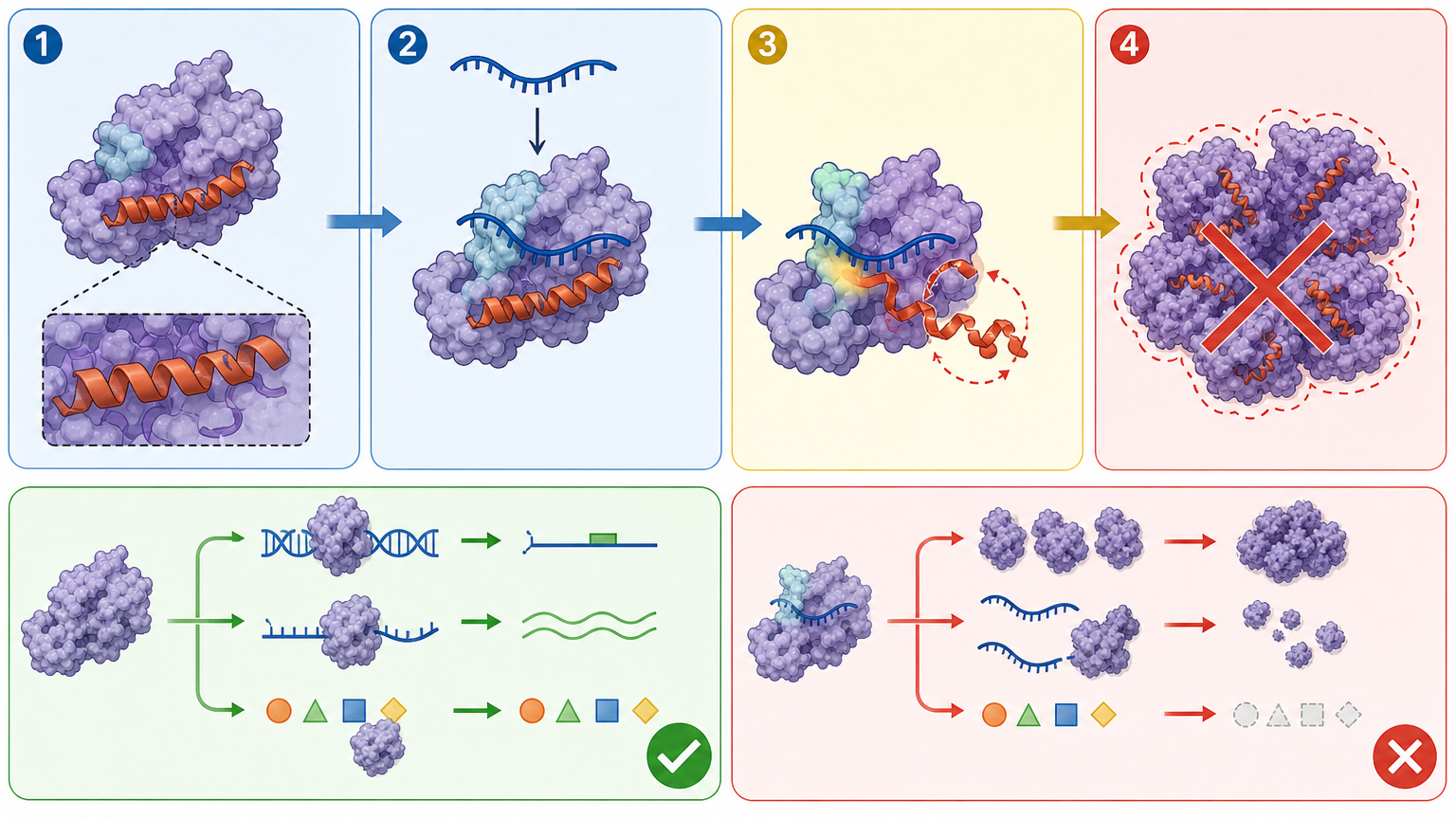
一开始,科学家只是在试管里验证了这个逻辑:加入短RNA后,原本会抱团的TDP-43果然保持了分散状态。但真正的惊喜在后面——
他们把Malat1_start注射进已经出现TDP-43聚集、运动神经元开始死亡的ALS小鼠体内。结果是,原本已经抱团的蛋白块被慢慢拆开,乱跑的TDP-43回到了细胞核里,甚至那些快要坏死的运动神经元,居然活了下来。
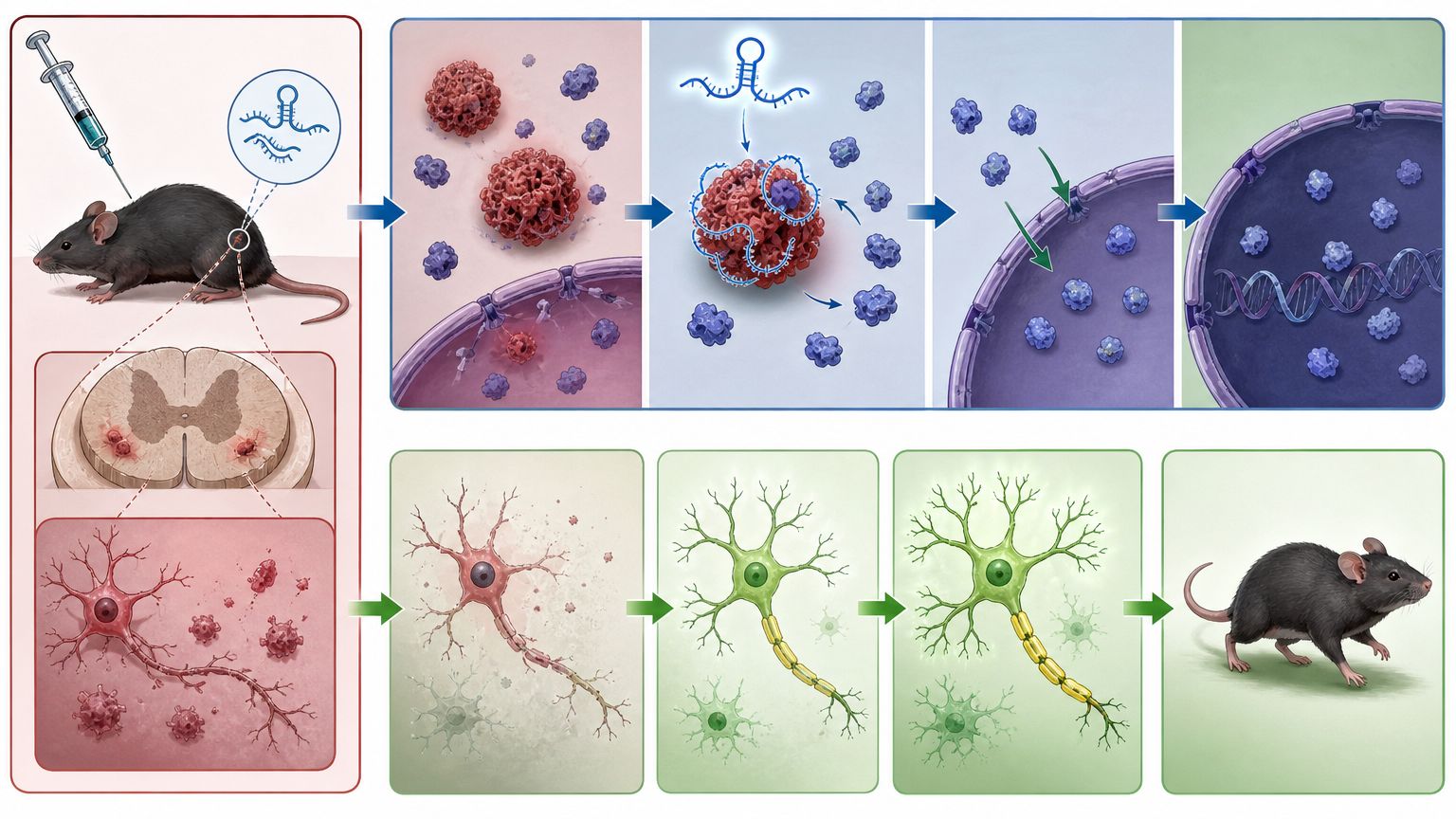
这是第一次,有药物能在动物模型里同时做到三件事:逆转已有的蛋白聚集、恢复蛋白的正常功能、阻止神经元死亡。
更关键的是,这个「秘书」很懂分寸。在患者来源的运动神经元里,它只纠正乱跑的TDP-43,完全不干扰正常TDP-43的RNA加工工作——就像一个只会提醒摸鱼员工的秘书,绝不会打断认真干活的人。
但别着急把「治愈渐冻症」的标签贴上去。这个疗法离真正走进病房,还有几道必须跨过去的坎。
最大的问题是「送货上门」。短RNA是大分子,没法自己穿过血脑屏障,现在的实验只能靠脊髓注射——这对患者来说是个不小的负担。科学家正在测试纳米载体和鼻腔给药的方式,但离稳定的临床方案还有距离。
另外,虽然短RNA对多种TDP-43突变体都有效,但渐冻症是个高度异质的疾病,有些患者的问题可能不止TDP-43这一个靶点。而且长期注射的安全性、会不会引发免疫反应,都还需要更久的观察。
说句实在的,这不是一劳永逸的「神药」,但它给渐冻症治疗打开了一扇全新的门——不再是跟蛋白块死磕,而是从根源上纠正蛋白的「行为偏差」。
我们总习惯把神经退行性疾病看成「蛋白的叛乱」,要靠药物去镇压。但肖特团队的研究却在说:有时候,给「叛乱者」找个合适的帮手,比镇压更有效。
「与其拆墙,不如扶稳门框。」这句话放在神经退行性疾病的治疗里,突然就有了新的重量。
未来的某一天,渐冻症患者可能不用再靠昂贵的药物维持生命,只需要定期注射一段小小的RNA——就像给大脑里的「问题员工」,派去一个能稳住局面的秘书。而这,可能就是我们离攻克渐冻症最近的一次。