
2 天前

2 天前
当一位32岁的多发性硬化症患者发现自己记不住刚说过的话,走路时腿开始不听使唤,医生通常会告诉她:这是免疫系统攻击了神经髓鞘。但剑桥和加州大学的两支团队在《自然》杂志上同时推翻了这个认知的一角——他们在患者大脑里发现,真正最先倒下的,是大脑皮层上层一群叫CUX2+的兴奋性神经元。这些神经元既不是髓鞘的组成部分,也不是免疫细胞攻击的直接目标,它们的死亡,源于自身DNA的损伤堆积和修复失灵。
你可以把神经元的DNA想象成一本不断被翻阅的旧书——日常代谢产生的活性氧、神经活动带来的转录压力、炎症因子的攻击,都是书页上不断出现的划痕和污渍。正常情况下,细胞会启动一套“DNA损伤反应(DDR)”机制修复这些伤口:单链断裂用“胶带”粘好,双链断裂就用“针线”缝合,其中最关键的缝合工具,是一种叫ATF4的转录因子。 但在多发性硬化症患者的CUX2+神经元里,这套修复系统失灵了。研究人员在患者大脑和小鼠模型中都发现,这些神经元的DNA上布满了未被修复的双链断裂标记,数量是其他神经元的3倍以上。更致命的是,本应指挥修复的ATF4和辅助修复的CUX2蛋白,在这些神经元里的活性大幅降低——相当于负责修书的工匠不仅人手不足,还弄丢了最趁手的工具。
为什么偏偏是CUX2+神经元遭殃?答案藏在多发性硬化症的核心炎症因子——干扰素-γ里。 当免疫系统被激活,干扰素-γ会涌入大脑,它像一把精准的钥匙,只打开CUX2+神经元里的“活性氧开关”。实验显示,仅仅是在培养皿里加入干扰素-γ,就能让这些神经元的活性氧水平飙升30%,直接击穿DNA双链。而其他神经元要么没有这个“开关”,要么能快速启动抗氧化机制,躲过一劫。
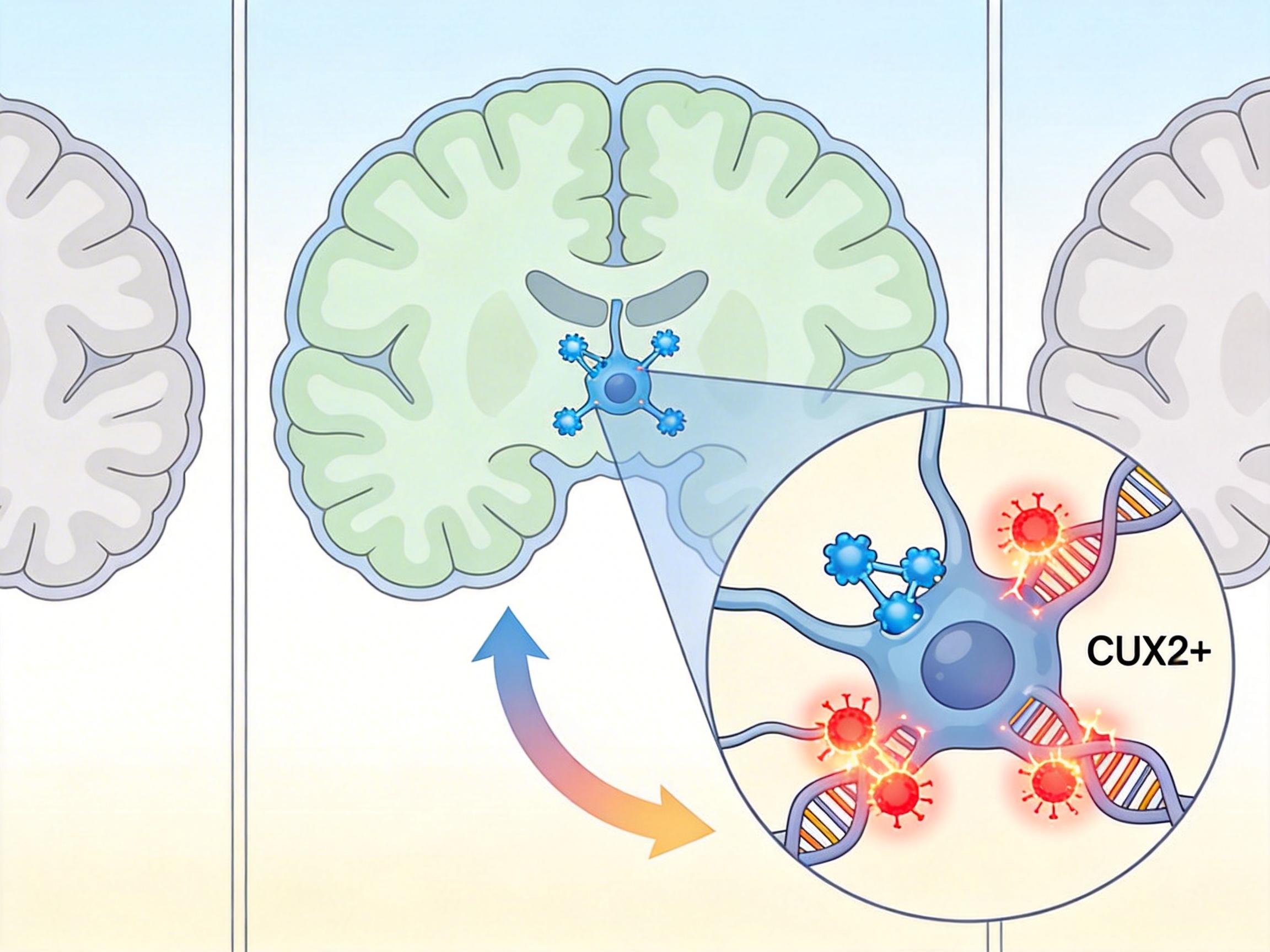
更关键的是,这些CUX2+神经元从发育阶段就带着“先天脆弱性”:它们是大脑中最后成熟的一批兴奋性神经元,在发育过程中需要快速分裂和转录,本就积累了更多DNA损伤,全靠ATF4和CUX2的修复能力维持存活。一旦炎症来袭,修复系统过载,这些神经元就成了最先被压垮的多米诺骨牌。
简单说:
目前多发性硬化症的主流治疗,几乎全是针对免疫系统的——要么抑制免疫细胞的活性,要么阻止它们进入大脑。这些疗法能有效减少炎症发作,但对已经出现DNA损伤的神经元,完全无能为力。 研究团队在小鼠实验中做了一个对比:用免疫抑制剂控制炎症的小鼠,CUX2+神经元的损伤仍在缓慢积累;而同时激活ATF4修复通路的小鼠,神经元死亡率下降了60%。这意味着,未来的治疗必须“双管齐下”:一边控制炎症,减少DNA损伤的来源;一边增强神经元自身的修复能力,补上现有治疗的盲区。
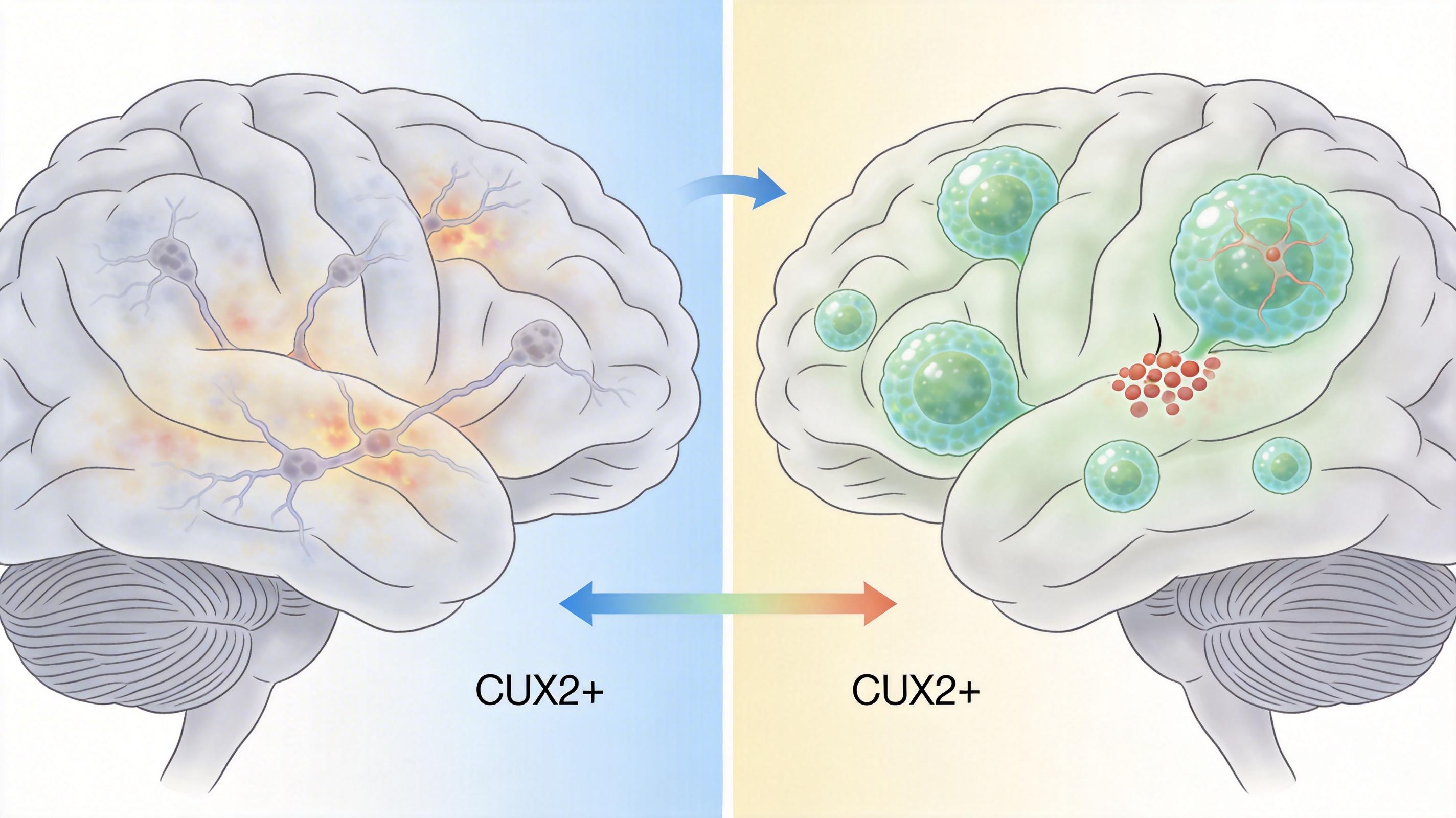
当然,这一机制也存在局限:目前的研究只验证了CUX2+神经元在多发性硬化症中的损伤,其他神经退行性疾病(如阿尔茨海默病)是否存在类似的神经元选择性损伤,还需要更多研究。而且直接激活ATF4通路可能带来的副作用,比如影响细胞正常的转录活动,也需要进一步探索。
当我们谈论神经退行性疾病时,总习惯把目光放在“被攻击的目标”上——比如髓鞘、淀粉样蛋白、tau蛋白。但这次的研究提醒我们,有些神经元的死亡,不是因为被外力摧毁,而是自身的“维护系统”先垮了。 “神经元的命运,藏在DNA的修复能力里。”这句话不仅适用于多发性硬化症,也适用于所有需要长期存活的神经元。未来的某一天,当医生给多发性硬化症患者开药时,处方上可能会同时出现免疫抑制剂和DNA修复激活剂——前者帮大脑挡住外敌,后者帮神经元修好自己的隐形伤口。
点击催更,成为大圆镜下一个视频选题!