对抗知识焦虑,从看懂这条开始
App 下载
肺腺癌的隐藏刹车:UFMylation调控的抑癌通路
蛋白质修饰|AKT蛋白|PHLDA3蛋白|UFL1酶|UFMylation|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
蛋白质修饰|AKT蛋白|PHLDA3蛋白|UFL1酶|UFMylation|肿瘤学|医学健康
你或许听过肺癌的靶向药、免疫疗法,但很少有人知道,我们细胞里藏着一套自带的“刹车系统”——它不是靠药物激活,而是靠一种叫UFMylation的蛋白质“修饰术”精准调控。
2026年《Cell Reports》上的一项研究,终于把这套刹车的运作逻辑拍在了明面上:在肺腺癌中,一种叫UFL1的酶会给PHLDA3蛋白“贴标签”,让它牢牢守在细胞膜上,把疯狂促癌的AKT蛋白死死摁住。而一旦这套修饰系统出了故障,刹车失灵,肺腺癌就会进入加速模式。
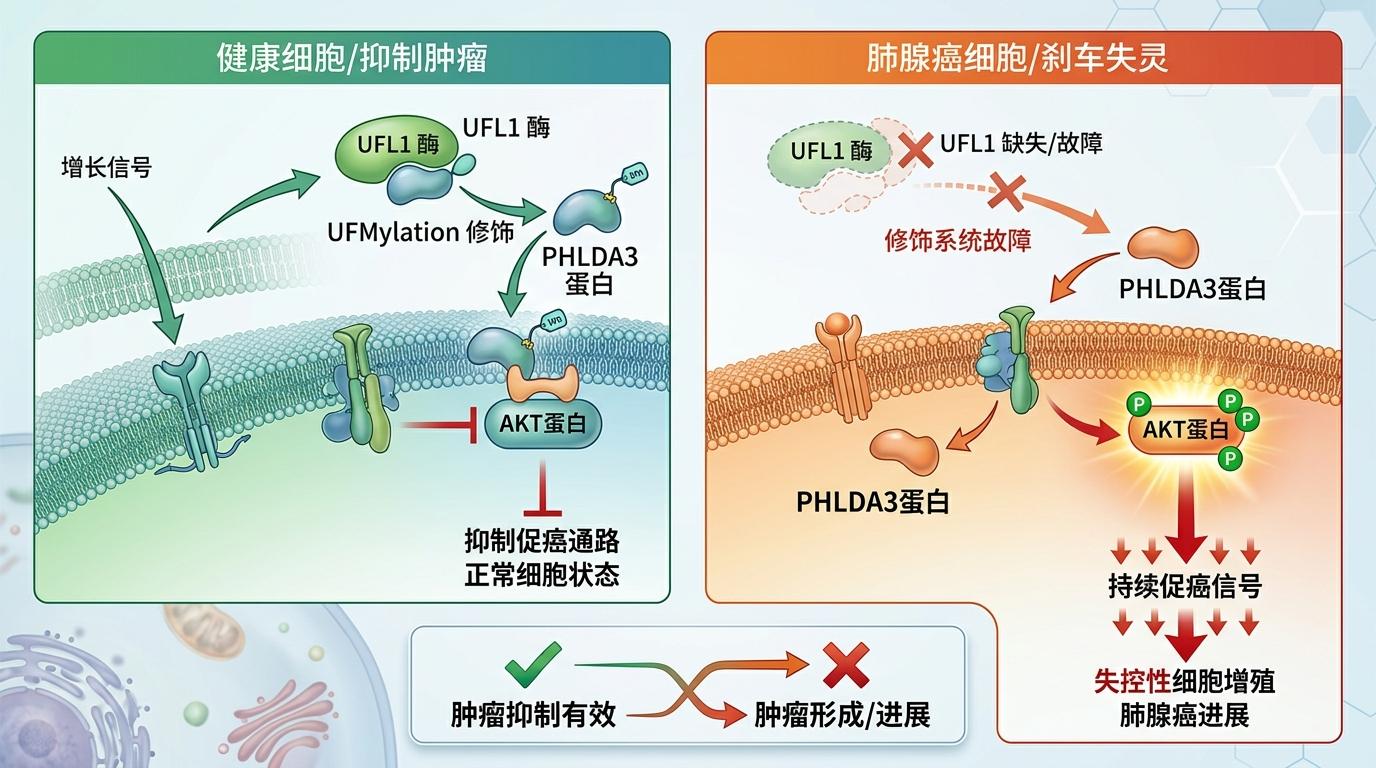
问题是,这套刹车为什么会失灵?又该怎么把它重新拧上?
要理解这套刹车系统,得先搞懂什么是UFMylation——你可以把它想象成细胞里的“快递贴单员”,用UFM1这个特殊“标签”,给特定蛋白质做标记,改变它们的位置和功能。这套系统有三个核心成员:负责激活标签的E1酶UBA5、负责传递标签的E2酶UFC1,以及负责精准找对“快递收件人”的E3酶UFL1。
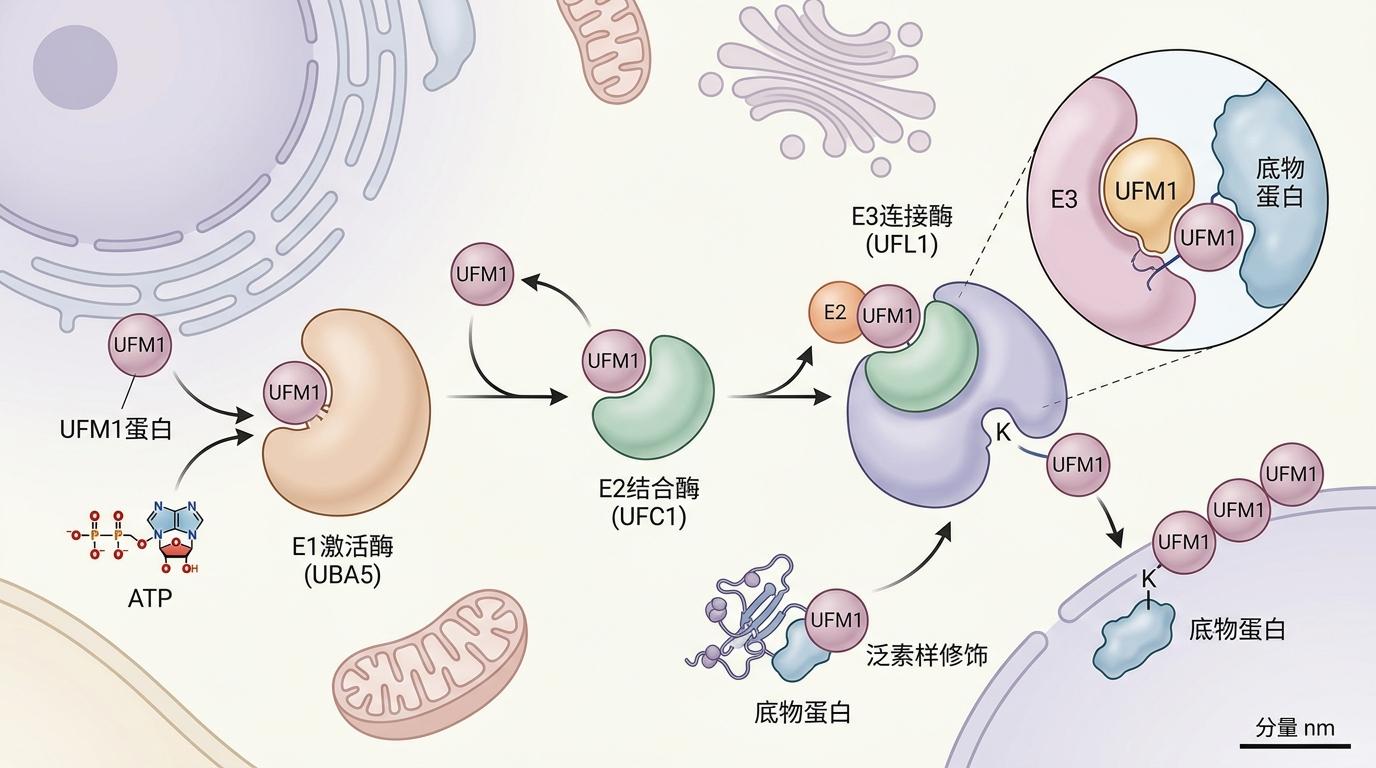
和我们熟悉的泛素化不同,UFMylation是个“小众工种”,只给特定蛋白贴标签,调控的都是细胞里的关键大事:比如修复受损的DNA、维持内质网的蛋白质生产秩序,还有——给癌细胞踩刹车。
在肺腺癌里,这个“收件人”就是PHLDA3。它是AKT蛋白的天然死对头:AKT是个疯狂的“细胞增殖司令”,一旦跑到细胞膜上结合PIP3分子,就会发出指令让细胞无限分裂;而PHLDA3能抢先一步结合PIP3,把AKT挡在细胞膜外,让它成了“没兵的司令”。
但PHLDA3自己也需要“助力”——UFL1给它贴的UFM1标签,能让它的“抢位能力”大幅提升,牢牢钉在细胞膜上,不给AKT任何可乘之机。
科学家在肺腺癌患者样本里发现了一个诡异的规律:约69%的肿瘤组织里,UFL1的含量明显降低,而同时有71%的肿瘤里,AKT蛋白处于过度激活状态。更关键的是,86%的低UFL1肿瘤,都伴随着高活性的AKT——这直接坐实了UFL1-PHLDA3-AKT这条刹车线的存在。
而刹车失灵的根源,就出在PHLDA3的突变上。
研究找到了三个最常见的突变位点:F41L、E82G和K106N。这些突变看似不起眼,却能精准破坏UFL1给PHLDA3贴标签的过程——要么让PHLDA3没法和UFL1结合,要么让标签贴错位置。没有了UFM1标签的PHLDA3,就像失去了磁铁的铁块,没法再牢牢吸附在细胞膜上,只能在细胞质里“飘着”。
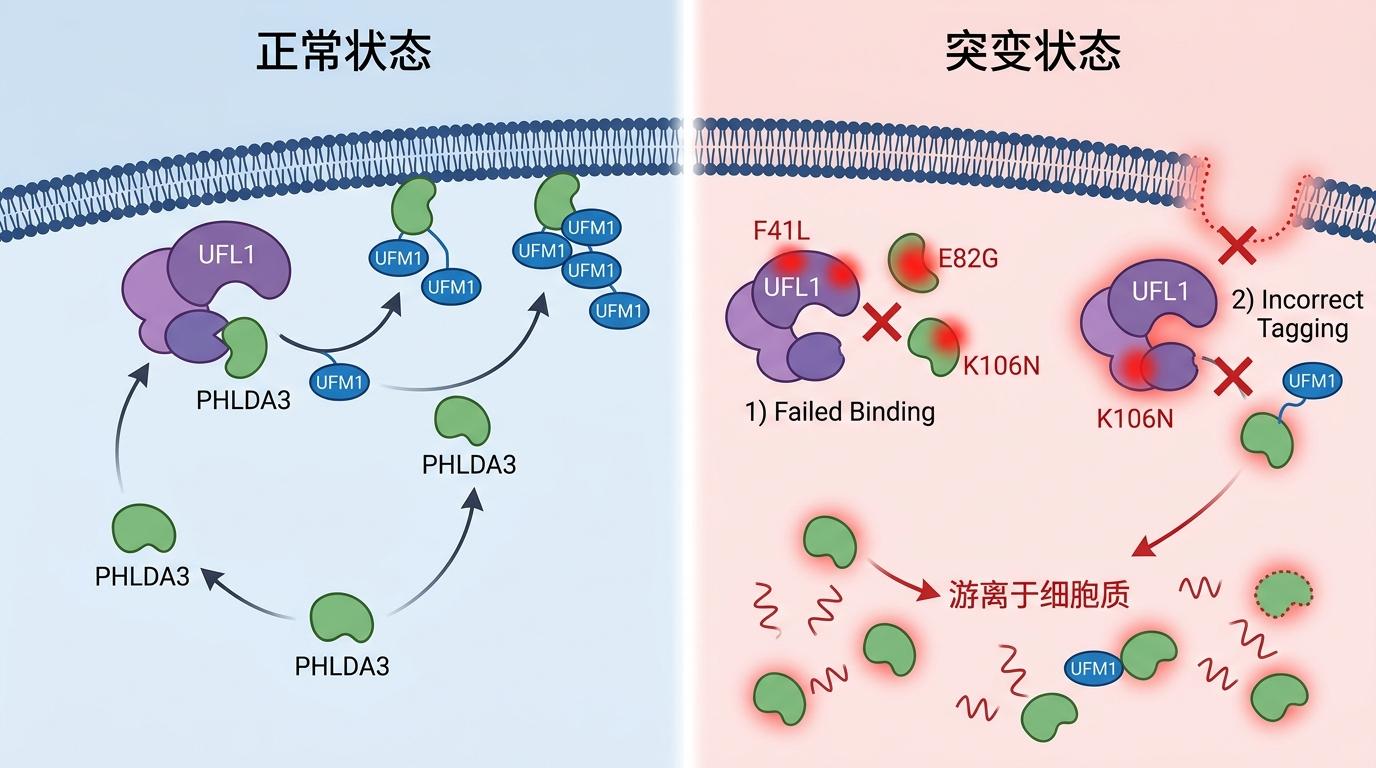
这下AKT彻底解放了。它能毫无阻碍地跑到细胞膜上结合PIP3,激活下游一系列促癌信号:细胞开始疯狂增殖,对化疗药物顺铂、紫杉醇的抗性也跟着增强,肿瘤进展速度直接翻倍。
在细胞实验和患者来源异种移植模型里,科学家验证了这套逻辑:给肿瘤细胞补上UFL1,PHLDA3就能重新回到细胞膜上,AKT的活性被抑制,肿瘤生长速度明显放缓;而如果把PHLDA3敲除,就算UFL1再多,也没法阻止AKT搞破坏。
有意思的是,UFMylation这套“贴标签”系统,还在肿瘤免疫里扮演着双重角色。
一方面,它能给免疫检查点蛋白PD-L1贴标签,促进PD-L1的降解——PD-L1是肿瘤细胞用来“躲猫猫”的伪装,降解后,T细胞就能更容易发现并攻击肿瘤。科学家甚至找到了能增强这种修饰的抑制剂compound-8,用它配合PD-1抑制剂,能大幅提升免疫治疗的效果。
但另一方面,它也能给T细胞表面的PD-1蛋白贴标签,让PD-1更稳定——PD-1是T细胞的“刹车”,稳定后会抑制T细胞的活性,反而帮了肿瘤的忙。
这种看似矛盾的调控,恰恰说明UFMylation是个极其精细的“分子开关”:它在不同细胞、不同蛋白上的作用,可能完全相反。这也给未来的治疗提出了挑战:我们需要的不是简单地激活或抑制UFMylation,而是精准地调控它在特定靶点上的功能。
目前已经有针对UBA5的抑制剂进入早期研究,比如DKM 2-93,能有效抑制UFMylation的整体活性,在肺腺癌模型里显示出了抑制肿瘤生长的潜力。但要把这些实验室里的发现变成临床能用的药物,还有很长的路要走——毕竟,我们得确保药物只在肿瘤细胞里“拧刹车”,不会误伤到正常细胞里的UFMylation系统。
过去我们对抗肺腺癌,大多是盯着AKT这类“致癌司令”猛打,却忽略了细胞里自带的“刹车系统”。这次的研究,就像给我们打开了一扇新的窗户:原来不用直接对抗AKT,只要把PHLDA3的“刹车踏板”重新踩下去,就能让疯狂的肿瘤慢下来。
修饰定生死,精准见疗效。这句话或许能概括UFMylation研究给我们的启示:在分子层面,一个小小的标签修饰,就能决定细胞是走向正常还是癌变;而未来的癌症治疗,也必然会从“广谱打击”走向“精准调控”——找到那些被忽略的分子开关,用最轻柔的方式,把失控的细胞拉回正轨。
毕竟,最好的治疗,往往是让细胞自己恢复秩序。