对抗知识焦虑,从看懂这条开始
App 下载
给癌细胞装监控,看清它的信号暗箱
麻省理工学院|荧光探针|细胞信号天线|HER2|EGFR|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
麻省理工学院|荧光探针|细胞信号天线|HER2|EGFR|肿瘤学|医学健康
你可能听过EGFR、HER2这些癌症靶点,但你不知道的是,这些细胞表面的「信号天线」,一直藏着一个连科学家都摸不透的暗箱——它们到底怎么配对、配对能撑多久,致癌突变又怎么把正常信号拧成致命指令?
过去几十年,这个问题像被锁在黑盒子里:传统荧光探针一照就灭,根本追不上那些可能持续几十秒甚至更久的分子互动。直到2026年4月,麻省理工学院的团队掏出了一盏「永不熄灭的灯塔」,第一次把这个暗箱的门彻底推开了。
你可以把传统荧光探针想象成一次性打火机——点几下就没火,还时不时闪一下。有机染料撑不过10秒,量子点会随机「黑屏」,连最耐用的荧光蛋白,也撑不过持续激光照射的5分钟。而癌细胞里的受体二聚化,偏偏是个慢动作:有的配对能持续几十秒,甚至几分钟。
这次用到的上转换纳米颗粒,是个完全不同的路数。它靠近红外光激发——就是那种能穿透皮肤的红外光——再把低能红外光转换成高能可见光。没有自发荧光干扰,不会中途黑屏,更不会被激光照到「熄火」。
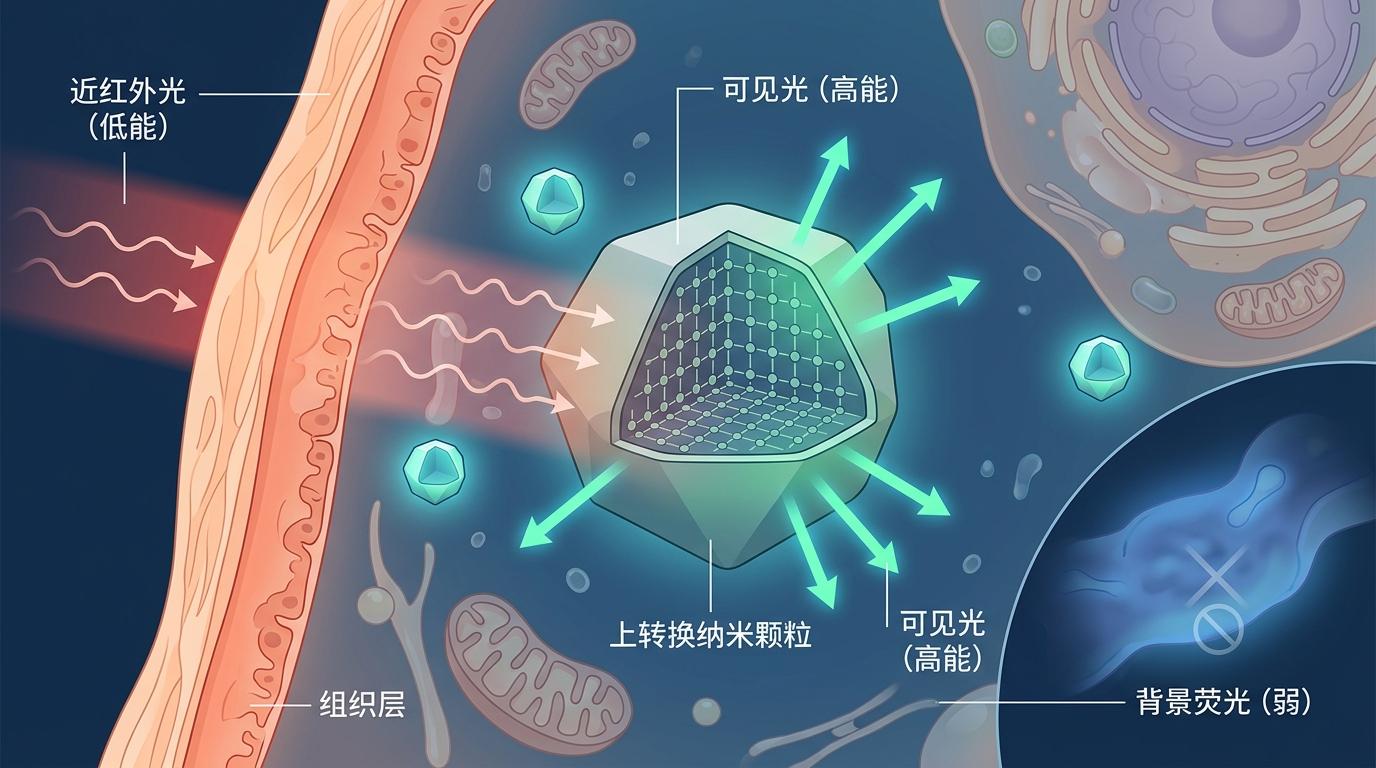
直给数据:
MIT团队给这种纳米颗粒套了三层壳:核心负责发光,中间层把能量牢牢锁住,外层裹上PEG分子避免被细胞当成垃圾清除。就像给灯塔装了防雾罩和永久电源,终于能在活细胞里做「长曝光拍摄」了。
过去科学家一直以为,HER3是个「依附者」——只能跟EGFR或HER2配对,自己单独待着的时候就是个「废柴」。但这次的长曝光追踪,直接推翻了这个结论。
他们看到,HER3会自己跟自己配对,形成稳定的同源二聚体。更关键的是,这些配对是「非活性」的——就像把天线暂时收进了储存库,不让它随便跟其他受体结合发出信号。而致癌突变会把这个储存库的门砸开,释放出大量游离的HER3,跟EGFR或HER2配对,发出持续的增殖信号。
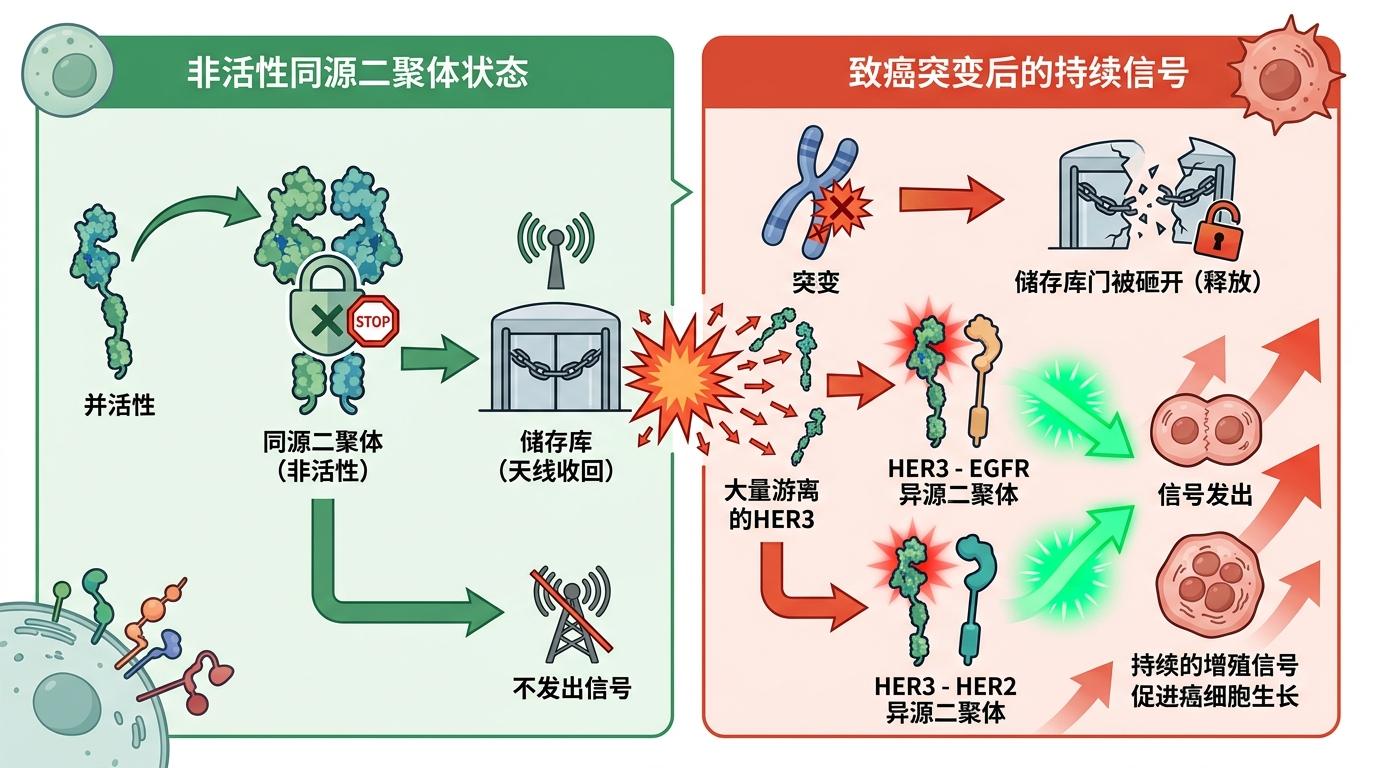
另一个颠覆认知的发现是:即使没有配体刺激,EGFR、HER2、HER3之间也一直在悄悄配对。过去我们以为「没信号就是没配对」,但实际上,细胞表面一直有一张默认的信号网络,配体只是把其中一些配对「加固」了。
不同致癌突变的影响也第一次被拍得明明白白:EGFR的常见突变会让同源二聚体变得异常稳定,相当于把天线永久架起来;而HER2突变的影响要温和得多,只是让它更容易跟其他受体搭伙。
当然,这项技术也有局限:目前还只能追踪三种受体,更小的纳米颗粒亮度还不够,而且没人知道这些纳米颗粒在细胞里待久了会怎么样。但它已经打开了一扇门——我们终于能看到癌细胞里的信号,是怎么从「小动作」变成「大灾难」的。
上转换纳米颗粒的市场已经在悄悄生长:2024年全球估值2.45亿美元,预计到2033年能涨到11.2亿美元。但从「实验室工具」变成「临床武器」,还有几道坎要跨。
首先是亮度和尺寸的平衡:现在的有效颗粒是10纳米,再小就会亮度暴跌,而要追踪更小的分子,得把颗粒缩到5纳米以下。其次是生物相容性:虽然PEG修饰已经降低了毒性,但长期留在体内的代谢路径还没完全搞清楚。
不过最关键的,是把「看到的动态」变成「能打的靶点」。比如HER3的储存库机制,就给了我们一个新思路:与其直接抑制HER3,不如想办法把它重新关回储存库,让它没法跟其他受体配对。已经有团队在尝试设计能诱导HER3同源二聚体的小分子,要是成功,可能比直接阻断信号的副作用小得多。
还有耐药性问题:很多EGFR抑制剂用到最后会失效,就是因为癌细胞改走HER3的信号通路。现在我们能看到这个切换的全过程,说不定就能找到打断它的时机——比如在HER3刚从储存库里出来的时候,就给它套上「枷锁」。
我们对癌症的认知,一直是在「盲人摸象」:从最初看到细胞长得不对劲,到找到致癌基因,再到看清信号通路的静态结构。现在,终于能看到这个通路的「动态直播」了。
看得越细,打得越准。 这不是一句空话:当我们能看清HER3怎么从储存库里跑出来,能看清突变怎么把天线焊死在激活状态,那些过去看起来无解的耐药性,那些找不到靶点的癌症,说不定就有了新的突破口。
未来的抗癌药,可能不再是「一刀切」地阻断信号,而是像精准调控的开关——该关的关上,该锁的锁住,让癌细胞的信号网络,重新回到该有的秩序里。