对抗知识焦虑,从看懂这条开始
App 下载
细菌用蛋白质造DNA,改写遗传规则
噬菌体|蛋白质模板|DRT3防御系统|Alex Gao团队|斯坦福大学|分子细胞生物学|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
噬菌体|蛋白质模板|DRT3防御系统|Alex Gao团队|斯坦福大学|分子细胞生物学|生命科学
如果有人告诉你,造DNA不一定需要DNA或RNA当模板——就像盖房子不用图纸,靠工匠的手就能砌出精准的砖墙——你大概率会觉得是天方夜谭。毕竟半个多世纪以来,分子生物学的核心共识就是:遗传信息的复制,必须依托核酸模板。但2026年4月,斯坦福大学Alex Gao团队在《Science》发表的研究,彻底打破了这个常识。他们发现一种叫DRT3的细菌防御系统,居然能用蛋白质当模板合成DNA,而这一切,只是细菌对抗病毒的生存策略之一。这种“无中生有”的DNA合成,到底是怎么实现的?
要理解这套系统,得先回到细菌和噬菌体的“军备竞赛”现场——这是一场持续了数十亿年的攻防战:噬菌体把DNA注入细菌细胞,疯狂复制自己,最后撑破宿主细胞扩散;细菌则演化出CRISPR、限制修饰系统等武器反击。DRT3就是细菌最新被发现的秘密武器之一。
它由两个逆转录酶Drt3a、Drt3b,再加一段非编码RNA组成。当噬菌体的ST61蛋白出现——相当于细菌检测到“敌人入侵”的信号——这套系统就会被激活。
两个酶的分工像一场精密的双人舞:Drt3a是循规蹈矩的那个,它遵循经典的“模板合成”逻辑,以非编码RNA里的ACACAC序列为蓝图,合成出对应的poly(GT) DNA链。
真正的颠覆来自Drt3b。
你可以把它想象成一台自带模具的打字机——不需要纸面上的字母模板,只要按键,就会反复打出“ACACAC”的固定序列。真实的机制比这更精确:Drt3b的活性位点上,几个特定的氨基酸残基(比如Glu26、Arg253)构成了一个“空间模具”,能精准识别并抓取腺嘌呤(A)和胞嘧啶(C),按固定顺序拼接成DNA链。没有核酸模板,完全靠蛋白质自身的结构定序。
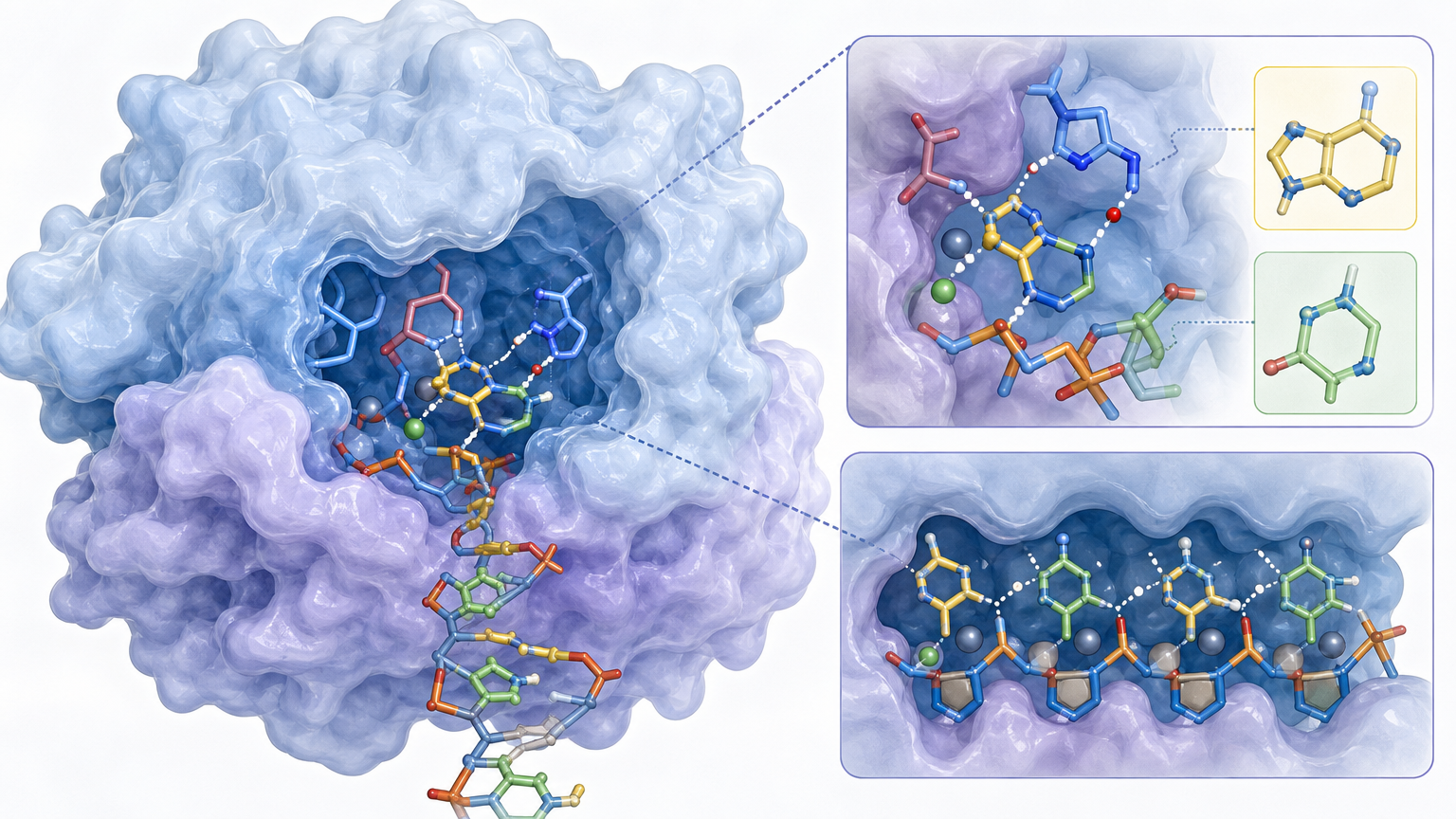
为了看清这套系统的真实模样,研究团队用冷冻电镜拍下了DRT3复合物的高分辨率三维结构——画面像一个完美的六边形齿轮:6个Drt3a和6个Drt3b交替排列,中间由6段非编码RNA撑起整个环状结构。
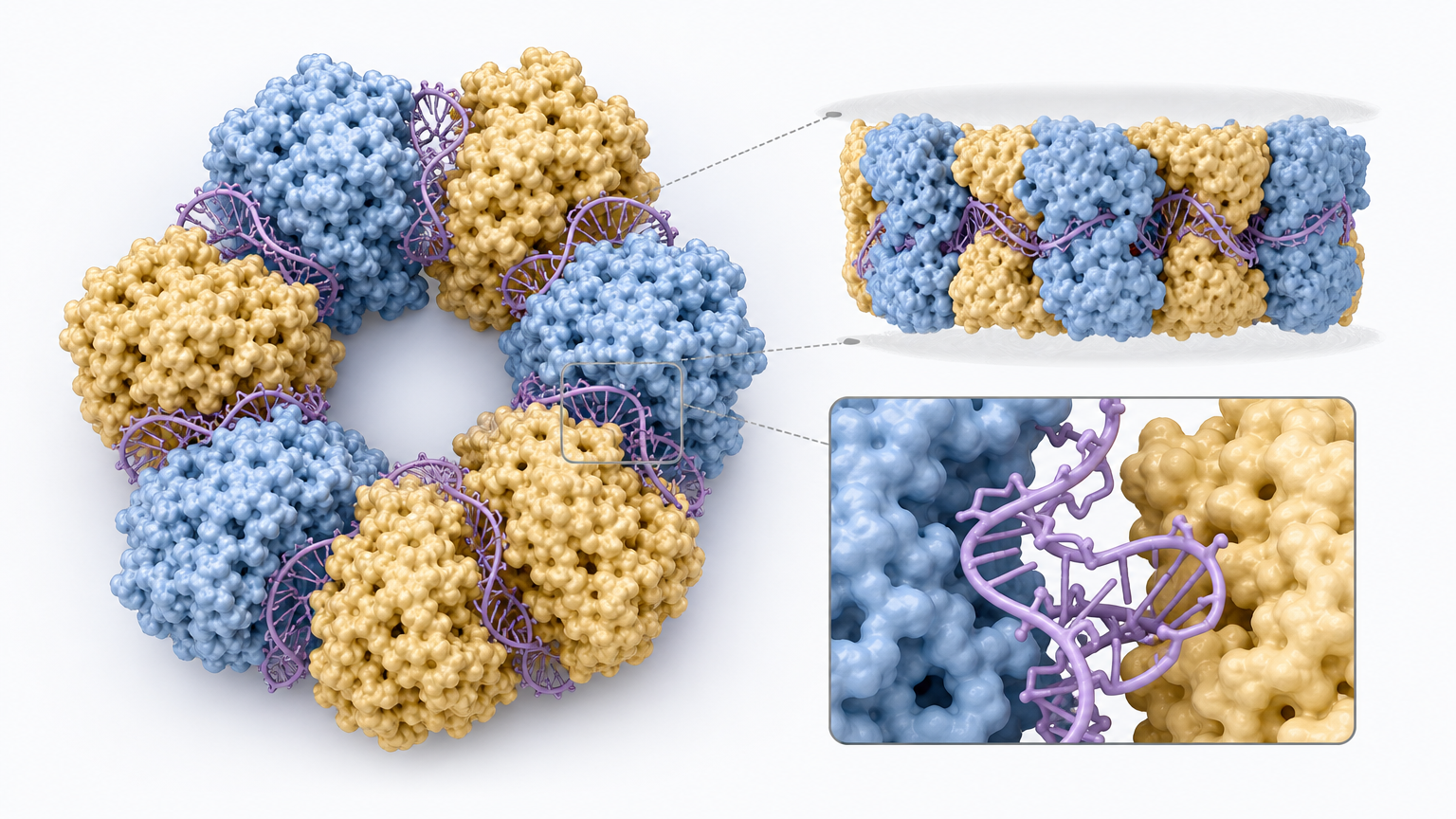
这个对称设计暗藏玄机:它能让两条互补的DNA链同步合成,效率直接拉满。非编码RNA在这里扮演了双重角色:既是Drt3a的合成模板,又是整个复合物的“骨架”,把两个酶牢牢固定在正确的位置上,确保它们不会“各自为战”。
合成出的是一段由GT和AC交替重复组成的长链双链DNA,它的作用目前还没有完全明确,但有几个合理的推测:可能是个“分子诱饵”,抢着结合噬菌体的复制酶,让病毒没法复制自己的DNA;也可能是个“自杀信号”,触发被感染细菌的程序性死亡,牺牲一个细胞,阻止病毒扩散到整个菌群;甚至可能激活细菌的其他免疫通路,拉起一张更严密的防御网。
不过这套系统也有局限:它只能合成固定的重复序列,没法像核酸模板那样合成任意复杂的DNA链。而且目前科学家还没完全搞懂,细菌是怎么精准识别噬菌体的ST61蛋白,又是怎么控制DNA合成的长度和时机的。
对基础生物学来说,这个发现的意义不亚于给中心法则补了一个新的注脚——原来蛋白质不只是执行功能的“工人”,还能当遗传信息的“模板”。这让科学家开始重新思考:早期生命的遗传信息传递,会不会有更多我们不知道的方式?
而在合成生物学领域,它更像打开了一个新的工具箱。如果能通过蛋白质工程改造Drt3b的“模具”,让它合成我们需要的特定重复序列,就能用它来制造DNA纳米材料——比如更稳定的药物递送载体,或者高密度的DNA数据存储介质。毕竟传统的DNA合成依赖模板,成本高、步骤复杂,而这种“自带模板”的酶,相当于把合成工具直接集成在了蛋白里。
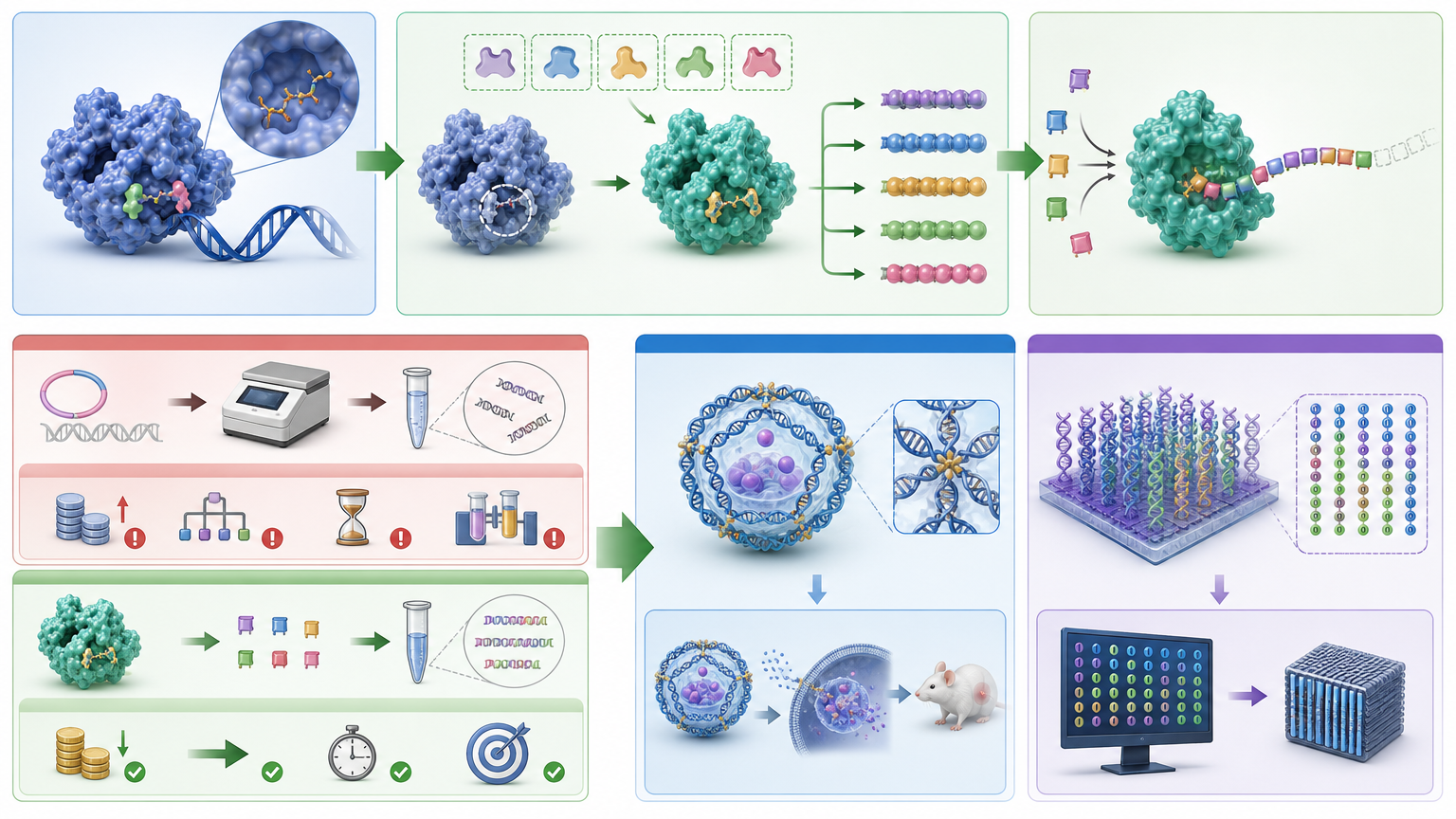
当然,这一切还停留在设想阶段。目前我们甚至还没完全搞清楚,DRT3合成的重复DNA链,到底是怎么干扰噬菌体复制的。但至少,我们已经知道了生命的可能性,比我们想象的要多得多。
当我们以为已经摸透了遗传信息传递的所有规则时,细菌用数十亿年演化出的生存策略,给了我们一记温柔的提醒:生命从不会被人类的定义框住。
蛋白质模板化DNA合成的发现,不是对中心法则的推翻,而是对生命多样性的补充——它让我们看到,为了活下去,生物能演化出多么匪夷所思的办法。就像在一片已经被探索过的森林里,突然发现了一条从未有人走过的小路,你不知道它通向哪里,但你知道,路的尽头一定有新的风景。
生命的规则,永远比我们知道的更多。