对抗知识焦虑,从看懂这条开始
App 下载
170万蛋白结构开源,AI重构药物研发底层逻辑
药物研发流程|分子钥匙|AI蛋白结构预测|蛋白质复合体结构|新药研发|大语言模型|医学健康|人工智能
对抗知识焦虑,从看懂这条开始
App 下载
药物研发流程|分子钥匙|AI蛋白结构预测|蛋白质复合体结构|新药研发|大语言模型|医学健康|人工智能
想象一下:一个藏着170万把“分子钥匙”的免费仓库,突然对全球科学家敞开大门。每一把钥匙,都对应着细胞里驱动生命运转的蛋白质复合体——这些由多条蛋白链缠绕而成的精密机器,曾是困扰人类半个世纪的“黑箱”。过去,解析一个蛋白复合体结构可能耗掉一个实验室数年时间;现在,AI在几天内就能完成百万级别的精准预测。这不是科幻,而是2026年4月摆在全球生命科学家面前的现实。这背后,是AI如何从“辅助工具”变成重构整个药物研发体系的底层力量?
你可以把单链蛋白质想象成一根单独的项链,而蛋白质复合体就是十几根项链缠绕成的巨型挂饰——不仅要知道每根项链的纹路,更要弄清它们如何勾连、嵌套,形成能完成特定任务的结构。过去,科学家只能靠冷冻电镜、X射线衍射等“笨办法”一点点“摸”结构,一个复合体的解析周期以年为单位,且成功率不足30%。
AlphaFold-Multimer的出现打破了这个僵局。它就像给AI装上了能“看见”进化密码的眼睛:通过分析数百万条蛋白质序列的协同进化信号,AI能精准预测不同蛋白链的结合位点和三维构象。你可以把这个过程理解成——通过观察全球不同地区语言的相似词汇,推断出它们共同的祖先语言,只不过AI处理的是氨基酸序列的“进化语法”。
但真实的机制比这更精确:AI会先对每条蛋白链单独预测结构,再通过注意力机制计算链间残基的相互作用能量,最终拼接出整个复合体的原子级模型。这次发布的170万个高置信度结构,就是用这套方法在H100 GPU集群上批量生成的——相当于把过去几十年的结构解析工作量,压缩到了几个月内。
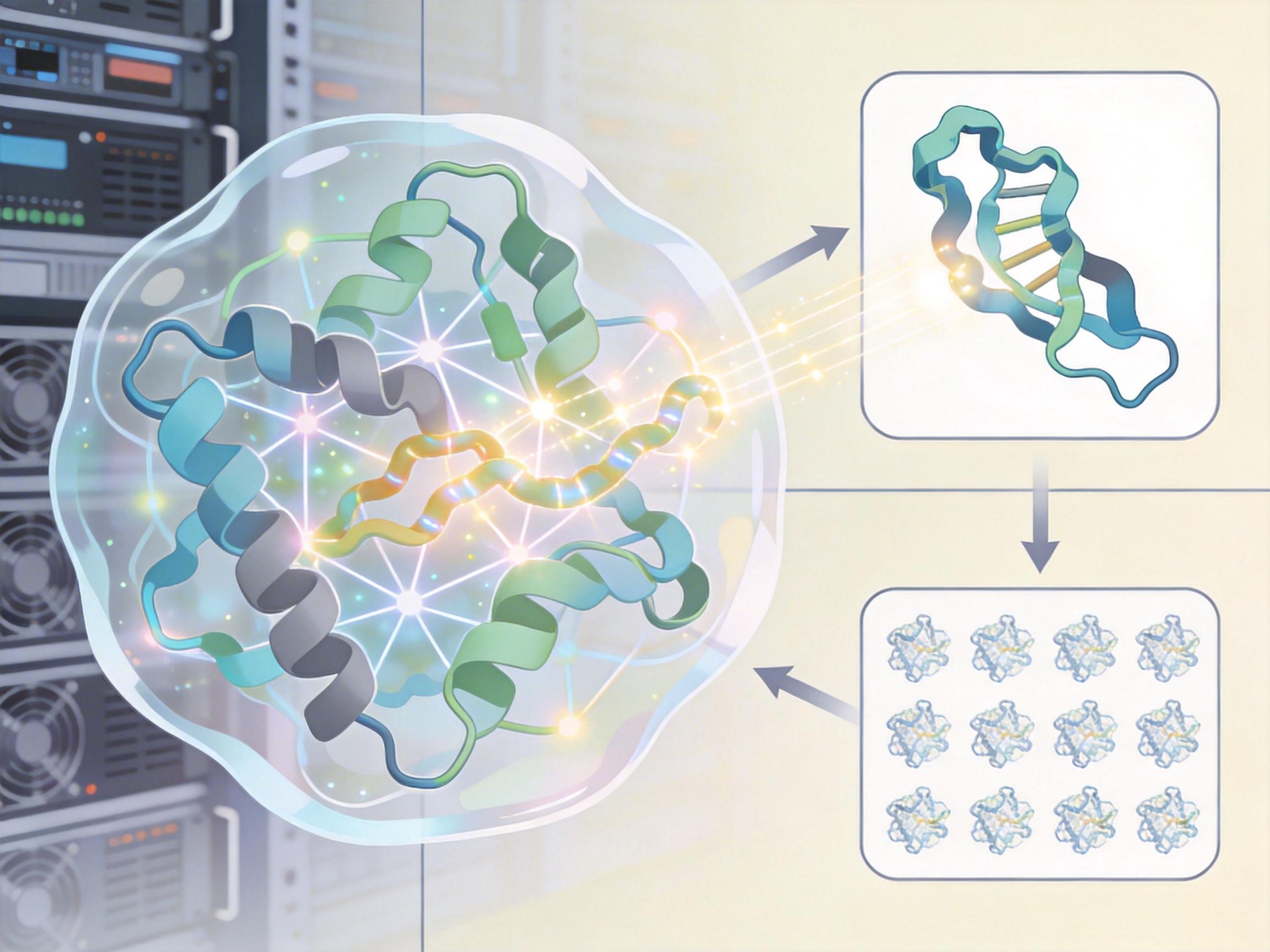
在AI介入之前,药物研发更像一场碰运气的“分子钓鱼”:科学家先锁定一个疾病相关的蛋白靶点,再从数百万个小分子化合物中筛选能结合靶点的“鱼饵”,成功率不足万分之一。而现在,AI能直接从蛋白复合体的结构出发,反向设计出完美匹配结合位点的分子,甚至能创造出自然界不存在的全新蛋白质。
比如该团队推出的蛋白质生成模型,能一步生成具有原子级精度的蛋白序列和结构。在针对127个靶点的湿实验验证中,86个靶点成功命中,其中单个蛋白的命中率高达63.5%,部分分子的亲和力达到皮摩尔级——这意味着它们能像钥匙插进锁孔一样精准结合靶点,直接具备成药潜力。
更重要的是,AI正在把药物研发从“单点突破”推向“体系革命”。2026年初启动的AI药物共创实验室,就是把AI模型、超算集群和自动化机器人整合进同一个闭环:AI设计分子,机器人自动合成并测试,测试数据再反馈给AI优化模型,整个周期从年压缩到月。这种“设计-合成-测试-优化”的自动化流水线,正在系统性降低药物研发的成本和失败率。
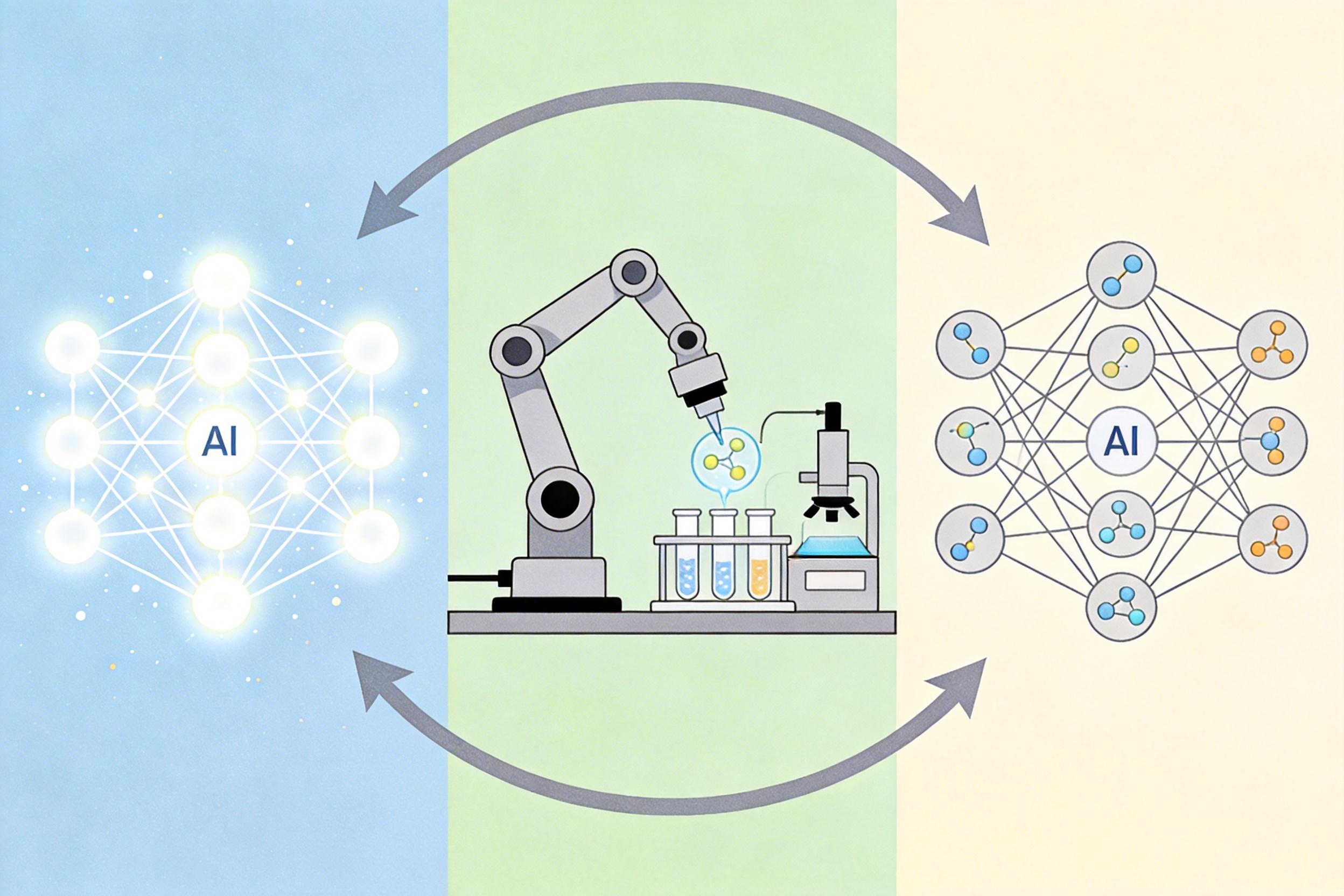
不过,这套体系并非无懈可击。AI模型目前只能预测静态结构,而蛋白质在细胞内是动态变化的——就像一把会变形的钥匙,AI预测的可能只是它最稳定的形态,而非发挥功能时的“工作形态”。此外,AI生成的分子虽然能精准结合靶点,但长期毒性和体内代谢性仍需大量验证,这也是当前AI药物研发的核心瓶颈。
170万个结构的免费开源,看似是科学共享的胜利,但背后藏着数据、伦理与监管的三重隐忧。
首先是数据偏见问题。当前AI模型的训练数据主要来自欧美人群的样本,针对发展中国家常见疾病的蛋白结构数据占比不足5%。这意味着AI设计的药物可能对特定族群效果不佳,甚至存在安全风险——就像用欧美人的脚型设计的鞋子,给亚洲人穿可能不合脚。
其次是生物安全风险。AI能轻松设计出自然界不存在的蛋白质,这既可能带来全新的治疗手段,也可能被用于制造生物武器。比如,通过修改毒素蛋白的结构,就能让它避开现有检测系统,这给全球生物安全监管带来了全新挑战。
最后是监管滞后。目前全球还没有针对AI生成药物的统一监管框架,AI模型的“黑箱”特性让监管机构难以验证其设计逻辑。当AI设计的药物出现不良反应时,责任该归属于模型开发者、药企还是数据提供者?这些问题至今没有明确答案。
当170万个蛋白结构在云端向全球开放时,我们看到的不仅是科学的进步,更是一场关于“知识共享”与“技术伦理”的博弈。AI正在把生命科学的研究门槛从昂贵的实验室设备,降低到能接入互联网的电脑前——一个非洲的研究生,也能借助这些数据设计针对疟疾的新药。
但技术从来都是双刃剑。它能加速治愈疾病的进程,也可能加剧医疗资源的不平等;能破解生命的密码,也可能打开潘多拉的魔盒。真正的挑战从来不是技术本身,而是我们如何用开放的心态拥抱进步,用审慎的态度应对风险。
金句:AI解锁生命密码,更要守住伦理边界