对抗知识焦虑,从看懂这条开始
App 下载
十年寻路铁死亡,找到抗癌新靶点GPX1
抗氧化防线|Wei Gu团队|化疗耐药|铁死亡通路|GPX1蛋白|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
抗氧化防线|Wei Gu团队|化疗耐药|铁死亡通路|GPX1蛋白|肿瘤学|医学健康
当医生告诉你“化疗耐药了”,这句话背后藏着癌细胞的狡猾——它们总能找到活路,躲开药物的追杀。铁死亡,这种依赖铁离子和脂质过氧化的新型细胞死亡方式,曾被寄予厚望,却卡在了“不敢用”的瓶颈:传统诱导铁死亡的药物要么毒性太大,要么一用就杀了正常细胞。直到哥伦比亚大学Wei Gu团队用十年时间,在癌细胞的抗氧化防线里撬开了一道新口子——他们找到了一条天然的铁死亡通路,而控制这道通路的GPX1蛋白,可能是让癌细胞“乖乖自杀”的关键。为什么GPX1能成为安全的抗癌靶点?这得从铁死亡的本质说起。
你可以把铁死亡想象成一场细胞里的“氧化火灾”:铁离子是助燃剂,细胞里的不饱和脂肪酸是燃料,当抗氧化系统失效,火焰就会烧穿细胞膜,让细胞彻底死亡。和我们熟悉的“细胞凋亡”不同,铁死亡专门针对那些依赖抗氧化系统存活的癌细胞——它们疯狂增殖产生的大量活性氧(ROS),本来是致命的,却被GPX4这类核心抗氧化酶死死摁住。
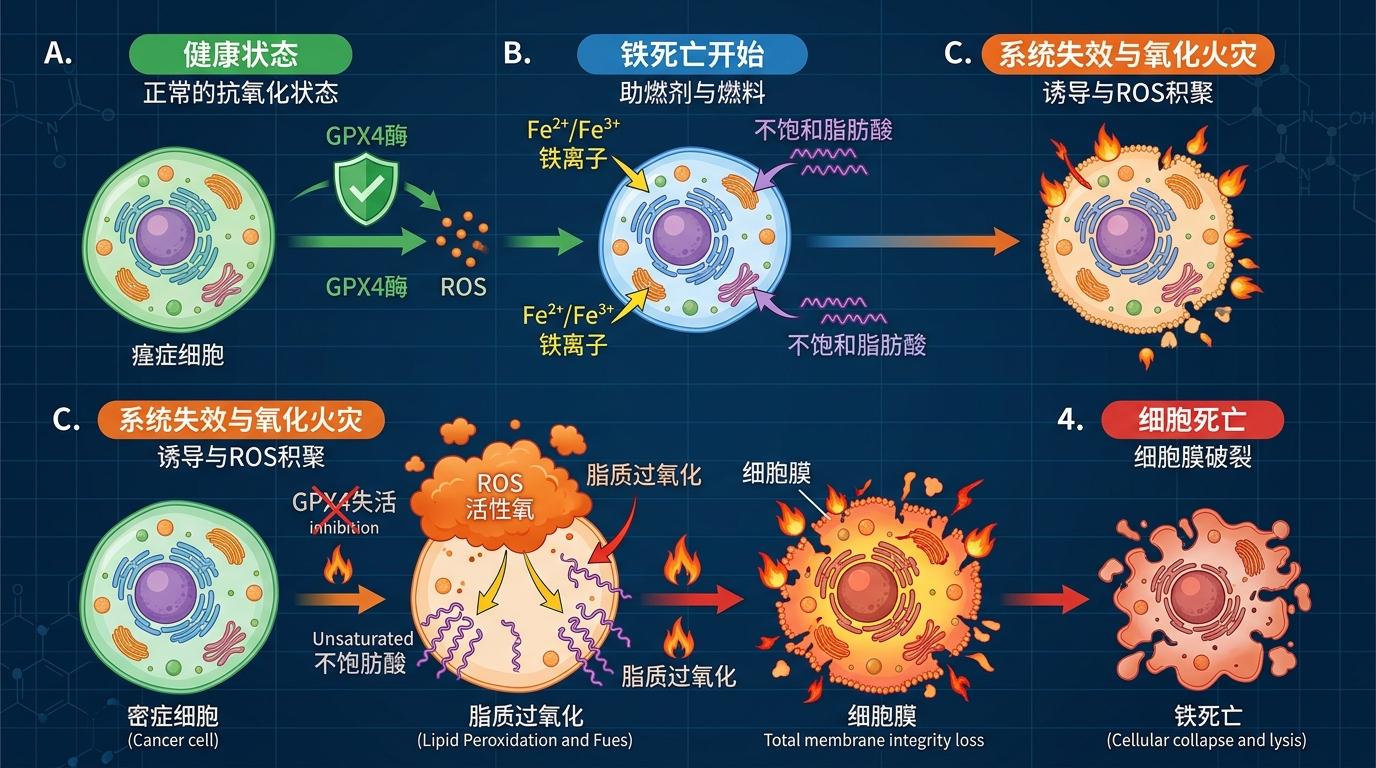
但问题来了,GPX4是正常细胞也离不开的“消防员”。之前科学家用化学药物抑制GPX4诱导铁死亡,结果发现对动物是致命的,这意味着任何靶向GPX4的药物,都可能把正常细胞和癌细胞一起烧死。整个领域陷入了僵局:明明知道铁死亡能杀癌,却找不到安全的打开方式。
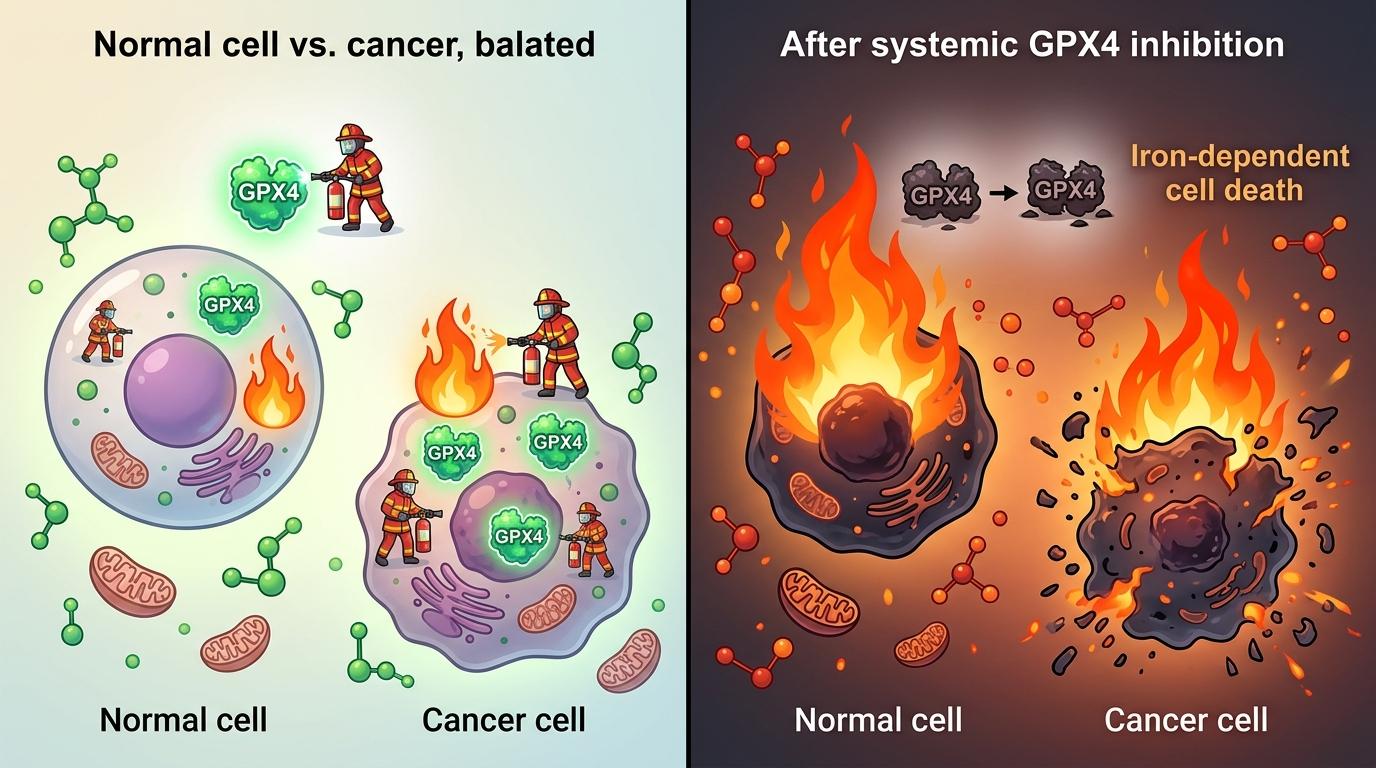
Gu团队在2015年就发现,肿瘤抑制基因p53能启动铁死亡,但他们不知道这条天然通路的其他成员。“文献里全是化学诱导的那套逻辑,我们连从哪找线索都不知道。”Gu说。于是他们决定用CRISPR-Cas9广撒网,把癌细胞的基因挨个敲除,看哪个基因消失后,癌细胞会在ROS刺激下触发铁死亡。
筛选结果指向了一个之前被忽略的蛋白——GPX1。
和GPX4这个“全民消防员”不同,GPX1更像“癌细胞专属保镖”:它是一种抗氧化酶,主要负责清除细胞里的过氧化氢,维持氧化还原平衡。但Gu团队发现,GPX1对正常细胞来说是“可有可无”的——敲除GPX1的小鼠能正常发育、繁殖,完全不影响生存;可对癌细胞来说,GPX1就是“续命符”:它们因为疯狂增殖产生的ROS浓度是正常细胞的数倍,必须靠GPX1不停“灭火”才能活下去。
更关键的是,GPX1不是单独工作的。它会和另一种叫OSBPL8的蛋白结合,形成一个复合物守在内质网膜上,专门清除内质网里的过氧化磷脂酰酸——这是铁死亡扩散的关键“火种”。当这个复合物被破坏,癌细胞里的氧化火灾就会失控,最终触发铁死亡。
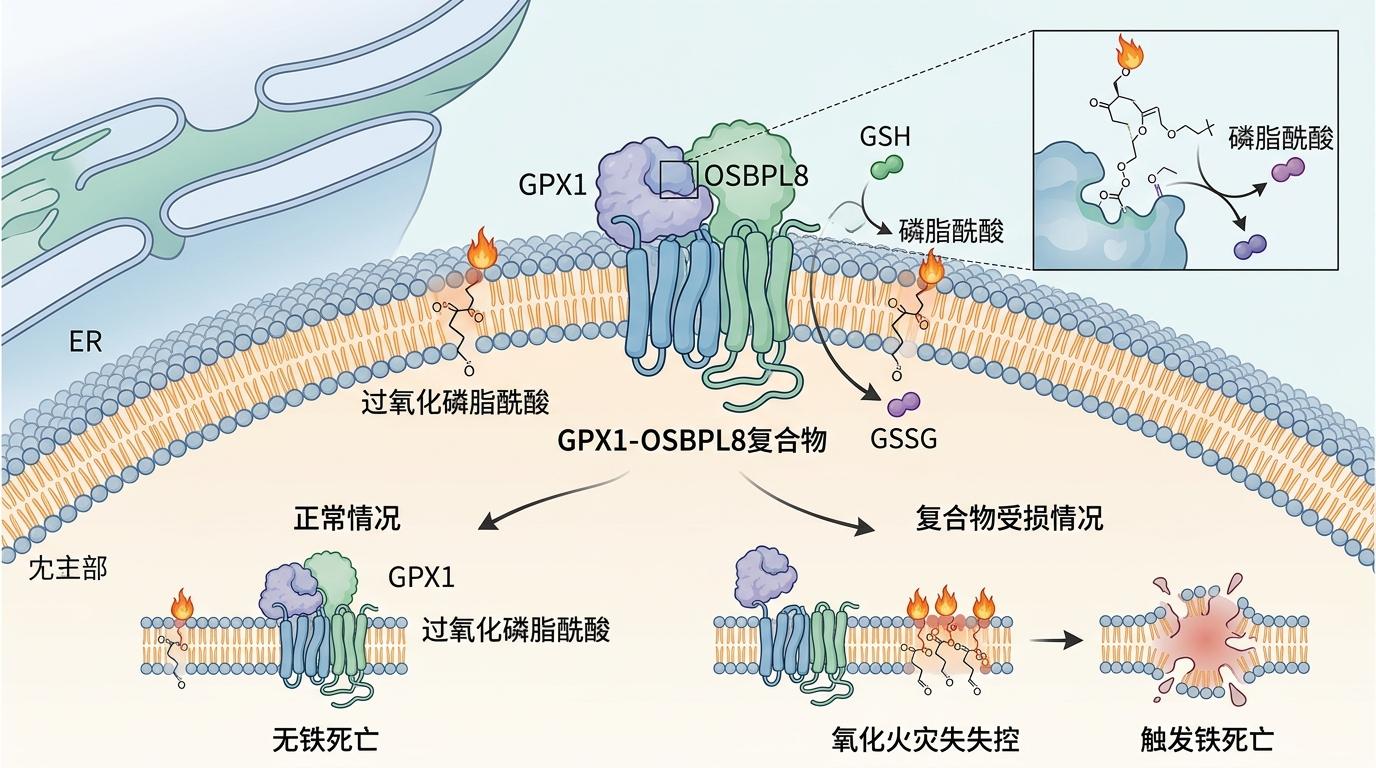
这是一条完全天然的铁死亡通路,和之前依赖化学药物的路径截然不同。更重要的是,它的“开关”GPX1,只在高ROS的癌细胞里发挥关键作用,正常细胞即使失去它,也有其他抗氧化系统补位。
目前Gu团队已经开始研发GPX1抑制剂,从临床前数据看,这种药物的潜力让人兴奋:在小鼠肿瘤模型中,抑制GPX1能让肿瘤体积缩小70%以上,而且对正常组织几乎没有损伤。
但这条路也不是没有挑战。GPX1的活性位点比较“平坦”,很难设计出只针对它的抑制剂,一不小心就会影响其他抗氧化酶;而且不同癌症的ROS水平不同,对GPX1的依赖程度也有差异——比如三阴性乳腺癌、慢性髓性白血病这类高ROS肿瘤,对GPX1抑制剂的响应会更明显,而一些ROS水平较低的肿瘤,可能需要结合其他ROS诱导疗法才能起效。
更值得关注的是,GPX1的作用不止在癌症里。神经退行性疾病比如帕金森病、亨廷顿病,同样存在ROS过高的问题,抑制GPX1可能也能通过调控铁死亡缓解病情,但这需要更严谨的研究来验证——毕竟神经细胞对氧化损伤的耐受度,和癌细胞完全不同。
从2015年发现p53和铁死亡的关联,到2026年找到GPX1通路,Gu团队花了十年时间,终于从“化学诱导”的死胡同里,找到了一条天然的抗癌路径。这十年的研究,本质上是在纠正一个误区:我们总想着用外力“杀死”癌细胞,却忘了细胞本身就有一套“自我清理”的程序。
“靶向癌细胞的命门,而非泛泛的杀伤。”这可能是铁死亡研究给我们的最珍贵启示。未来的抗癌药物,或许不再是不分敌我“狂轰滥炸”,而是像一把精准的钥匙,只拧开癌细胞的死亡开关,让正常细胞安然无恙。而GPX1,就是我们找到的第一把这样的钥匙。