
5 个月前

5 个月前
对无数在辅助生殖道路上跋涉的家庭而言,最深的绝望莫过于“反复着床失败”(RIF)。当一枚枚通过严格筛选的优质胚胎被植入,换来的却是一次次阴性的验孕结果,那种感觉如同将最珍贵的种子播撒在看似肥沃的土壤,却始终等不来破土的嫩芽。临床数据显示,约有15%至20%的不孕患者深陷此困境。长久以来,医生们手握的工具——无论是依赖主观经验的B超内膜厚度测量,还是捕捉静态分子信息的基因阵列检测——似乎都无法完全勘破这片“土壤”的秘密。子宫内膜,这个孕育生命的初始温床,成了一个难以捉摸的“黑箱”。
然而,就在最近,一项发表于《自然·通讯》(Nature Communications)的突破性研究,如同一道强光,照亮了这个“黑箱”的内部。研究团队以一种前所未有的方式,将“芯片技术”与“评分系统”巧妙结合,不仅精准描绘出每个患者子宫内膜的真实状态,更开创了一条从评估、治疗到监测的个性化诊疗新路径。
在过去,评估子宫内膜容受性的主流技术是子宫内膜容受性阵列检测(ERA)。它通过一次性的内膜活检,分析200多个相关基因的表达,来判断所谓的“着床窗口期”是否偏移。这无疑是一次巨大的进步,让人们首次从分子层面窥探内膜的秘密。但ERA的局限也日益凸显:它像一张静态的照片,只能捕捉特定时刻的状态,却无法反映子宫内膜在整个月经周期中随激素变化的动态微环境。此外,其临床有效性也面临争议,一些大规模研究未能证实其能显著提高活产率,让这项技术的应用充满了不确定性。
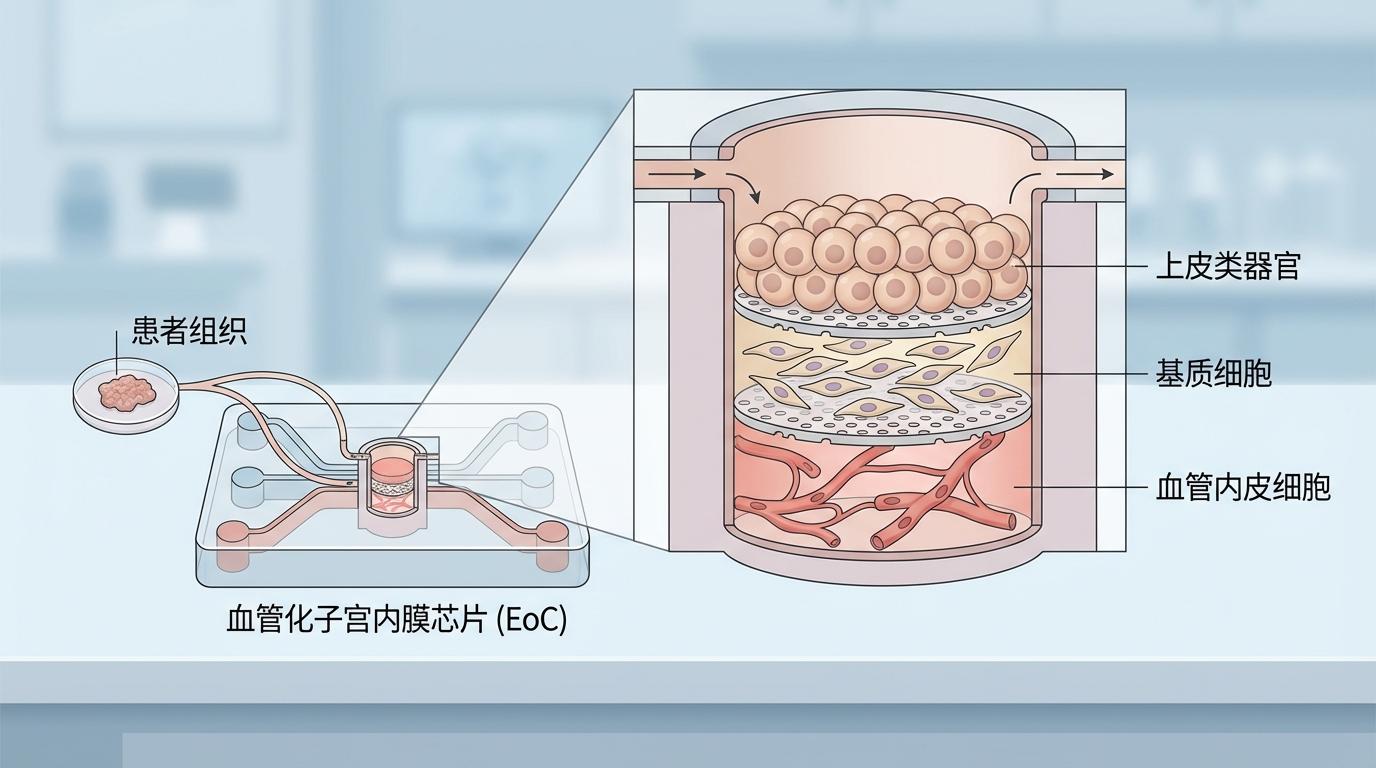
此次研究的核心突破,在于创造了一个“活”的模型——患者来源的血管化子宫内膜芯片(EoC)。这并非简单的细胞培养皿,而是一个高度仿生的微型器官。研究人员从患者身上获取极少量内膜组织,在芯片上重建了包含上皮类器官、基质细胞和血管内皮细胞的三层核心结构。
这个微缩的“子宫花园”拥有惊人的能力:
通过小鼠模型验证,这款芯片的生理还原度极高,其激素受体和关键容受性标志物的表达模式,与体内组织几乎完全一致,成功地将一个动态、复杂且高度个体化的子宫内膜微环境,浓缩到了方寸之间。
有了可靠的“替身”,如何客观地评估它的状态?研究团队随即开发了一套名为**“子宫内膜容受性评分系统”(ERS2)**的量化工具。这套系统如同为子宫内膜的“肥力”打分,主要依据两大维度:
每个指标满分5分,总分20分。研究定义12-20分为具备良好容受性。在对12名不孕患者的测试中,这套评分系统展现了惊人的预测力:正常子宫内膜患者的得分普遍在13-15分,她们后续的胚胎移植大多成功;而反复着床失败的患者,评分则普遍低于12分,后续移植也未能成功。这把客观的标尺,首次让医生能够清晰、量化地判断患者子宫内膜的真实潜能。
这项研究最令人振奋的价值,远不止于精准评估。它将这一平台延伸至个性化治疗,真正实现了“评估-治疗-监测”的一体化闭环。
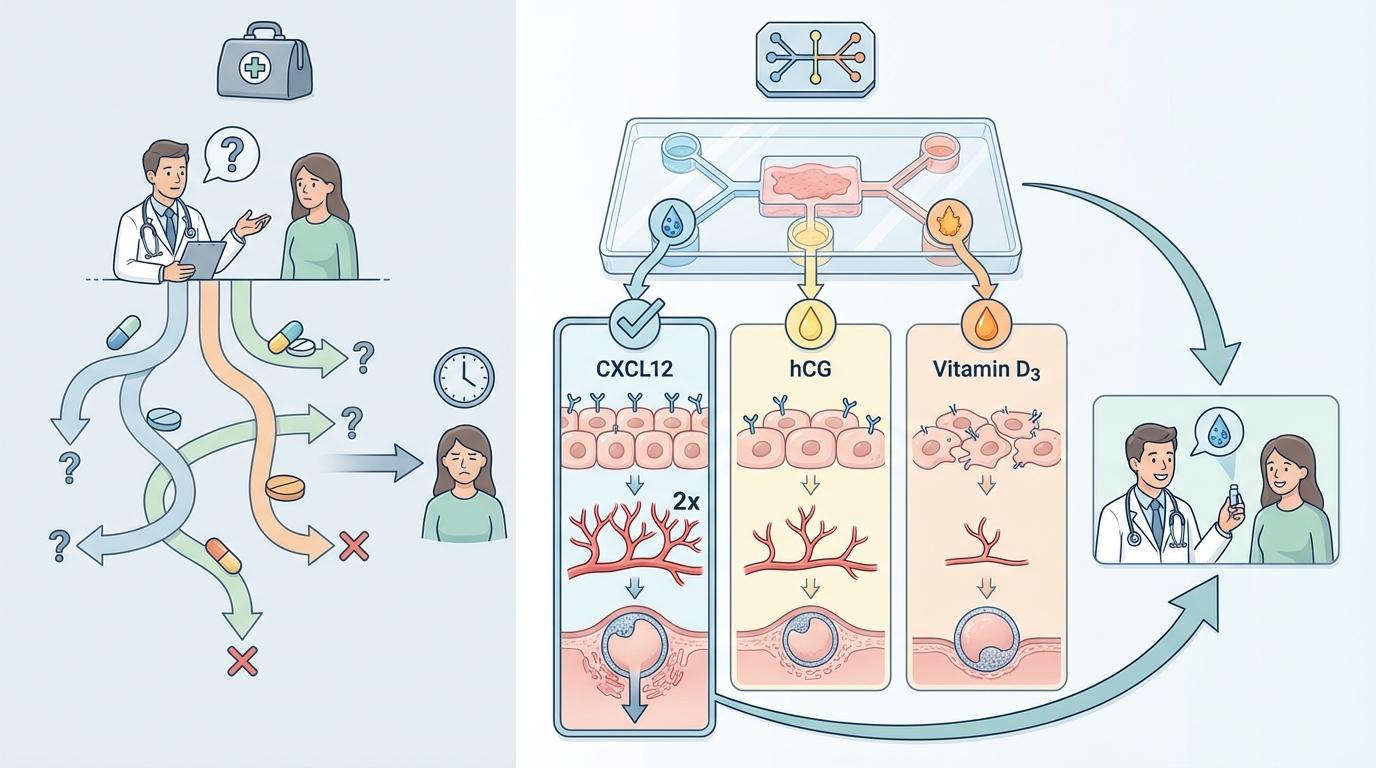
对于一名宫腔粘连的患者,传统的治疗方案往往依赖医生经验,患者可能需要经历漫长的试错过程。而现在,研究团队直接在她的“子宫芯片”上测试了三种潜在的治疗药物:CXCL12、人绒毛膜促性腺激素(hCG)和维生素D3。结果清晰地显示,CXCL12表现最为出色,它不仅能让关键的整合素表达恢复正常,还能使血管芽面积提升两倍,甚至改善了模拟胚胎的滋养层细胞侵袭深度。这意味着,在对患者本人进行任何治疗前,医生就已经找到了最优的候选方案。
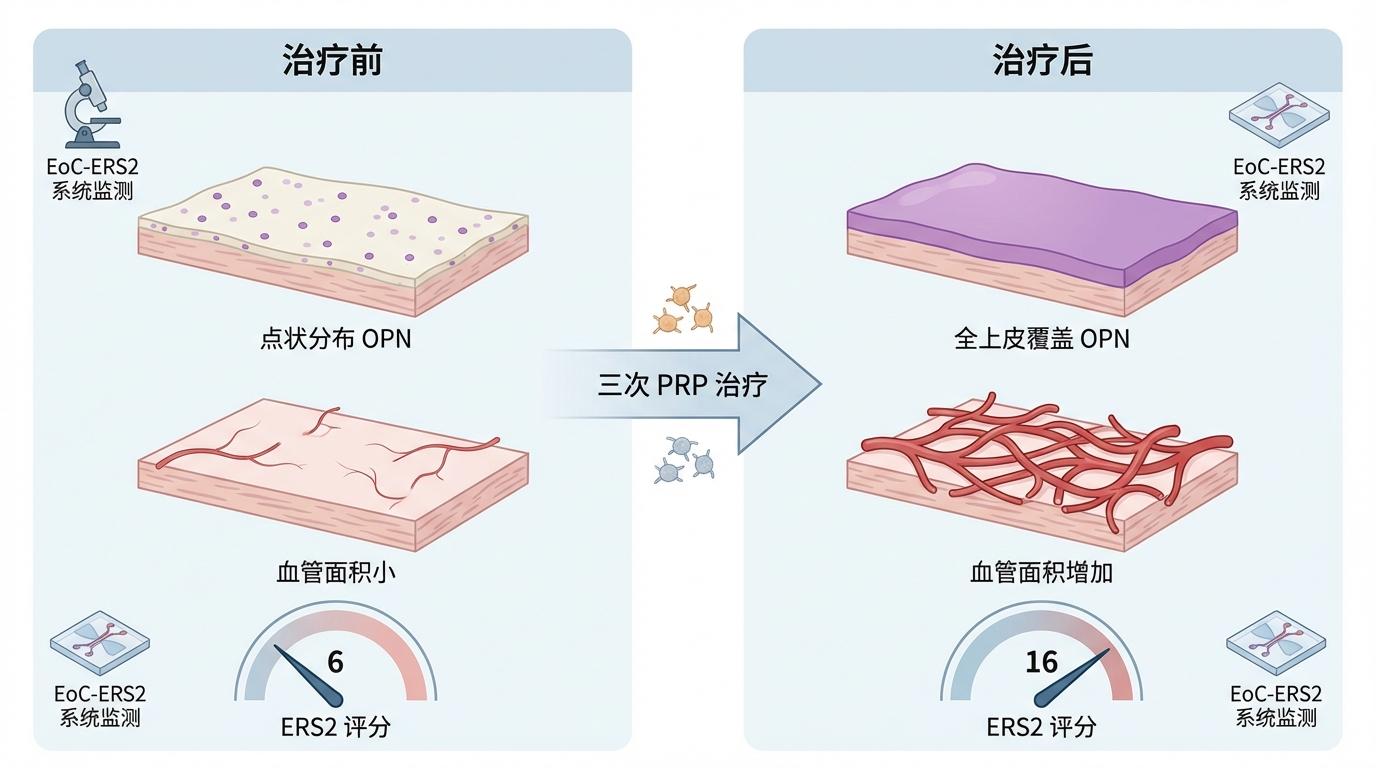
另一个更具说服力的案例来自一名反复着床失败合并反复妊娠丢失的患者。她接受了富血小板血浆(PRP)治疗,这是一种新兴的修复内膜的手段,但其效果一直缺乏客观的监测指标。研究团队利用EoC-ERS2系统全程追踪了她的治疗过程。三次治疗后,芯片上的变化令人鼓舞:原本呈“点状分布”的骨桥蛋白(OPN)变成了“全上皮覆盖”,血管面积增加了一倍,ERS2评分从最初的6分飙升至16分!这个动态变化无可辩驳地证实了PRP治疗的有效性,为患者和医生注入了强大的信心。
“患者来源子宫内膜芯片+评分系统”的组合,标志着生殖医学正从“经验医学”向“精准医学”迈出决定性的一步。它彻底改变了“反复着床失败”的诊疗范式:
目前,这项技术的研发团队已经启动了多中心临床验证,这预示着它距离进入常规临床应用又近了一步。可以预见,随着器官芯片技术的不断成熟和成本的降低,未来每一位面临生育困境的女性,或许都能拥有一个属于自己的“子宫芯片”,它将像一位忠实的向导,引领医生和患者在复杂的生育迷宫中找到最精准的路径。
这不仅仅是一次技术的革新,更是一场观念的革命。它让我们重新认识到,生命孕育的奥秘,可以通过科技的力量被一步步揭示和优化。那个曾经让无数家庭心碎的“黑箱”,正在变得透明,而从这透明中,我们看到了更多新生命诞生的希望。
点击充电,成为大圆镜下一个视频选题!