对抗知识焦虑,从看懂这条开始
App 下载
肺部硬化元凶锁定:一种蛋白“内乱”如何引发致命纤维化?
PNAS期刊|娄红祥团队|山东大学|细胞骨架蛋白|肺纤维化|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
PNAS期刊|娄红祥团队|山东大学|细胞骨架蛋白|肺纤维化|肿瘤学|医学健康
我们的肺,如同一块精密而富有弹性的织物,每一次呼吸都依赖于其数亿个微小气囊的舒张与收缩。然而,随着年龄增长或持续的损伤,这块织物可能悄然发生变化——它逐渐失去柔软,变得僵硬、厚重,布满疤痕。这种被称为“肺纤维化”的病变,如同在生命的气囊中缓慢注入水泥,最终让呼吸变得异常艰难。这不仅是衰老的标志,更是一种致命的倒计时。多年来,科学家们一直在追问:这场无声的硬化,究竟是如何在我们的细胞深处启动的?
就在不久前,这一谜题迎来了关键性的突破。山东大学的娄红祥与董婷团队在国际顶尖期刊《美国国家科学院院刊》(PNAS)上发表了一项里程碑式的研究,将矛头直指细胞内部一种名为**波形蛋白(vimentin)**的“内乱”。
这项于2026年1月20日发布的研究,首次清晰地描绘出了一条从蛋白质失序到器官衰老的完整通路。研究人员发现,在衰老的肺成纤维细胞——负责修复组织、但也可能制造疤痕的“建筑工”细胞——内部,作为细胞骨架关键组分的波形蛋白发生了异常聚集,形成了混乱的团块。这一现象,与细胞的加速衰老和肺纤维化的启动密切相关。
更重要的是,他们找到了这场混乱背后的“失职者”:一种名为**钙腔蛋白(calumenin)**的分子伴侣。正常情况下,钙腔蛋白就像一位尽职的质量总监,确保每一条波形蛋白都能被正确折叠成型。然而,在病理刺激下,细胞内钙信号的异常波动会导致这位“总监”被降解。失去了监管,波形蛋白便开始“野蛮生长”,错误折叠并堆积成团,最终将成纤维细胞推向衰老,并促使其分泌大量导致纤维化的“毒性”因子。
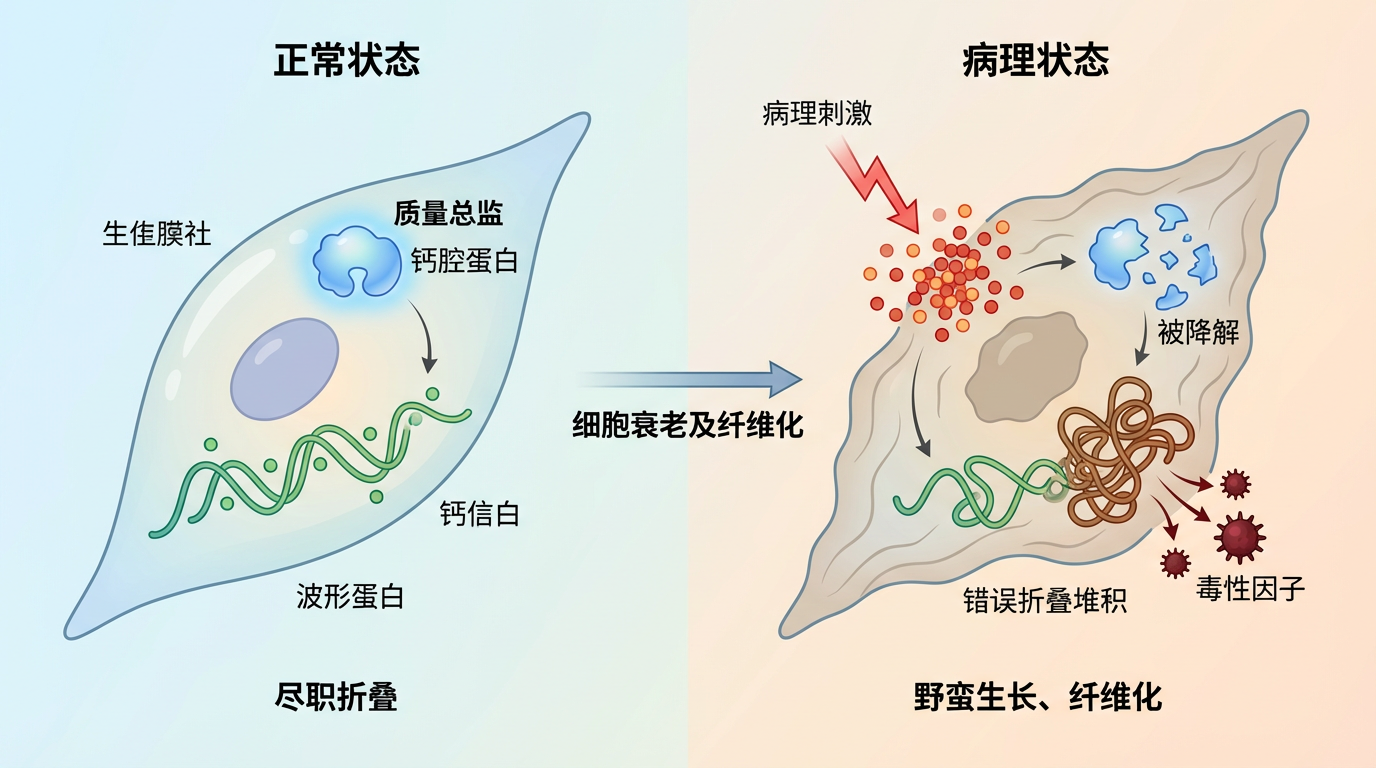
这一发现如同一道闪电,照亮了肺纤维化研究的盲区。它告诉我们,肺部的硬化并非始于宏观的组织损伤,而是源于微观世界里一场关于蛋白质质量控制的“系统崩溃”。
要理解这一发现的重要性,我们必须先了解一个核心概念:蛋白质稳态(Proteostasis)。可以把它想象成一个高效的细胞工厂,每时每刻都在生产、折叠、运输和回收蛋白质。这个工厂拥有一套极其精密的质量控制体系,确保所有蛋白质产品都能合格上岗,而残次品则被迅速销毁。
分子伴侣,如钙腔蛋白,就是这个质控体系的关键员工。它们的职责是帮助新生的蛋白质链正确折叠成三维结构,或是在蛋白质受损时帮助其修复,实在无法修复的则打上“报废”标签,送往降解系统。
当衰老或疾病来临时,这个质控体系的效率会大幅下降。就像工厂里的质检员纷纷离岗,残次品开始堆积。这些错误折叠的蛋白质不仅无法发挥正常功能,还会像黏稠的胶水一样聚集在一起,形成有毒的聚集体,干扰细胞的正常运作。这正是许多衰老相关疾病的共同病理基础:
而娄红祥与董婷团队的研究,则首次将这块“多米诺骨牌”推向了肺纤维化领域。他们证明,波形蛋白的聚集,正是成纤维细胞衰老并最终导致肺部 scarring 的那张关键骨牌。
当成纤维细胞因蛋白质稳态失衡而进入衰老状态后,它并不会安静地“退休”,而是变成了一个麻烦的制造者。衰老细胞会启动一种被称为**“衰老相关分泌表型”(SASP)**的程序,开始向周围环境释放大量的炎性因子、生长因子和组织重塑酶。
这种分泌行为就像一种“恶性通讯”,衰老的成纤维细胞不断向邻近的健康细胞发送“求救”和“警报”信号。这些信号本意是召唤免疫细胞来清除受损组织,但在慢性、持续的衰老状态下,它反而制造了一个长期的、低度的炎症环境。这个环境会:
过去的研究已经证实,通过药物特异性地清除这些衰老细胞(即Senolytics疗法),可以显著缓解小鼠的肺纤维化。而最新的研究则从源头上解释了这些细胞为何会衰老,为我们提供了一个更早、更精准的干预窗口:阻止蛋白质的“内乱”,或许就能阻止衰老细胞的出现和它们的“恶性通讯”。
这项基础研究的突破,正迅速转化为精准医疗的新希望,并与当前的技术浪潮汇合,开辟了多元化的治疗路径。
科学与技术角度: 最直接的启发是,波形蛋白聚集体本身就是一个极具吸引力的新药靶点。研究团队通过筛选,已经发现了一种名为**“9-85”的天然产物**,它能像“拆迁队”一样,特异性地破坏波形蛋白聚集体,并在动物模型中成功缓解了肺纤维化。这验证了靶向蛋白质稳态的可行性。未来,开发更高效、更安全、能够稳定钙腔蛋白或直接清除波形蛋白聚集体的小分子药物,将成为研发的焦点。
产业化前景: 这一发现为制药行业开辟了全新的赛道。目前,针对肺纤维化的药物(如吡非尼酮和尼达尼布)只能延缓疾病进程,无法逆转。靶向蛋白质稳态的策略,则有望从根本上修复细胞功能,实现真正的“对因治疗”。与此同时,人工智能(AI)正在加速这一进程。例如,英矽智能(Insilico Medicine)利用生成式AI平台,已经成功开发出靶向全新纤维化通路的小分子药物INS018-055,并进入临床试验阶段。AI的强大算力可以帮助科学家更快地筛选化合物、预测靶点,与新的生物学发现形成合力。
治疗方式革新: 除了新靶点,给药方式的创新也在重塑治疗格局。传统的口服药物存在全身副作用。针对肺部疾病,吸入式给药正成为趋势。通过将药物制成微米级的颗粒,可以直接递送到肺泡,不仅能大幅提高局部药物浓度,还能显著降低对肝脏、肾脏等器官的负担。目前,吸入型的吡非尼酮和尼达尼布已在临床试验中展现出良好的安全性和潜力。
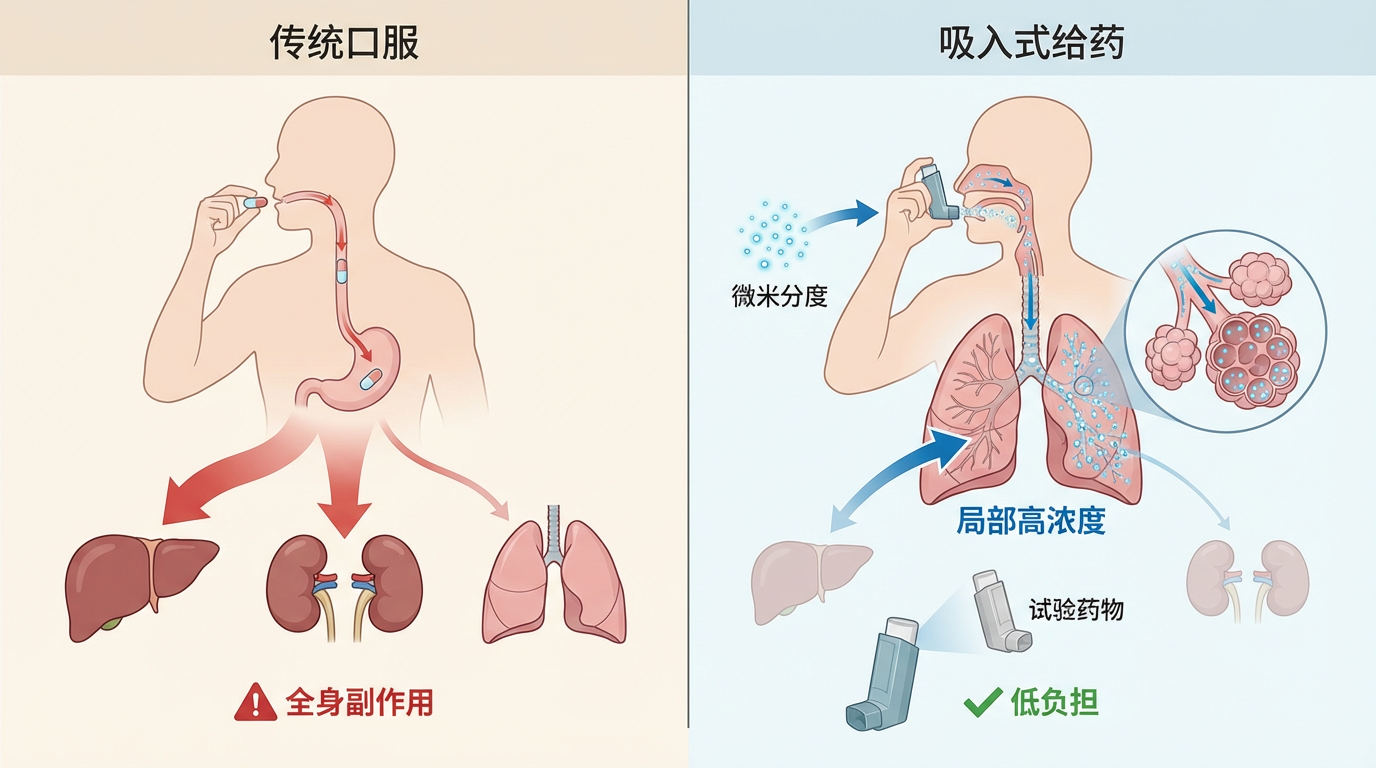
展望未来,对抗肺纤维化乃至衰老本身,将不再是“打地鼠”式的对症治疗,而是基于系统性理解的精准调控。两大技术趋势正在引领这场变革。
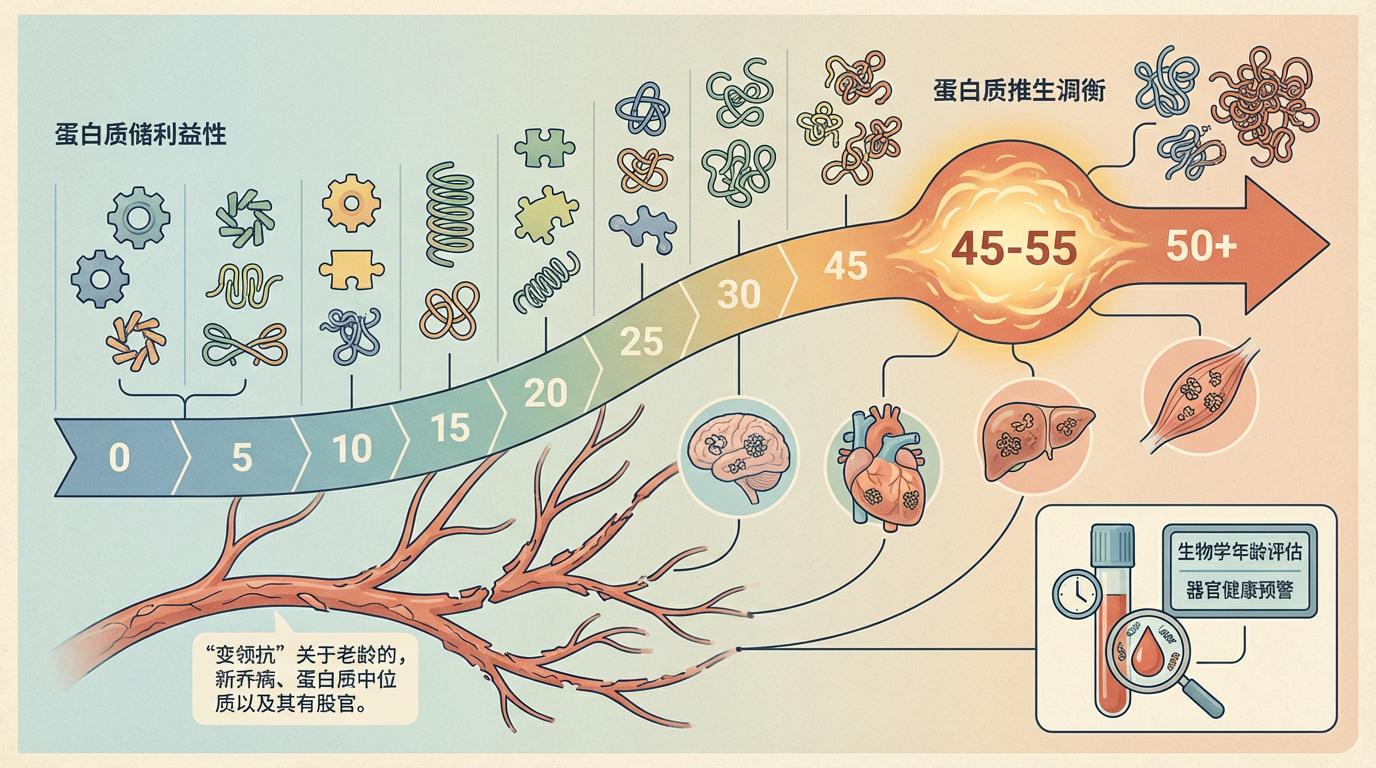
首先是蛋白质组学的深度应用。以中国科学院刘光慧院士团队的研究为例,他们绘制了横跨人类50年生命周期的多组织蛋白质组衰老图谱。这项宏大的工程揭示,蛋白质稳态的失衡是一个系统性的衰老特征,而血管系统是衰老的“先锋”。他们甚至发现,45-55岁是多器官蛋白质组经历剧烈重塑的关键转折点。这意味着,我们未来或许可以通过简单的血液检测,利用“蛋白质组衰老时钟”来评估个体的生物学年龄和器官健康状况,并在纤维化等疾病发生前进行预警和干预。
其次是人工智能与大数据的融合。AI不仅能加速药物发现,还能整合影像学、基因组学和蛋白质组学数据,为每位患者构建个性化的疾病模型。AI辅助诊断系统(如FDA批准的Fibresolve)已经能够更精准地解读CT影像,实现早期诊断。未来,AI将帮助医生制定最优的联合用药方案,预测治疗反应,实现真正的“千人千面”的精准医疗。
从肺部这块生命织物的逐渐硬化,到一个蛋白质分子的错误折叠,科学为我们揭示了衰老与疾病之间深刻而精妙的联系。山东大学团队的发现,不仅为肺纤维化患者带来了新的曙光,更深刻地提醒我们:维持细胞内部的秩序与稳态,是抵御衰老侵蚀的核心。
这场对抗“硬化”的战争,本质上是与熵增和无序的抗争。幸运的是,随着我们对蛋白质稳态、细胞衰老机制的理解日益深入,以及AI、纳米技术等强大工具的加持,我们正获得前所未有的能力去修复细胞的“质控系统”,去干预衰老的“多米诺骨牌”。未来的医学,或许不再仅仅是治疗疾病,而是致力于让生命的织物,在时间的洪流中,更长久地保持其柔韧与活力。