对抗知识焦虑,从看懂这条开始
App 下载
心梗治疗新靶点:RNA修饰调控心肌细胞生死
RNA修饰|南京医科大学|心肌细胞|m6A甲基化|铁死亡|心脑血管疾病|分子细胞生物学|生命科学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
RNA修饰|南京医科大学|心肌细胞|m6A甲基化|铁死亡|心脑血管疾病|分子细胞生物学|生命科学|医学健康
当27岁的长期吸烟者突发心梗被送进急诊时,医生们清楚:这个年轻人的心脏里,正有无数心肌细胞在以一种诡异的方式死去——不是常见的凋亡,也不是坏死,而是铁死亡:一种依赖铁离子、由脂质过氧化物撑破细胞膜的新型细胞死亡。中国心梗患者正以每年超10%的速度年轻化,而我们对这种“新型杀手”的调控机制,直到最近才摸到门道。南京医科大学的研究团队,在小鼠心梗模型里揪出了一条操控心肌细胞生死的隐秘通路——RNA上的一个甲基化修饰,正在悄悄决定着心脏的命运。为什么这个微小的化学修饰,能成为心梗治疗的关键突破口?
你可以把RNA上的m6A修饰——也就是给RNA分子的特定腺苷碱基加个甲基基团——理解成给快递贴了个“加速销毁”的标签。这个标签的“贴标员”是一种叫METTL3的蛋白,它能精准找到目标RNA,给它打上标记,让细胞里的降解系统优先处理它。
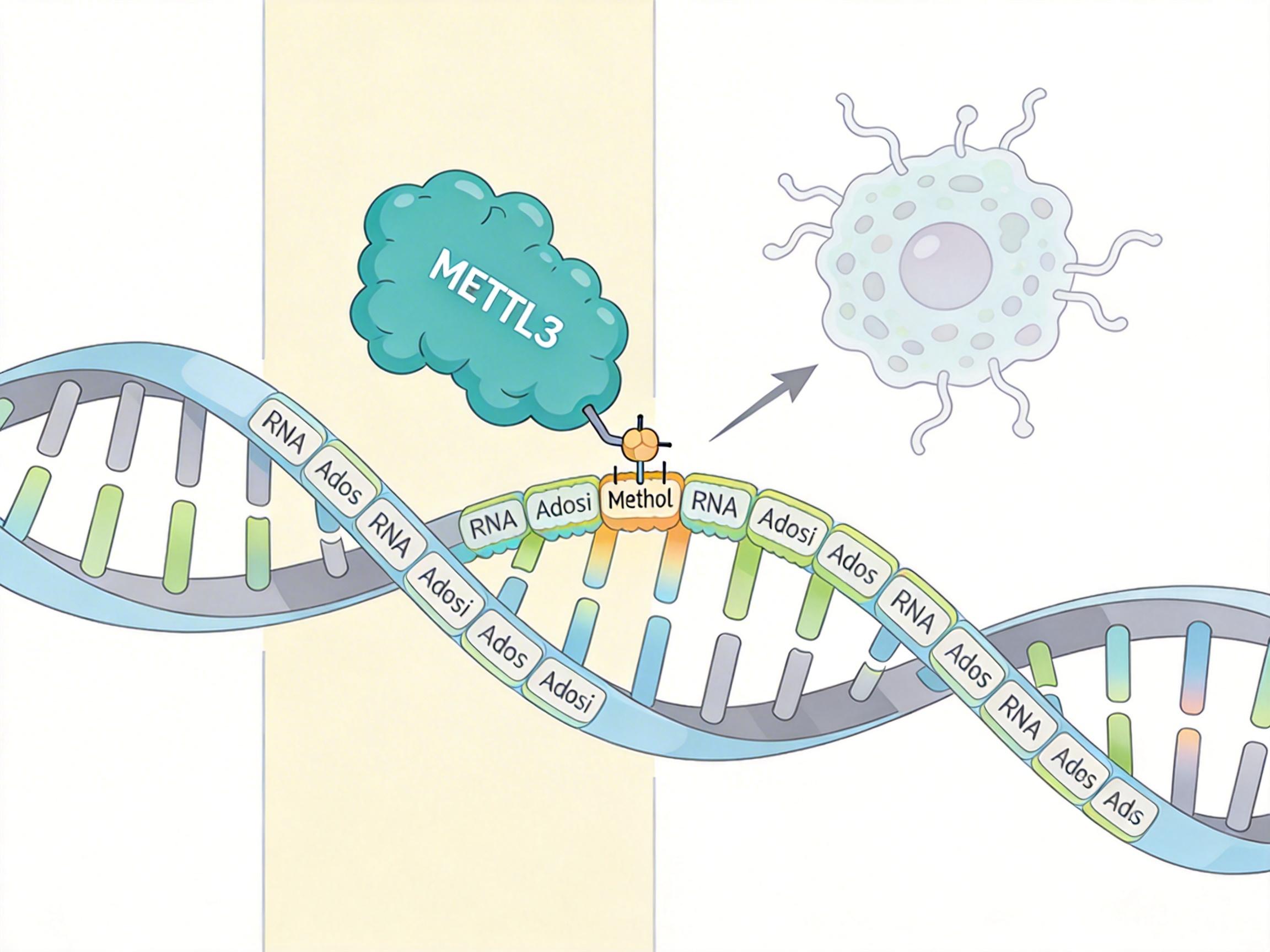
在心肌梗死的小鼠心脏里,研究人员发现METTL3的活性异常升高,它盯上了一个叫Dnajb1的基因。Dnajb1编码的DNAJB1蛋白,是心肌细胞里的“分子卫士”:它能紧紧拉住谷胱甘肽过氧化物酶4(GPX4)——这个蛋白是抑制铁死亡的核心防线,负责清除细胞里的脂质过氧化物。一旦DNAJB1减少,GPX4就会被自噬系统快速降解,细胞的抗氧化防线彻底崩溃,铁死亡随之爆发。
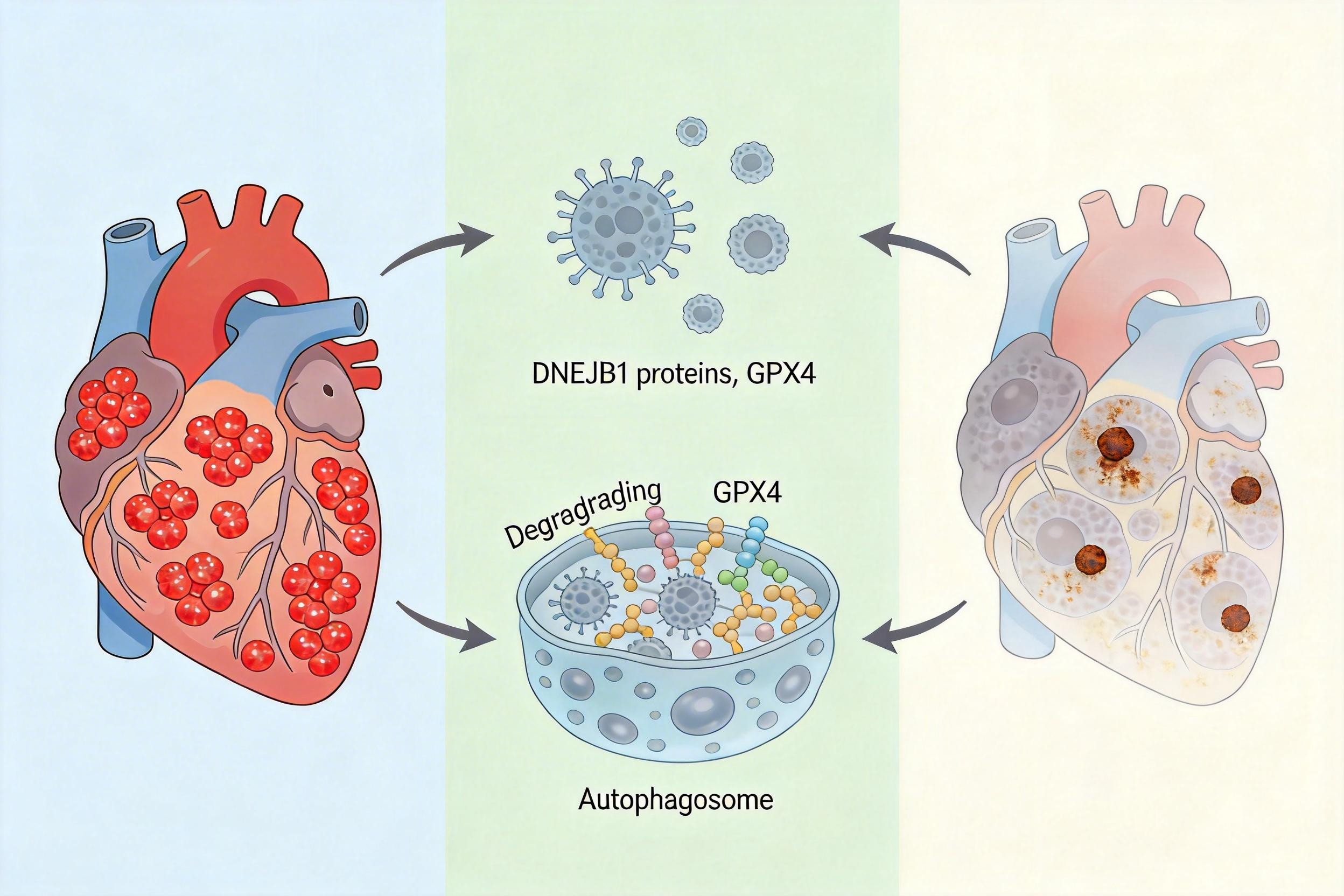
METTL3正是通过给Dnajb1的mRNA打上m6A标签,加速了它的降解,让DNAJB1的含量骤降。就像有人偷偷剪了消防水管,等火灾(心梗)发生时,连灭火的水(GPX4)都没了。
但细胞不会坐以待毙。研究人员发现,还有另一种叫IGF2BP3的蛋白,会和METTL3“抢生意”——它能竞争性地结合Dnajb1的mRNA,而且它的结合是给RNA贴“保护标签”,能延缓降解,让DNAJB1保持足够的产量。
这是一场动态的平衡:心梗发生时,METTL3活性飙升,试图压过IGF2BP3的保护作用;如果能激活IGF2BP3,或者抑制METTL3,就能让Dnajb1的mRNA稳定下来,DNAJB1含量回升,重新拉住GPX4,阻止铁死亡。
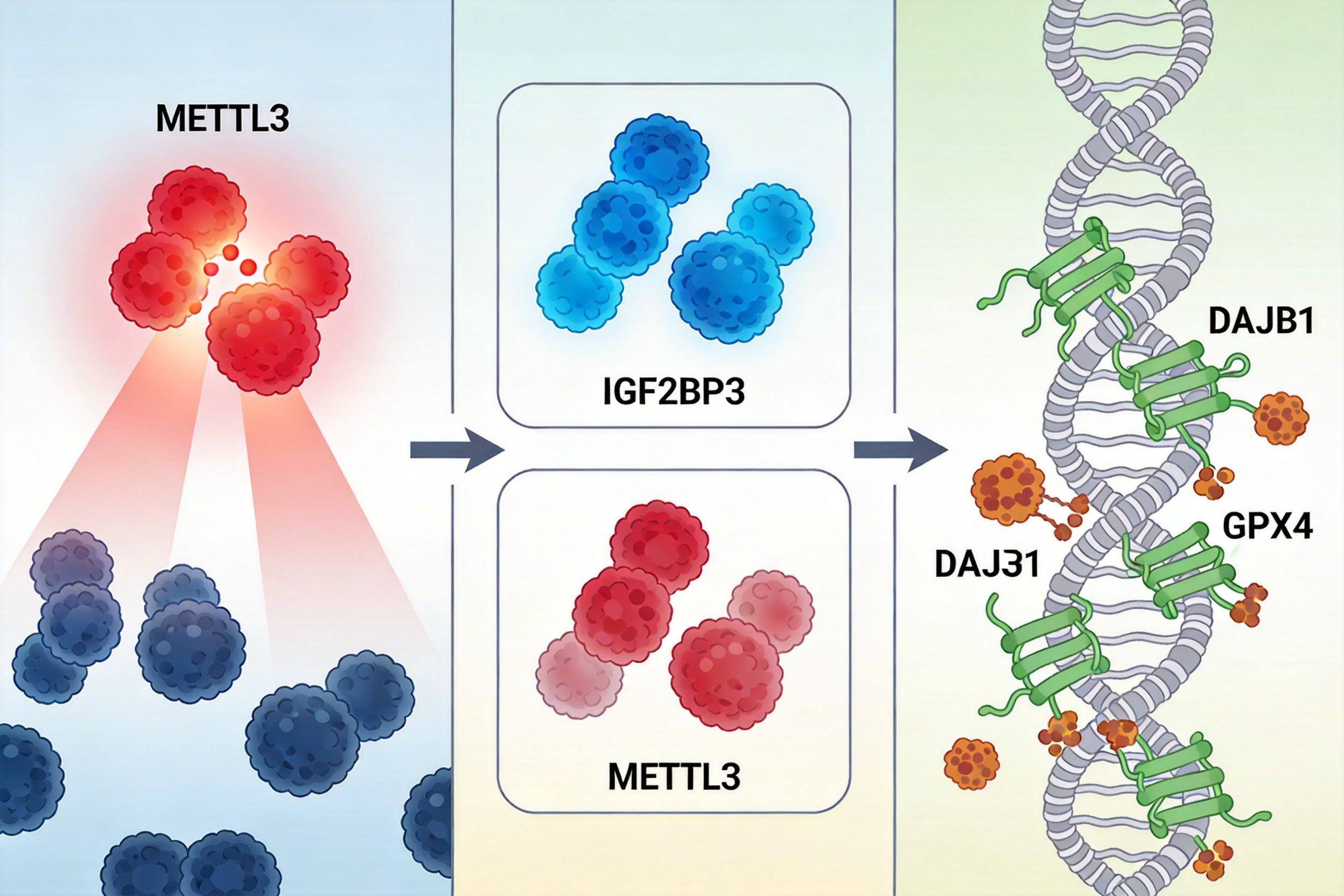
动物实验的数据直白得惊人:给心梗小鼠过表达DNAJB1,心梗面积缩小了近30%,心功能指标提升了40%;但如果同时过表达METTL3,这些保护效果会被完全抵消——就像刚补好的水管又被剪碎了。
更关键的是,研究团队找到了现成的METTL3抑制剂STM2457。在小鼠模型里,这种药物能显著降低心肌细胞的铁负荷和脂质过氧化水平,甚至能逆转部分已经发生的纤维化。
我认为,这项研究最被忽视的价值,在于它把“表观转录组调控”这个抽象概念,和心梗治疗这个临床刚需紧紧绑在了一起。过去我们总盯着基因的“开关”(DNA甲基化、组蛋白修饰),却忘了RNA才是基因到蛋白的“中间执行人”——给RNA贴个标签,就能直接调控蛋白产量,这比编辑基因要灵活得多,也安全得多。
当然,从实验室到临床还有几道坎要跨:比如METTL3抑制剂在人体的安全性,毕竟METTL3在全身细胞都有表达,精准抑制心脏里的METTL3而不影响其他器官,是个不小的挑战;再比如,人类心梗患者的心肌组织里,METTL3和Dnajb1的调控关系,是否和小鼠完全一致,还需要大样本的临床验证。
但至少我们找到了一个明确的方向:不用再盲目地“抢救”心肌细胞,而是可以通过调控RNA修饰,给心肌细胞的“自我保护系统”充能——这比直接给心脏“补细胞”要现实得多。
当我们把目光从宏大的“心脏修复”,聚焦到RNA分子上那一个小小的甲基基团时,才发现生命的调控机制,精细得像一台精密的钟表。每一个标签的贴与撕,每一次蛋白的结合与解离,都在决定着细胞的生死,最终影响着一个人的健康与生命。
“RNA修饰,是细胞生死的隐形开关。”这句话或许能概括这项研究的核心意义:我们终于在心肌细胞的死亡迷宫里,找到了一盏能操控方向的灯。未来的心梗治疗,或许不用再等细胞坏死之后再“亡羊补牢”,而是可以提前给RNA贴好“保护标签”,让心肌细胞自己守住防线。