
3 个月前

3 个月前
“人到中年,连喝水都长胖。”这句无奈的调侃,精准地捕捉了无数人跨过35岁门槛后的集体焦虑。年轻时,胡吃海喝后的体重增长似乎总能通过几周的节食和运动轻松抹去;而立之年后,即便严格自律,腰围却依然像一匹脱缰的野马,不受控制地向外扩张。一项覆盖超过800万日本成年人的大规模研究证实了这一普遍感受:从35岁开始,无论男女,身体质量指数(BMI)都呈现出不可逆转的上升趋势。
长久以来,我们习惯将这一切归咎于一个看似无法抗拒的自然法则——新陈代谢变慢。这个解释简单、直观,足以安慰我们在健身房挥汗如雨却收效甚微的挫败感。然而,科学的指针正悄然转向一个全新的方向。2021年发表于《科学》的一项里程碑式研究颠覆了这一传统认知,通过对覆盖29个国家、超过6000人的数据分析发现,人类在20岁到60岁之间的代谢率其实保持着惊人的稳定。这意味着,困扰一代人的中年发福,其背后真正的“黑手”并非代谢,而是我们体内一场更为隐秘的细胞风暴。
真正的突破来自美国希望之城医学中心(City of Hope)的王琼团队与加州大学洛杉矶分校(UCLA)杨霞团队的合作研究。他们在《科学》杂志上发表的论文,首次从细胞层面揭开了中年发福的神秘面纱。研究指出,问题的核心不在于能量消耗的减少,而在于脂肪组织的生成方式发生了根本性改变。
传统观念认为,成年后我们体内的脂肪细胞数量基本恒定,长胖只是单个脂肪细胞被撑得更大。但这项研究通过精密的动物实验发现,中年小鼠的内脏脂肪扩张,超过80%的脂肪细胞竟然是新生成的!这彻底颠覆了以往的认知。身体并非在为现有的“仓库”添货,而是在疯狂地“新建仓库”。
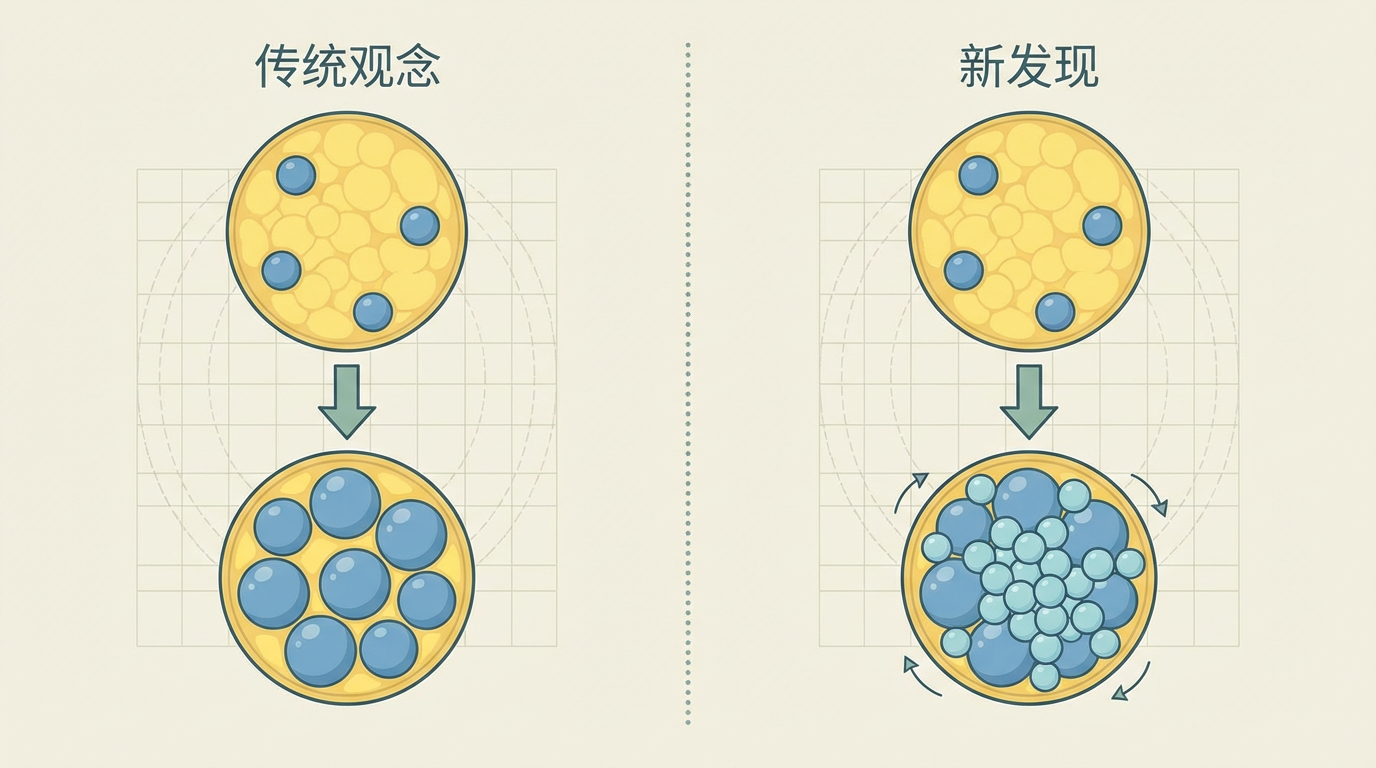
是什么在驱动这场疯狂的“基建”?科学家们锁定了一群特殊的细胞——脂肪前体细胞类群(CP-A)。这些细胞如同沉睡的建筑队,在生命的前半段几乎处于休眠状态。然而,一旦进入中年,它们仿佛接到了某种神秘指令,被集体“唤醒”,以惊人的速度增殖并分化成新的脂肪细胞,尤其偏爱在腹部内脏周围“安营扎寨”。
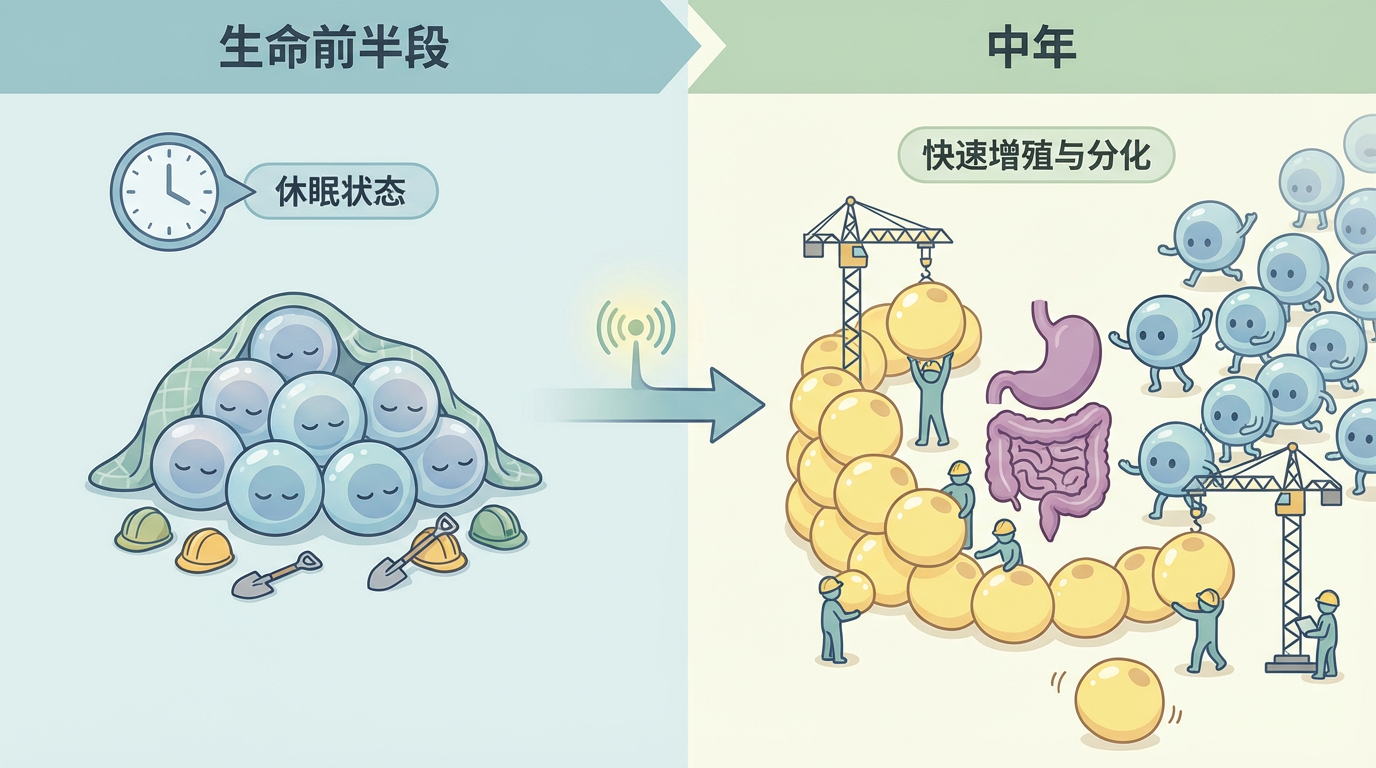
CP-A细胞的发现,如同一束光照进了中年肥胖的黑箱。它们是一种中年特异性的脂肪前体细胞,具有超乎寻常的增殖和成脂能力。在小鼠实验中,研究人员观察到,CP-A细胞在小鼠9个月大(相当于人类中年)时开始涌现,12个月大时达到峰值,其出现的时间线与体重增长的轨迹完美吻合。
更具说服力的证据来自移植实验:当科学家将中年小鼠的CP-A细胞移植到年轻小鼠体内时,这些年轻的宿主也迅速出现了内脏脂肪堆积的“发福”迹象。这无可辩驳地证明,CP-A细胞本身就是驱动脂肪生成的独立引擎,其强大的能力不受宿主年龄环境的影响。
那么,是什么按下了CP-A细胞的“启动键”?研究团队进一步发现了一条名为**白血病抑制因子受体(LIFR)的信号通路**。LIFR就像是CP-A细胞专属的“加速按钮”。在中年时期,这条通路被激活,向CP-A细胞发出指令,驱动它们疯狂制造脂肪。有趣的是,年轻的脂肪细胞生成并不依赖这条通路。这意味着,LIFR信号通路是中年发福的一个特异性开关,为未来的精准干预提供了可能。
这项研究还解开了一个长期困扰人们的谜题:为什么中年男性更容易出现标志性的“啤酒肚”?实验数据显示,CP-A细胞的活跃以及由其驱动的脂肪生成,主要发生在雄性小鼠的内脏脂肪组织中,而雌性小鼠的体重增长则相对平缓。研究人员在人类成年男性的内脏脂肪样本中也发现了类似的CP-A细胞群,其数量随年龄增长而增加。
这一发现具有深远的现实意义。它表明,中年男性的腹部肥胖并非简单的生活习惯问题,而是有着深刻的、由性别决定的生物学根源。内脏脂肪的过度堆积,远不止是美观问题,它与胰岛素抵抗、2型糖尿病、心血管疾病等一系列代谢紊乱密切相关。因此,理解CP-A细胞的性别特异性,对于制定针对性的健康策略至关重要。
CP-A细胞和LIFR信号通路的发现,为对抗中年发福打开了一扇全新的大门。它标志着体重管理的科学路径正在从宏观的“热量平衡”转向微观的“细胞调控”。
未来的可能性令人振奋:
最终,这项科学突破让我们得以用一种全新的、更富有同理心的视角来看待中年发福。它不再仅仅是个人意志力的失败,也不是一句简单的“新陈代谢慢了”就能概括。它是一场在我们体内悄然发生的、由特定基因和细胞程序驱动的生物学事件。
理解这一点,并非为放弃努力寻找借口,而是为更智慧的战斗指明了方向。我们对抗的不再是模糊的“岁月”,而是具体的细胞、特定的信号通路。科学正以前所未有的清晰度,为我们绘制出这场战争的地图。虽然精准的“细胞武器”仍在研发之中,但这张地图已经告诉我们,通过科学的生活方式管理,结合未来的医学干预,我们完全有希望打破“年龄-体重”的恶性循环,赢得这场关乎健康与活力的中年保卫战。
点击充电,成为大圆镜下一个视频选题!