对抗知识焦虑,从看懂这条开始
App 下载
乳腺癌淋巴转移真相:癌细胞和免疫细胞在共谋
空间转录组学|单细胞RNA测序|免疫细胞|淋巴结转移|乳腺癌|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
空间转录组学|单细胞RNA测序|免疫细胞|淋巴结转移|乳腺癌|肿瘤学|医学健康
全球每4个女性癌症患者里,就有1个是乳腺癌——而90%的乳腺癌死亡,都不是因为最初那个乳房里的肿瘤,而是它偷偷溜去身体其他部位的「分身」。淋巴结就是这些分身最常潜伏的「中转站」,一旦癌细胞在这里站稳脚跟,患者的生存几率会直接腰斩。但几十年来,科学家始终没搞懂:明明淋巴结本该是免疫细胞的「哨所」,怎么就成了癌细胞的「避难所」?南京师范大学的研究团队,用36万个细胞的「高清档案」,第一次拆穿了这场发生在我们身体里的「共谋」。
研究人员给78位乳腺癌患者的原发肿瘤和转移淋巴结做了「细胞CT」——单细胞RNA测序加空间转录组学,前者能看清每个细胞的「工作状态」,后者能定位这些细胞在组织里的「具体位置」,相当于把转移现场的每一个参与者、每一次对话都录了下来。
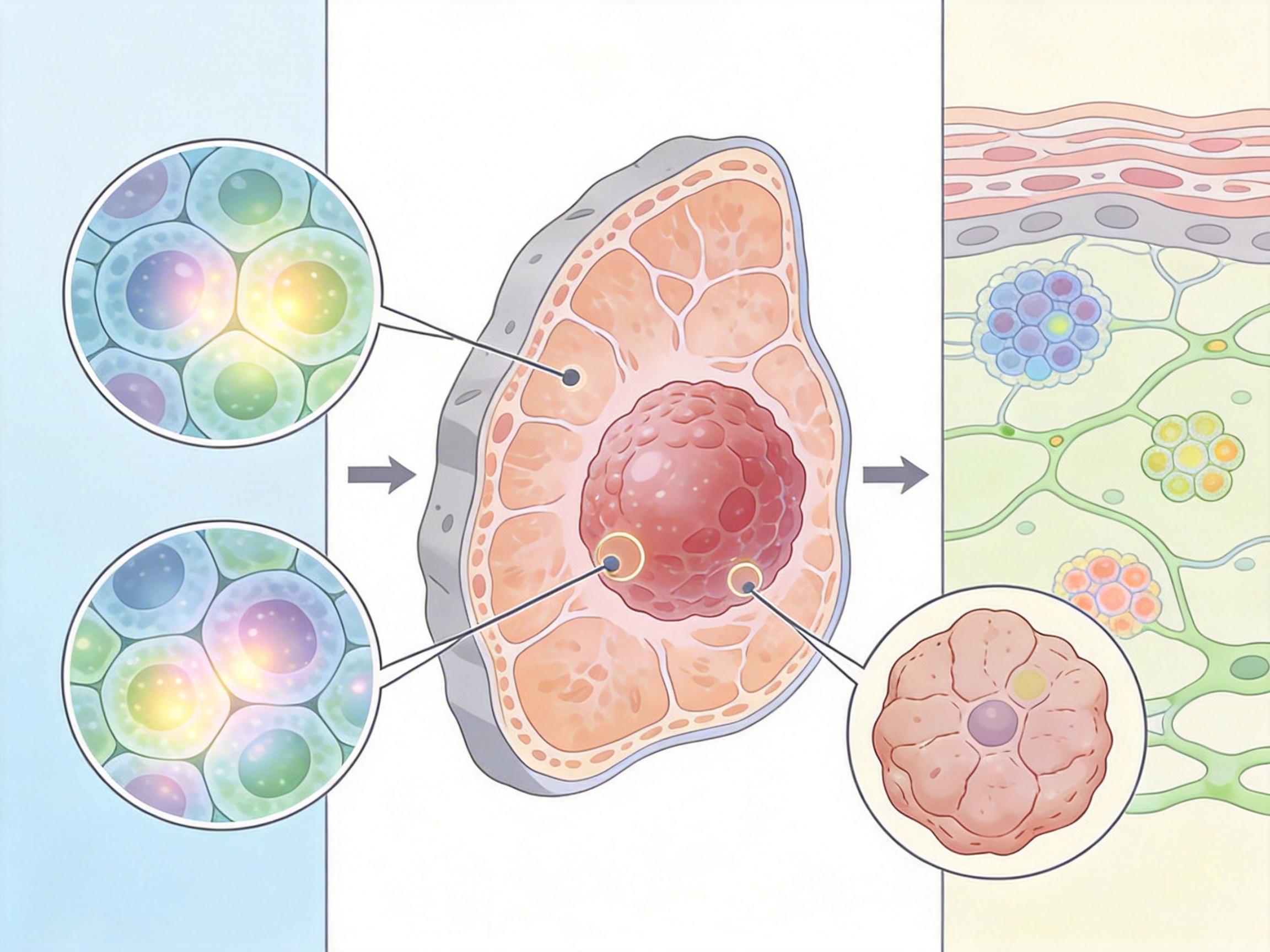
在36万个细胞的「众生相」里,他们先锁定了一群「早期播散癌细胞」。这群细胞不像其他癌细胞那样等肿瘤长大再跑路,而是早早从原发肿瘤里「溜号」,躲进淋巴结里潜伏。更可怕的是,它们不是孤军奋战:一边给自己换了套「代谢系统」——把主要能量来源从糖酵解切换到氧化磷酸化,就像把烧煤的发动机换成了烧天然气的,在淋巴结缺氧缺营养的环境里也能维持运转;一边还在给免疫细胞「发暗号」。
你可以把这个过程想象成:小偷提前踩点找到空房子,先给房子换了个省电的空调保证自己不被热死,然后联系了小区里的保安,让对方别查自己的身份证。
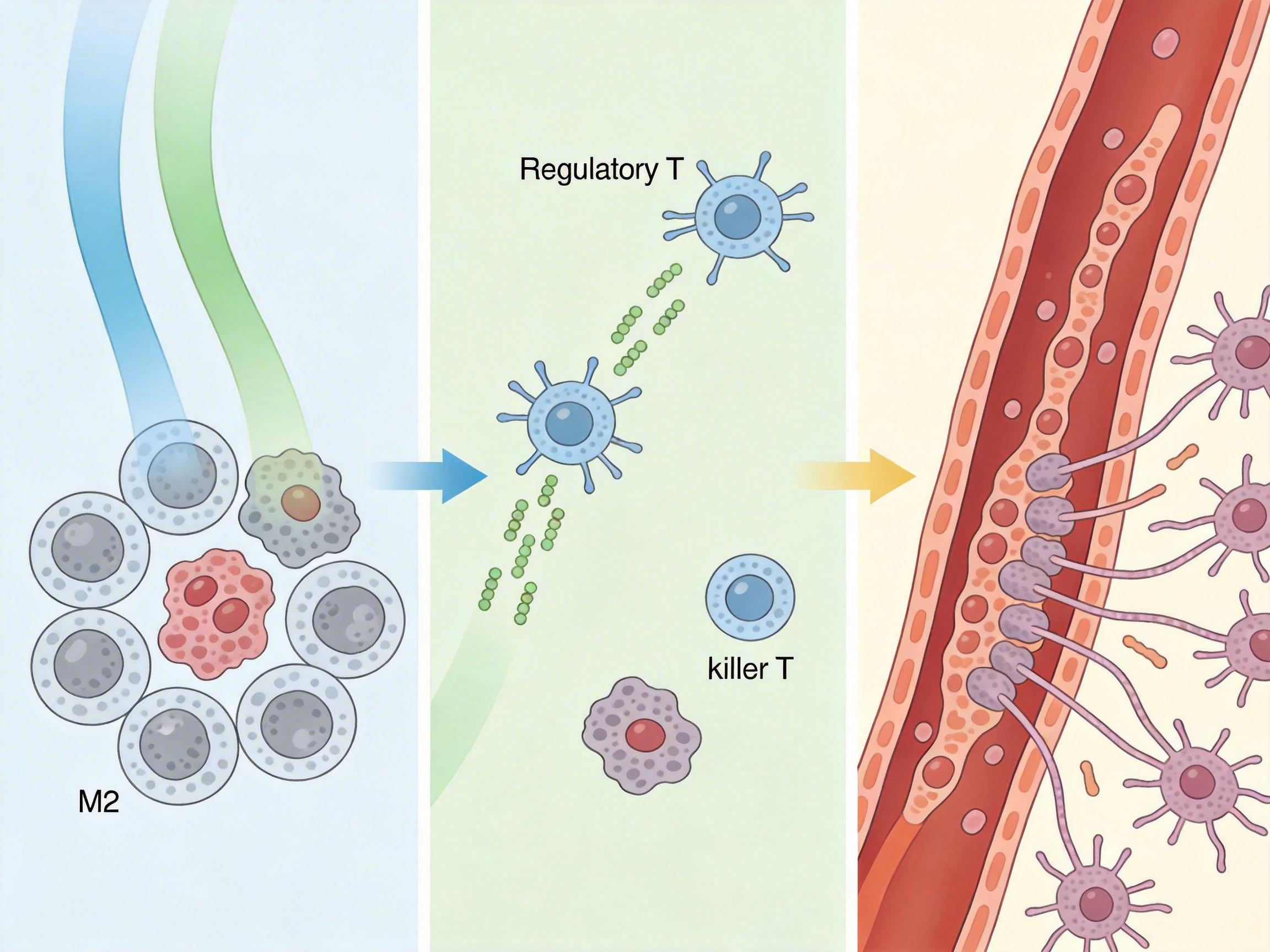
如果说早期播散癌细胞是「主犯」,那M2型巨噬细胞就是最关键的「帮凶」。这种细胞本来是免疫系统的「清洁工」,负责清理体内的垃圾和异物,但在淋巴结里,它被癌细胞策反了。
研究人员通过空间转录组学看到,M2型巨噬细胞紧紧贴在癌细胞周围,一边分泌CCL22和CXCL12这两种信号分子——前者专门招募免疫抑制性的调节性T细胞,后者直接抑制杀伤性T细胞的活性,相当于把淋巴结里的「警察」都调走、把「武器」都没收了;一边还在给癌细胞「打鸡血」,让它们变得更具侵袭性,甚至能诱导癌细胞的上皮-间质转化,让它们更容易钻进血管跑到其他器官。
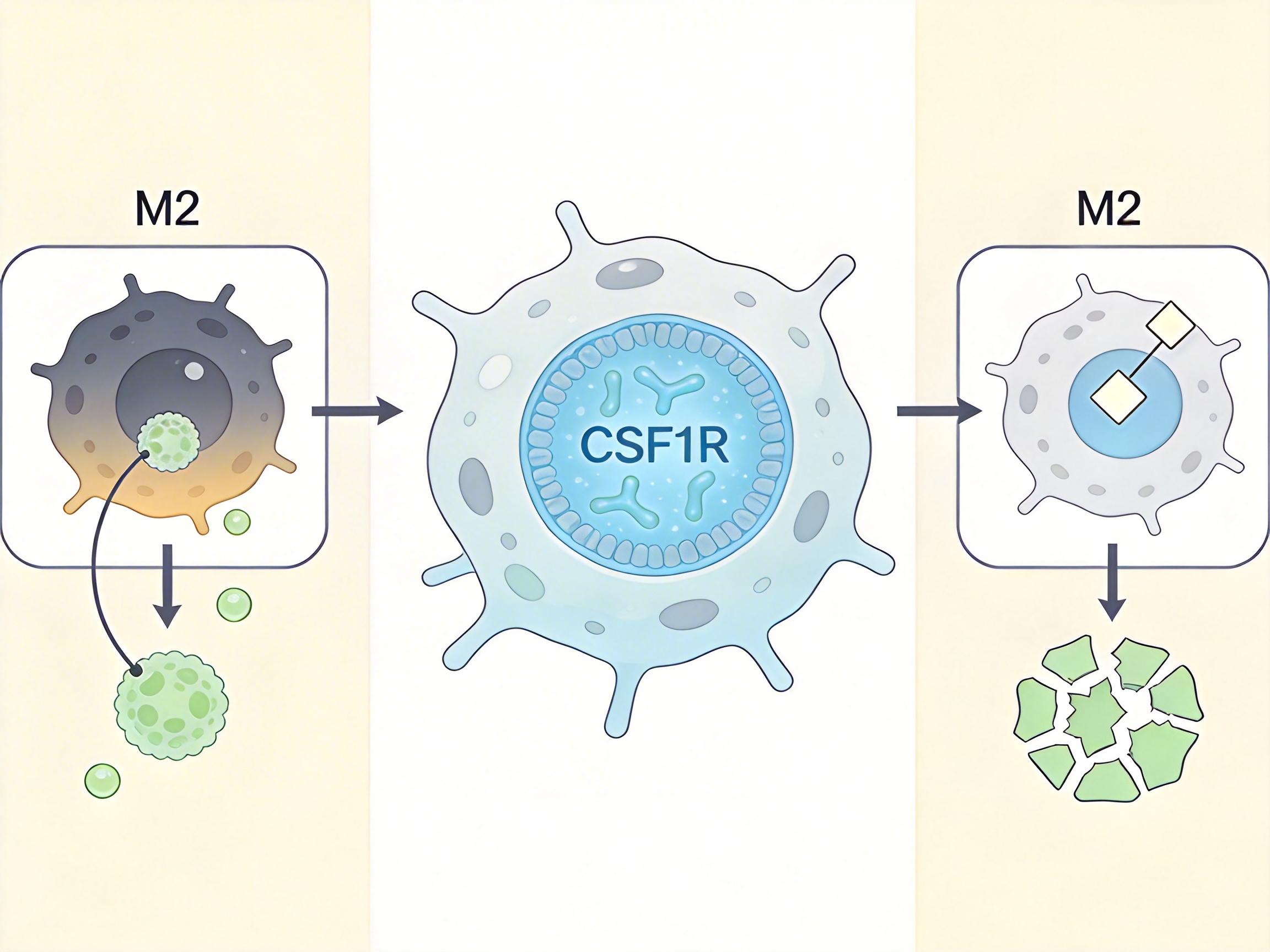
更精准地说,M2型巨噬细胞是通过CSF1R这个「信号开关」接收癌细胞指令的。当癌细胞释放出对应的信号分子,CSF1R就会被激活,巨噬细胞就从「清洁工」变成了「帮凶」。而研究人员发现,已经用于其他癌症治疗的培西达替尼和舒尼替尼,恰好能关掉这个开关——阻断CSF1R的信号,就能让巨噬细胞恢复「清洁工」的本职,同时打破癌细胞的免疫抑制屏障。
到这里,乳腺癌淋巴转移的三重机制终于清晰了:癌细胞负责「跑路」和「伪装」,代谢重编程负责「续命」,免疫细胞负责「掩护」——三者形成了一个闭环,让癌细胞在淋巴结里从潜伏到壮大,再到向全身扩散。
我认为,这项研究最有价值的地方,不是找到了一两个治疗靶点,而是第一次用「全景视角」展现了癌症转移的复杂性。过去我们总把癌症当成单一的「敌人」,要么想办法杀死癌细胞,要么想办法激活免疫系统,但这次的研究告诉我们:癌症是一个「生态系统」,癌细胞、代谢环境和免疫细胞之间的相互作用,才是转移的核心。
比如,早期播散癌细胞的代谢重编程,不仅是为了自己生存,还会改变周围的微环境——释放的乳酸会进一步抑制免疫细胞的活性;而M2型巨噬细胞分泌的信号分子,又会反过来促进癌细胞的代谢重编程。这种「相互喂养」的关系,才是转移最难被打破的地方。
现在,我们终于有了一张清晰的「转移地图」,知道该去哪里切断癌细胞的「补给线」,该怎么唤醒被策反的免疫细胞。培西达替尼和舒尼替尼的新用途,只是第一步——未来我们或许能找到更精准的方法,直接针对早期播散癌细胞的代谢弱点,或者阻断癌细胞和巨噬细胞之间的「暗号」。
癌症之所以可怕,从来不是因为它有多强,而是因为它太懂得「借势」——借身体的营养,借免疫的漏洞,借我们对它的无知。而这次的研究,就是把它的「借势」逻辑摊开在阳光下。
看清共谋,才能打破共谋。