对抗知识焦虑,从看懂这条开始
App 下载
肝癌偷能量的秘密被找到,老药能治新病
脂质合成|HIV老药|ADSL-INSIG通路|有氧糖酵解|肝癌|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
脂质合成|HIV老药|ADSL-INSIG通路|有氧糖酵解|肝癌|肿瘤学|医学健康
你可能听说过癌细胞靠“有氧糖酵解”疯狂抢葡萄糖——就像一个永远吃不饱的饕餮,哪怕氧气充足,也偏要走低效但快速的代谢路径。但很少有人知道,这些抢来的葡萄糖,除了供能,还被癌细胞偷偷“变”成了建造自己的“建材”——脂质。浙江大学等团队的最新研究,终于揪出了癌细胞完成这一“偷梁换柱”的核心链条,更让人意外的是,一款已用了多年的HIV老药,居然能打断这个链条。
过去我们只知道,癌细胞的葡萄糖代谢和脂质合成都很活跃,但一直没搞懂两者是怎么联动的——就像看到两个忙碌的车间,却找不到连接它们的传送带。
这次的研究终于找到了这条传送带:ADSL-INSIG-SREBP轴。你可以把它想象成癌细胞内部的一条“物流专线”:
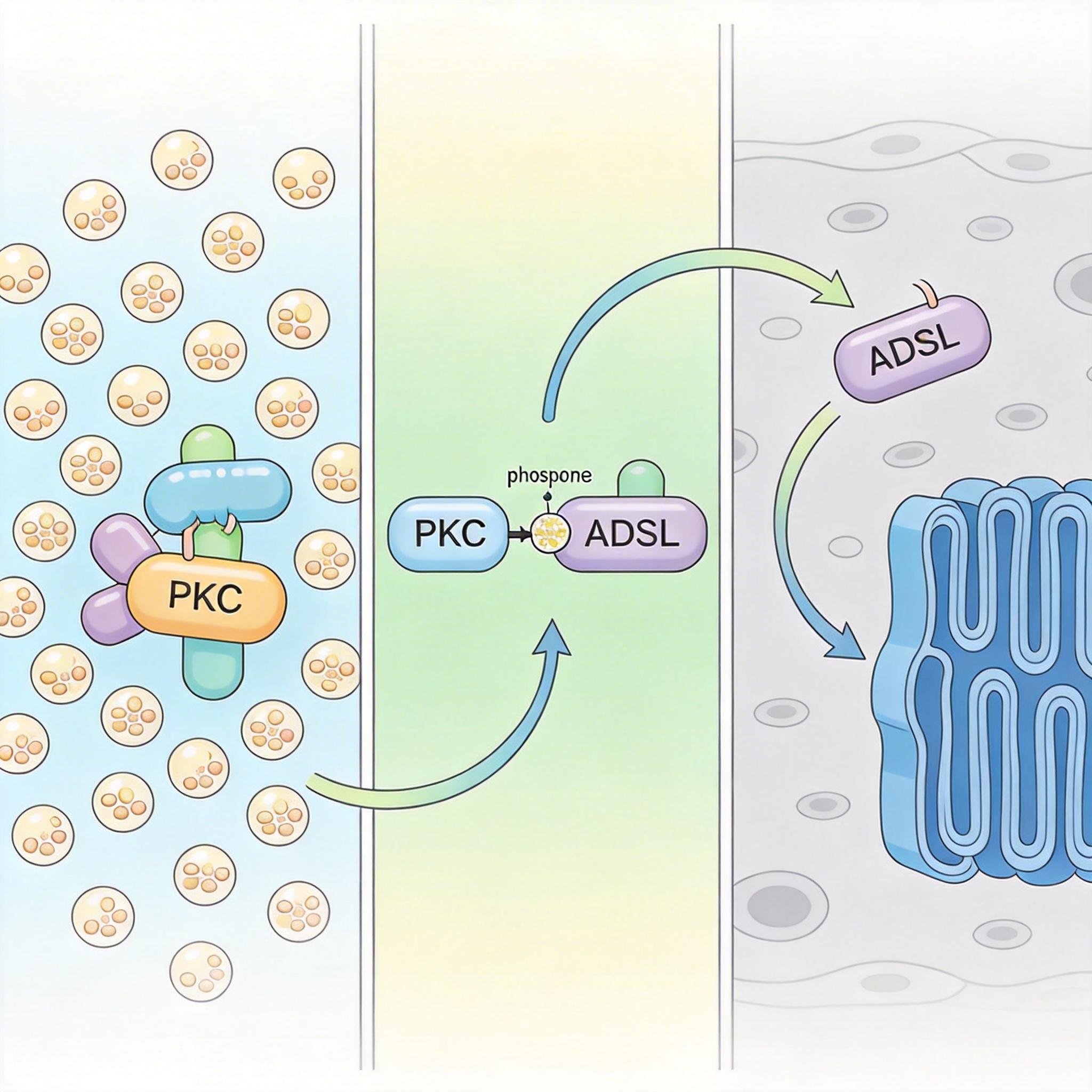
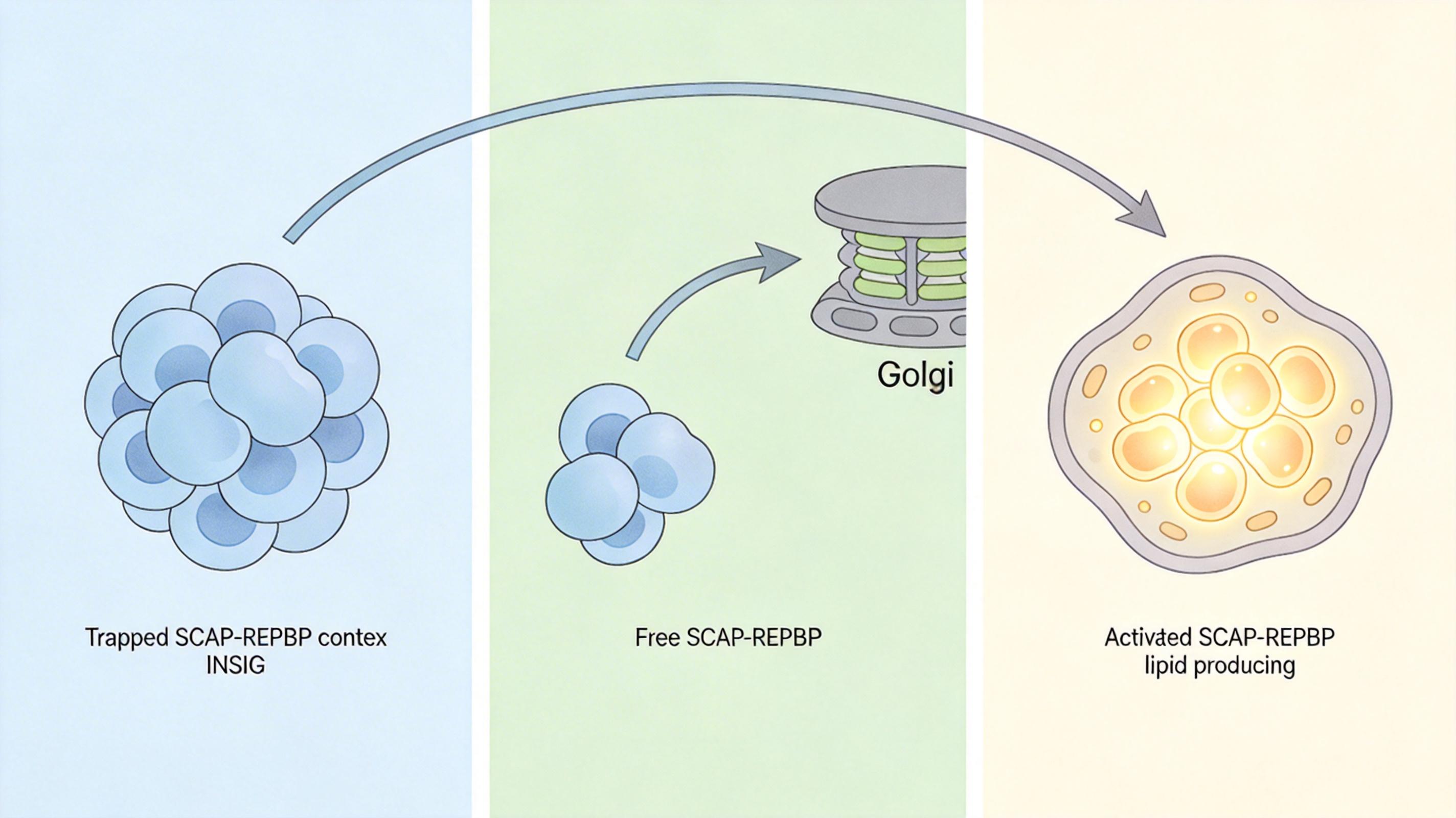
简单说,这条通路让癌细胞能把抢来的葡萄糖,直接转化为构建细胞膜、支持增殖的脂质,实现了“能量-建材”的一站式供应。
研究团队通过虚拟筛选发现,一款已获批的HIV药物艾舒法韦林,能精准阻断ADSL和INSIG的结合——就像给那条“物流专线”设了路障,让葡萄糖无法转化为脂质。
更关键的是,艾舒法韦林和肝癌一线药物仑伐替尼联用,能产生协同效应:单独用仑伐替尼,癌细胞可能还能通过其他途径凑够脂质;但加上艾舒法韦林,就彻底掐断了脂质的主要来源,肿瘤生长被显著抑制。
临床数据也给了这个策略信心:肝癌患者体内,ADSL的磷酸化水平、INSIG的琥珀酰化程度,和SREBP-1的激活程度以及不良预后正相关——也就是说,这条通路越活跃,患者的病情越严重,这也反向证明了靶向这条通路的价值。
当然,这个策略也有局限:艾舒法韦林原本是治HIV的,用于肝癌的最佳剂量、长期安全性,还需要更多临床试验验证;而且不是所有肝癌患者都适合,得先检测体内相关分子的水平才能确定。
其实不止肝癌,几乎所有肿瘤都在玩“代谢重编程”的把戏——就像游戏里的作弊码,能让癌细胞突破正常细胞的代谢限制,疯狂增殖。
SREBP作为调控脂质合成的核心转录因子,在多种肿瘤中都处于激活状态:乳腺癌细胞靠它合成的脂质构建侵袭性的细胞膜,前列腺癌细胞靠它储存能量应对微环境的营养匮乏。而这次发现的ADSL-INSIG-SREBP轴,可能是肿瘤代谢重编程的一个“通用节点”——这意味着,艾舒法韦林的抗癌潜力,或许不止于肝癌。
不过,肿瘤的代谢网络就像一张复杂的蜘蛛网,掐断一条线,它可能会从另一条线绕过去。比如有些癌细胞在脂质合成被阻断后,会转而增强脂肪酸的摄取,或者激活其他代谢通路。这也是为什么联合治疗如此重要——要同时掐断多条“补给线”,才能让癌细胞无路可逃。
从发现癌细胞的代谢异常,到找到具体的调控通路,再到老药新用的尝试,人类对抗肿瘤的每一步,都是在破解它的“生存密码”。
这次的研究最动人的地方,不在于发现了一个新的靶点,而在于它让我们看到:那些已经在临床使用多年的老药,可能还藏着我们没发现的潜力——就像一把旧钥匙,居然能打开新的锁。
代谢重编程的战场,从来都是藏在分子里的博弈。 未来,或许会有更多老药被重新发掘,成为对抗肿瘤的新武器,而我们对肿瘤代谢的每一点理解,都在把胜利的天平向人类这边倾斜。