对抗知识焦虑,从看懂这条开始
App 下载
CAR-T攻克实体瘤,这次瞄准了肿瘤的"朋友圈"
肿瘤微环境|卵巢癌|纪念斯隆凯特琳癌症中心|uPAR靶点|CAR-T疗法|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
肿瘤微环境|卵巢癌|纪念斯隆凯特琳癌症中心|uPAR靶点|CAR-T疗法|肿瘤学|医学健康
当一位晚期卵巢癌患者躺在手术台上,医生能做的往往只是切除可见的肿瘤——那些藏在腹腔、肝脏甚至肺里的微小转移灶,就像撒在土壤里的种子,迟早会重新发芽。这正是实体瘤的残酷之处:它们不仅有顽强的癌细胞本体,还拉上了成纤维细胞、免疫抑制细胞组成"保护朋友圈",把免疫疗法挡在门外。但最近,纪念斯隆凯特琳癌症中心的研究团队,给CAR-T装上了一个新导航,让它既能精准追杀癌细胞,还能端掉肿瘤的"朋友圈"——在小鼠模型里,这个疗法甚至彻底清除了全身的转移灶。
你可以把肿瘤想象成一个伪装成伤口的"非法工地"——正常伤口愈合时,人体会调动细胞修复组织,而肿瘤却劫持了这套程序,让周围的细胞都变成它的帮凶。uPAR,也就是尿激酶纤溶酶原激活物受体,就是这个非法工地的"通用工牌"。
在健康人体里,uPAR只在少数免疫细胞上低调存在,负责伤口愈合的收尾工作。但到了肿瘤里,不管是最具侵袭性的癌细胞,还是帮忙搭建纤维化屏障的成纤维细胞,或是专门压制免疫细胞的髓系抑制细胞,都会齐刷刷地亮出uPAR这个工牌。研究团队分析了1万多份肿瘤样本后发现,12种癌症里都有uPAR的身影,尤其是肺癌、胰腺癌、卵巢癌这些难治性实体瘤,uPAR几乎成了标配。
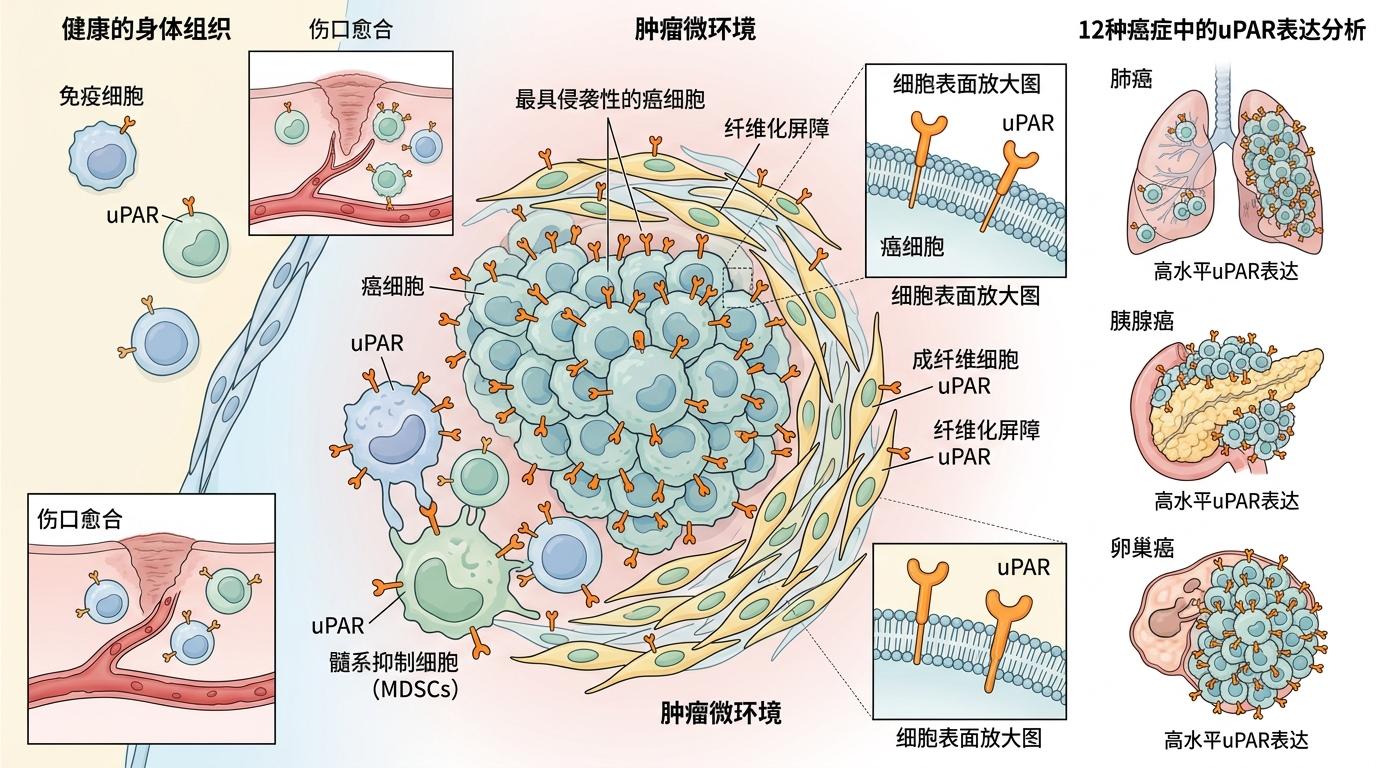
更关键的是,uPAR不是某一类细胞的专属标记,而是肿瘤"恶性状态"的标志——只要细胞在为肿瘤干活,不管是癌细胞还是帮凶,都会带上这个标记。这就给了CAR-T一个精准打击整个肿瘤生态系统的机会,而不是像以前那样,只能盯着单一类型的癌细胞打。
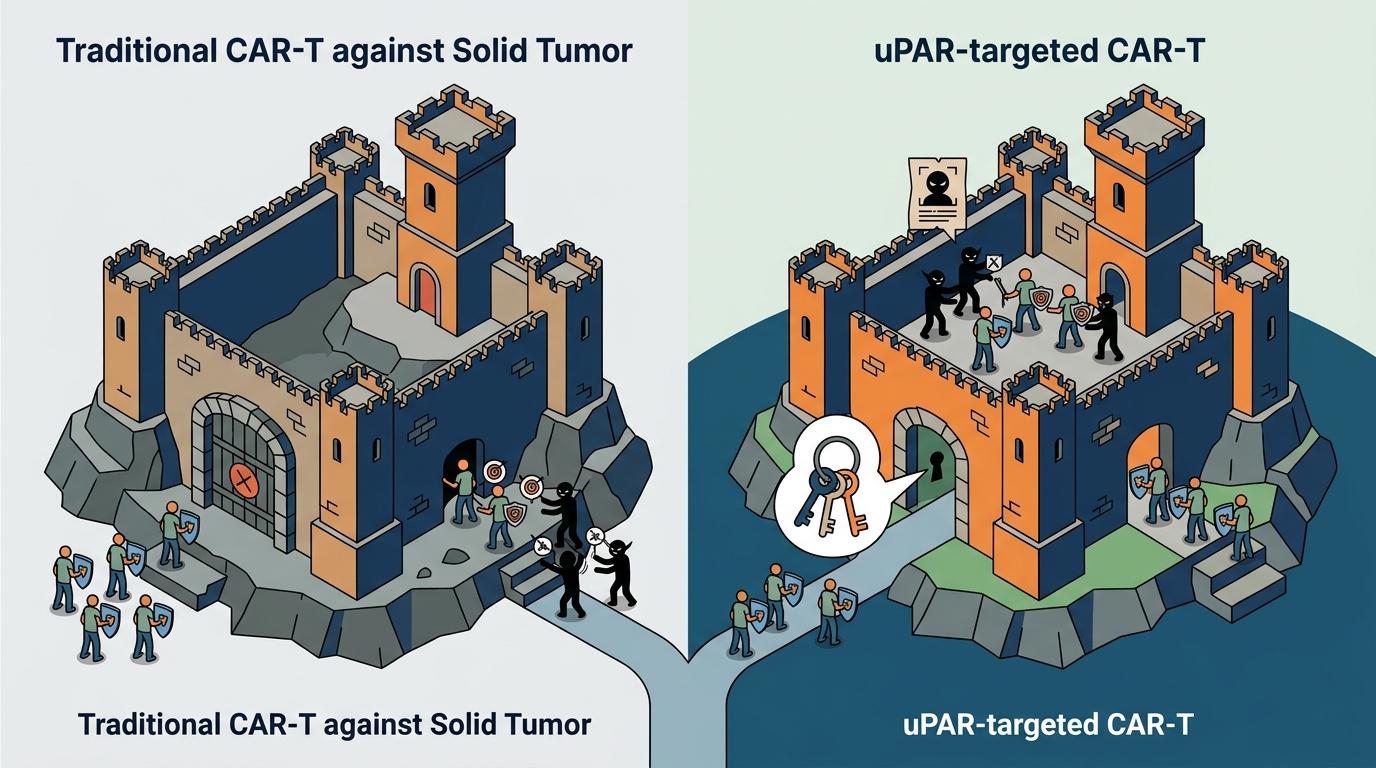
传统CAR-T对付实体瘤的困境,就像一群士兵攻打被高墙和雇佣兵包围的城堡——要么找不到城堡的入口,要么进去了也被雇佣兵缴械。而靶向uPAR的CAR-T,相当于同时拿到了城门钥匙和雇佣兵的通缉令。
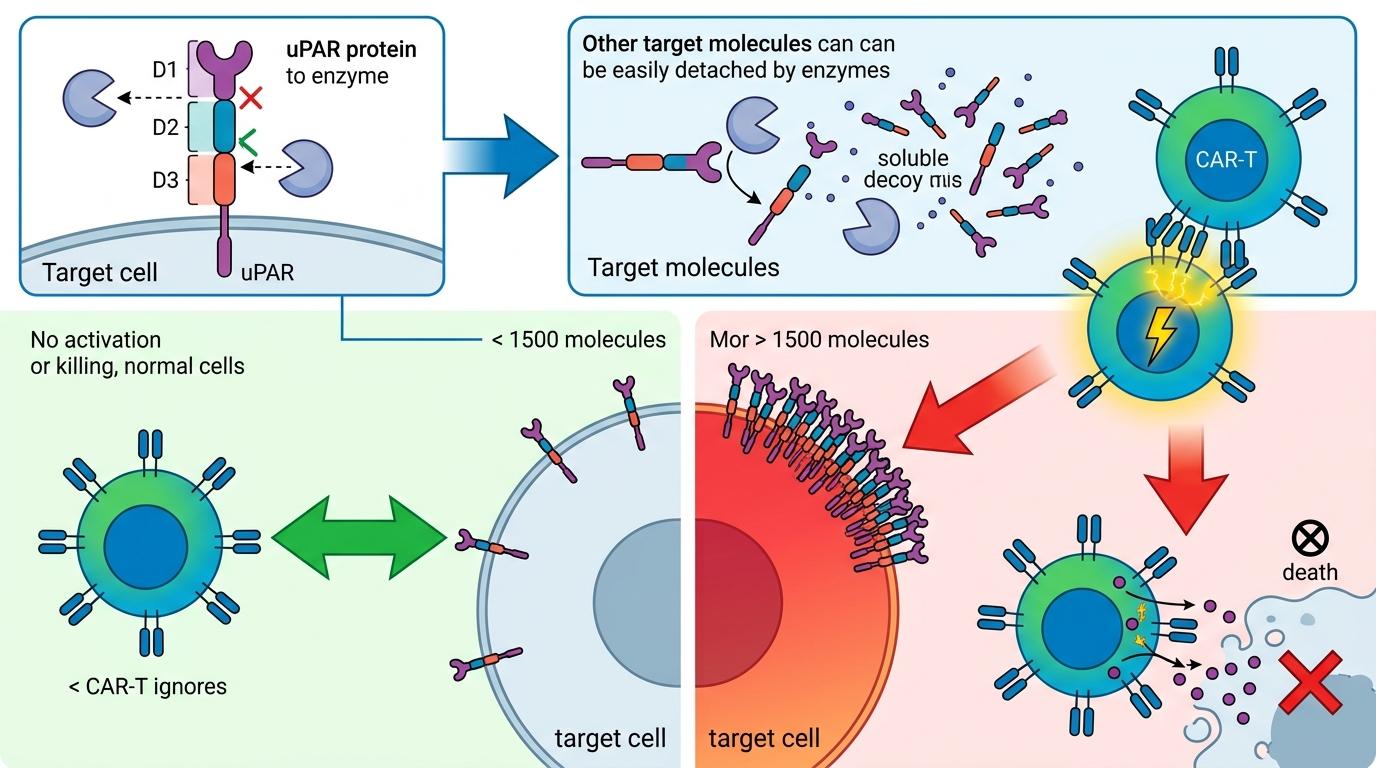
研究团队给CAR-T选了个聪明的瞄准点:uPAR的D2-D3结构域。这个区域很少会被蛋白酶切割脱落,不会像其他靶点那样,被血液里的可溶性蛋白干扰得"找不着北"。实验显示,只要靶细胞表面有1500个uPAR分子,CAR-T就能精准识别并发起攻击,而没有uPAR的正常细胞,完全不会被误伤。
在卵巢癌小鼠模型里,这个疗法展现出了惊人的效果:手术切除原发肿瘤后,一次低剂量的uPAR CAR-T输注,就彻底清除了全身的微小转移灶,小鼠实现了超过150天的无瘤生存;而只接受手术的小鼠,很快就因肿瘤复发死亡。更让人惊喜的是,那些被治愈的小鼠,后来再接种癌细胞时,身体能快速发起免疫反应,直接把癌细胞扼杀在摇篮里——这意味着CAR-T在它们体内留下了长效的免疫记忆。
uPAR CAR-T的临床前数据足够亮眼,但要真正走进病房,还有几道坎要跨。
首先是安全性。虽然uPAR在正常组织里表达很低,但它毕竟在部分免疫细胞上存在。研究团队在人源化小鼠模型里验证了安全性:CAR-T在清除肿瘤的同时,没有造成持续的骨髓抑制,只是短暂影响了部分单核细胞,而这些细胞的前体细胞能快速补充,很快就能恢复正常。不过,人体的免疫系统比小鼠复杂得多,长期的安全性还需要临床试验来验证。
其次是肿瘤微环境的差异。小鼠模型里的肿瘤微环境,和人类晚期实体瘤里那种被严重纤维化、免疫抑制的环境相比,还是简单了不少。比如胰腺癌,它的肿瘤周围有厚厚的纤维化组织,就像穿了一层防弹衣,CAR-T能不能顺利穿透这层屏障,还是个未知数。
还有联合治疗的潜力。研究发现,顺铂这类化疗药物能诱导肿瘤细胞衰老,让它们表达更多的uPAR,这时候再用CAR-T,效果会更好。未来,把uPAR CAR-T和化疗、放疗甚至免疫检查点抑制剂结合起来,可能会给晚期实体瘤患者带来更多希望。
从只能对付血液肿瘤的"抗癌神药",到有望攻克实体瘤的广谱疗法,CAR-T的每一步突破,都在刷新人类对抗癌症的边界。uPAR CAR-T的意义,不仅在于找到了一个新靶点,更在于它提供了一种全新的思路:对付肿瘤,不能只盯着癌细胞,还要端掉它的"朋友圈"。
当然,现在还不是欢呼的时候。临床前的成功,距离真正造福患者还有一段路要走。但至少,我们已经在实体瘤这个坚不可摧的堡垒上,打开了一道裂缝。
瞄准肿瘤生态,而非单一细胞