内容由AI生成,思考得你完成
App 下载
内容由AI生成,思考得你完成
App 下载
在病毒的世界里,有一些名字仅凭耳闻便足以令人不寒而栗。马尔堡病毒(Marburg virus)正是其中之一。作为埃博拉病毒的“同门兄弟”,它同样能引发致死率高达**88%**的出血热,像一个无形的幽灵,在非洲大陆不时掀起致命的波澜。近年来,疫情频发的消息更让公共卫生界警铃大作。然而,与埃博拉病毒已拥有有效疫苗和抗体疗法形成鲜明对比的是,人类在马尔堡病毒面前,长期以来几乎“手无寸铁”——没有任何一款获批的疫苗或特效药。
病毒的“钥匙”——其表面的糖蛋白(GP),是所有入侵策略的核心,也是科学家们研发武器的主要靶点。但马尔堡病毒的这把“钥匙”极其狡猾,它的结构很不稳定,难以被精确瞄准。这导致疫苗研发步履维艰,即便从幸存者体内分离出的抗体,也大多效力微弱,病毒只需一个微小的变异就能轻松摆脱束缚。这场与致命病毒的攻防战,似乎陷入了一个难以逾越的技术瓶颈。
然而,僵局的打破往往源于基础科学的突破。近日,发表在顶级期刊《自然》(Nature)上的一项研究,为这场战斗带来了颠覆性的转机。美国华圣顿大学的David Veesler和Fabio Benigni团队,通过结构生物学与计算设计的精妙结合,不仅稳固了这把善变的“钥匙”,还找到了一把能将其彻底锁死的“万能锁”。
这项研究的核心成果,是一种名为MARV16的全人源单克隆抗体。它的出现,彻底改写了马尔堡病毒抗体疗法的效力天花板。
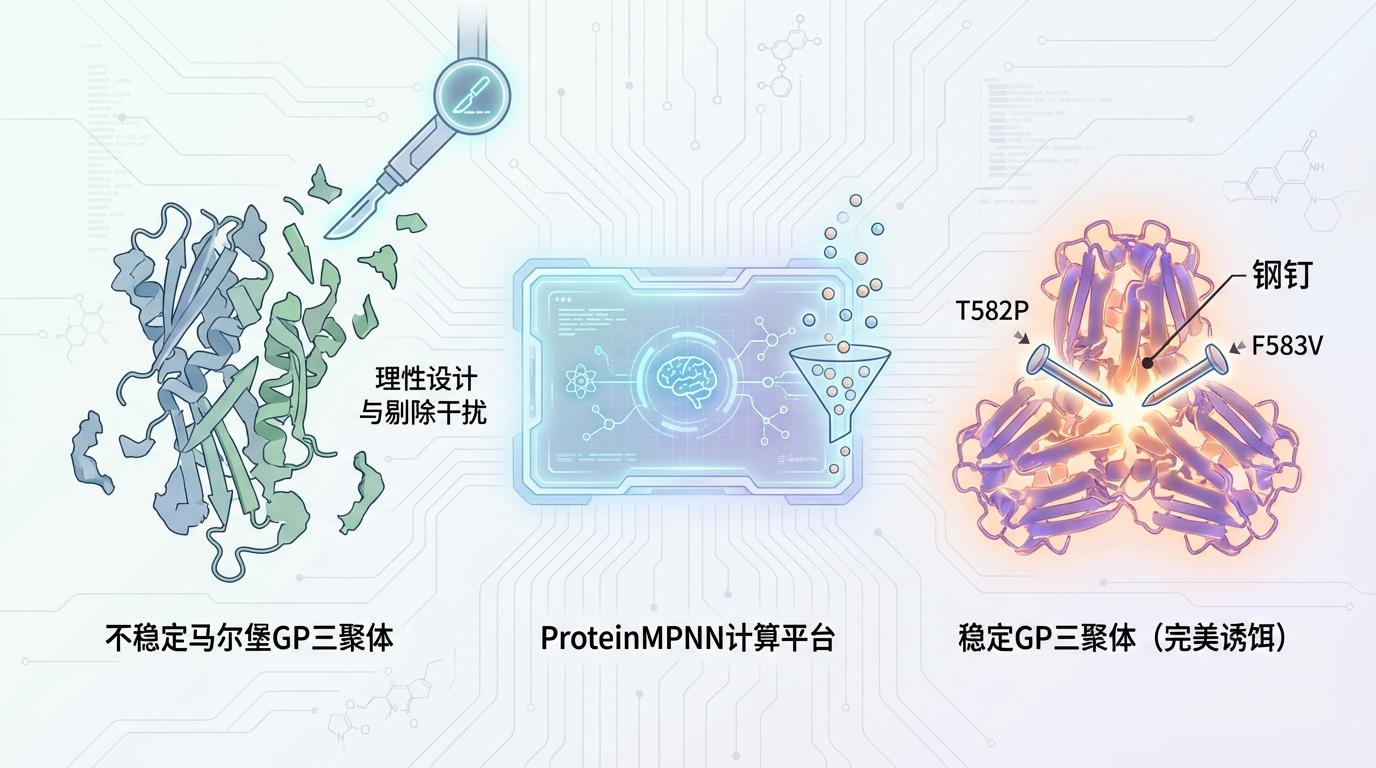
研究团队首先像修复一件精密仪器一样,对马尔堡病毒的糖蛋白(GP)进行了“理性设计”。他们剔除了不必要的“干扰”部分,并借鉴了埃博拉病毒研究的经验。随后,他们借助强大的人工智能工具——计算蛋白质设计平台ProteinMPNN,在原子级别上对GP蛋白进行筛选和改造。最终,他们找到了两个关键的氨基酸突变位点(T582P和F583V),这两个点突变如同给松散的结构打入了“钢钉”,成功创造出一种前所未有稳定的GP三聚体。这个稳定的GP蛋白,成为了完美的“诱饵”。
有了完美的“诱饵”,研究团队利用携带人类抗体基因的转基因小鼠进行免疫,成功“钓”到了一系列高潜力的抗体。经过严格筛选,MARV16脱颖而出。
它的强大超乎想象:
MARV16为何如此强大?借助2.6 Å高分辨率的冷冻电镜技术,科学家们得以在原子尺度上一窥究竟。答案令人惊叹:MARV16采用了一种独特的“双重锁定”机制。

此前的抗体大多只能攻击病毒蛋白上的一个点,而MARV16则像一只精准的手,同时抓住由GP1和GP2两个不同亚基共同构成的三维空间位点。这种独特的结合方式赋予了它两种强大的功能:
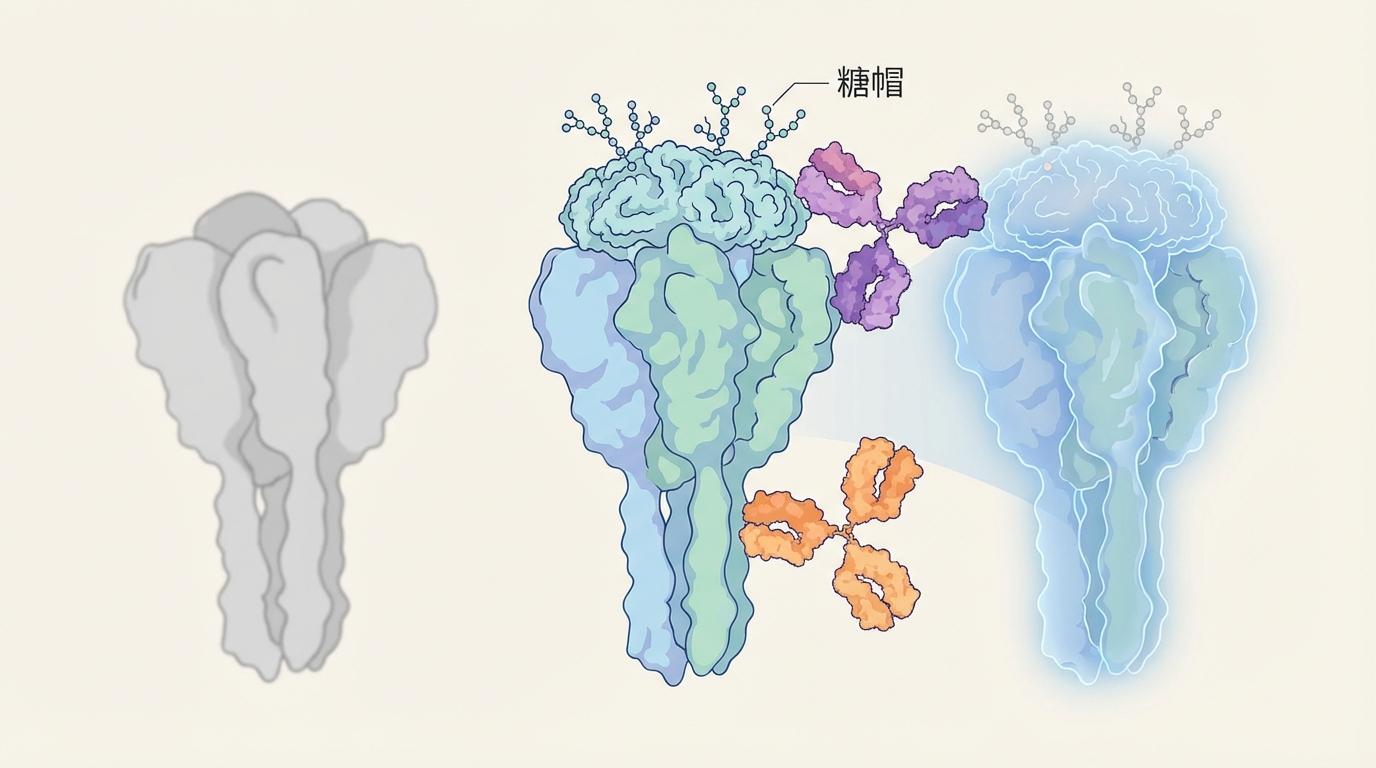
这种双管齐下的策略,正是其强大中和能力的结构基础。这项研究还首次清晰揭示了马尔堡病毒GP蛋白“糖帽”的精细结构,修正了科学界此前的错误认知,进一步加深了对这类致命病毒的理解。
MARV16的突破性意义远不止于其本身。结构分析显示,它的结合位点与过去发现的其他抗体完全不重叠。这意味着它们可以“并肩作战”,同时结合在同一个病毒蛋白上。这为开发“鸡尾酒疗法”铺平了道路。
病毒逃逸实验证实了这一策略的巨大优势。在MARV16单药的压力下,病毒仅需一个突变就有可能逃逸。但当MARV16与另一种抗体联合使用时,病毒必须同时在两个不同位置发生多个突变才能存活,这极大地提高了耐药的门槛,有效防止了病毒在治疗过程中产生耐药性。
更令人振奋的是其临床应用潜力。在豚鼠模型中,即使在感染病毒4天后再注射MARV16,依然能挽救60%的动物生命。这表明MARV16不仅是潜在的预防手段,更是一种极具希望的暴露后治疗药物,能为已经感染的患者带来生机。
这项由结构生物学驱动的发现,不仅为对抗马尔堡病毒这一重大公共卫生威胁提供了强有力的“新武器”,更重要的是,它展示了一种全新的研发范式:通过精准的蛋白质设计和深入的结构分析,我们可以为最危险的病毒打造出前所未有的高效疗法。这束来自微观世界的光,正照亮我们抵御未来高致死性病毒大流行的新路径。