
9 天前

9 天前
一位62岁的卵巢癌患者在经历两次化疗复发后,抱着最后一丝希望参加了免疫治疗临床试验,结果却令人失望——她的肿瘤对PD-1单抗毫无反应。这不是个例:卵巢癌作为女性生殖系统死亡率最高的恶性肿瘤,对当前大热的免疫检查点阻断疗法有效率仅4%-15%,绝大多数患者只能在化疗耐药的绝望中等待。但华中科技大学的团队最近发现,这类「免疫冷肿瘤」里藏着一个被忽略的关键开关,而它的激活,竟和一个常见的抑癌基因缺失直接相关。
你可以把PTEN基因想象成细胞里的「安全闸」——它像个尽职的守门人,死死按住PI3K/AKT这条促进细胞疯长的信号通路。但在卵巢癌里,这个守门人经常「离岗」:高级别浆液性卵巢癌中PTEN单等位基因缺失率高达36%,68.9%的上皮性卵巢癌都存在PTEN蛋白表达降低。
当PTEN缺失,安全闸彻底失灵,PI3K通路持续亢奋,不仅会催着肿瘤细胞疯狂增殖,还会悄悄重塑肿瘤周围的环境:原本应该来剿灭肿瘤的CD8+T细胞数量骤减,免疫抑制性的M2巨噬细胞、调节性T细胞却越聚越多,形成一个密不透风的「免疫囚笼」。更关键的是,研究团队通过单细胞RNA测序和多重免疫组化染色发现,PTEN缺失的卵巢癌组织里,一种叫B7H3的蛋白含量异常升高——而它,正是关闭抗肿瘤免疫的「隐形开关」。
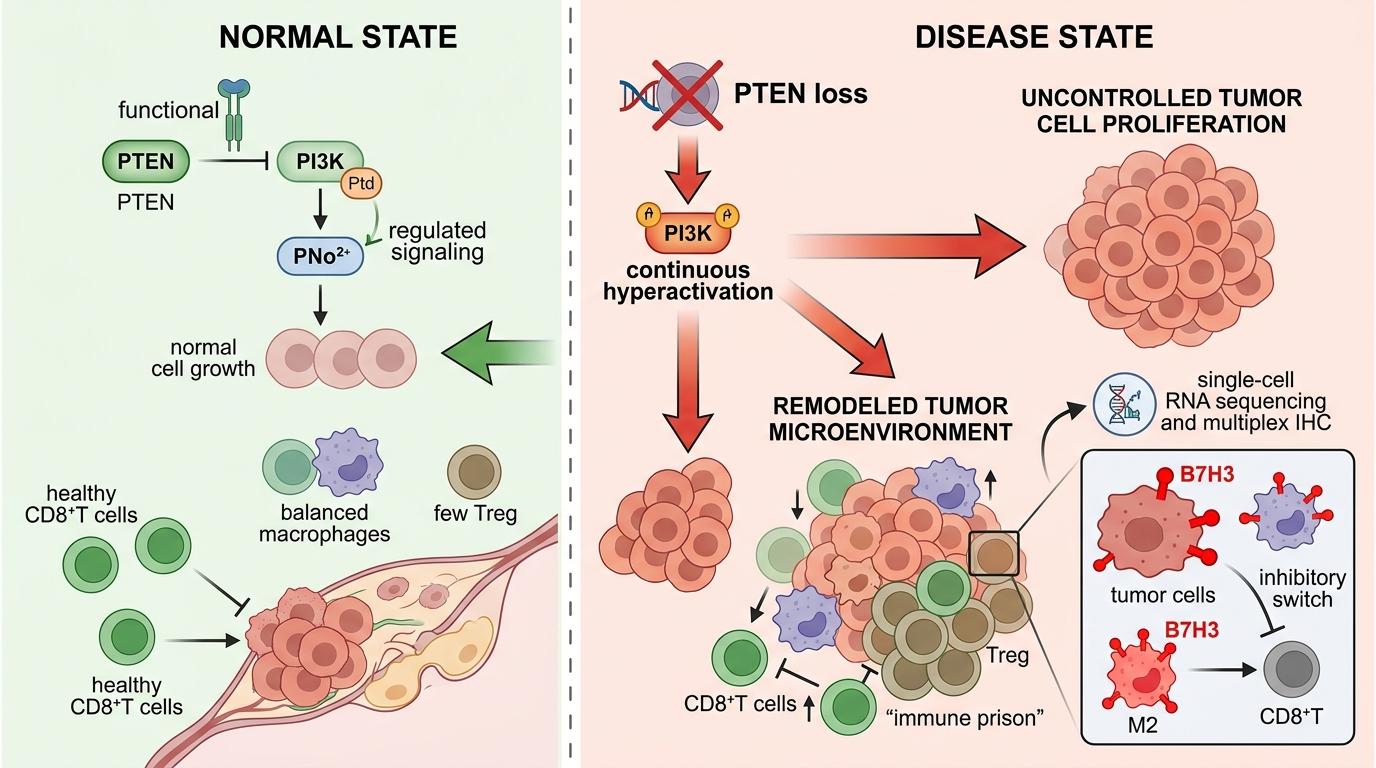
这不是简单的「A导致B」,而是一套精密的连锁陷阱:
PTEN缺失首先激活了mTORC2蛋白复合物,后者会给FOXO1/3这两个转录因子打上「磷酸化标签」,把它们锁在细胞质里,让它们失去调控基因的能力。FOXO1/3失活后,原本被它促进表达的MXI1蛋白含量骤降——MXI1是c-Myc的「天然抑制剂」,它的减少相当于给c-Myc松了绑。
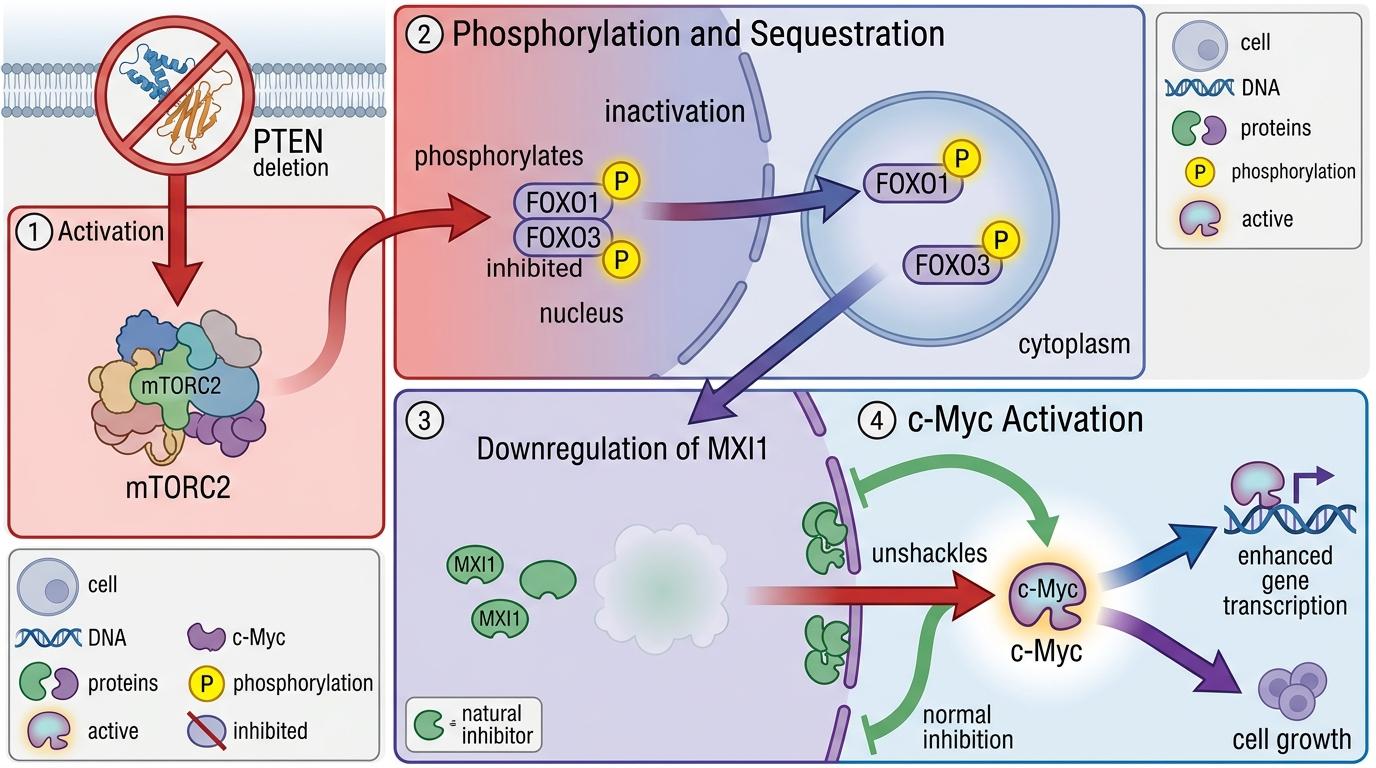
c-Myc是细胞里的「转录推土机」,一旦活性增强,就会疯狂推动下游基因的表达,其中就包括B7H3。当肿瘤细胞表面堆满B7H3,它会像一层「隐形斗篷」,直接抑制CD8+T细胞的增殖和杀伤能力,还会招募更多免疫抑制细胞,把肿瘤的「免疫囚笼」焊得更牢。
在小鼠模型里,这个机制得到了完美验证:给PTEN缺失的卵巢癌小鼠注射抗B7H3抗体后,肿瘤生长被显著抑制,小鼠生存期明显延长;但如果提前清除小鼠体内的CD8+T细胞,这种治疗效果就会完全消失——这意味着,抗B7H3疗法的核心,就是重新唤醒被压制的CD8+T细胞。
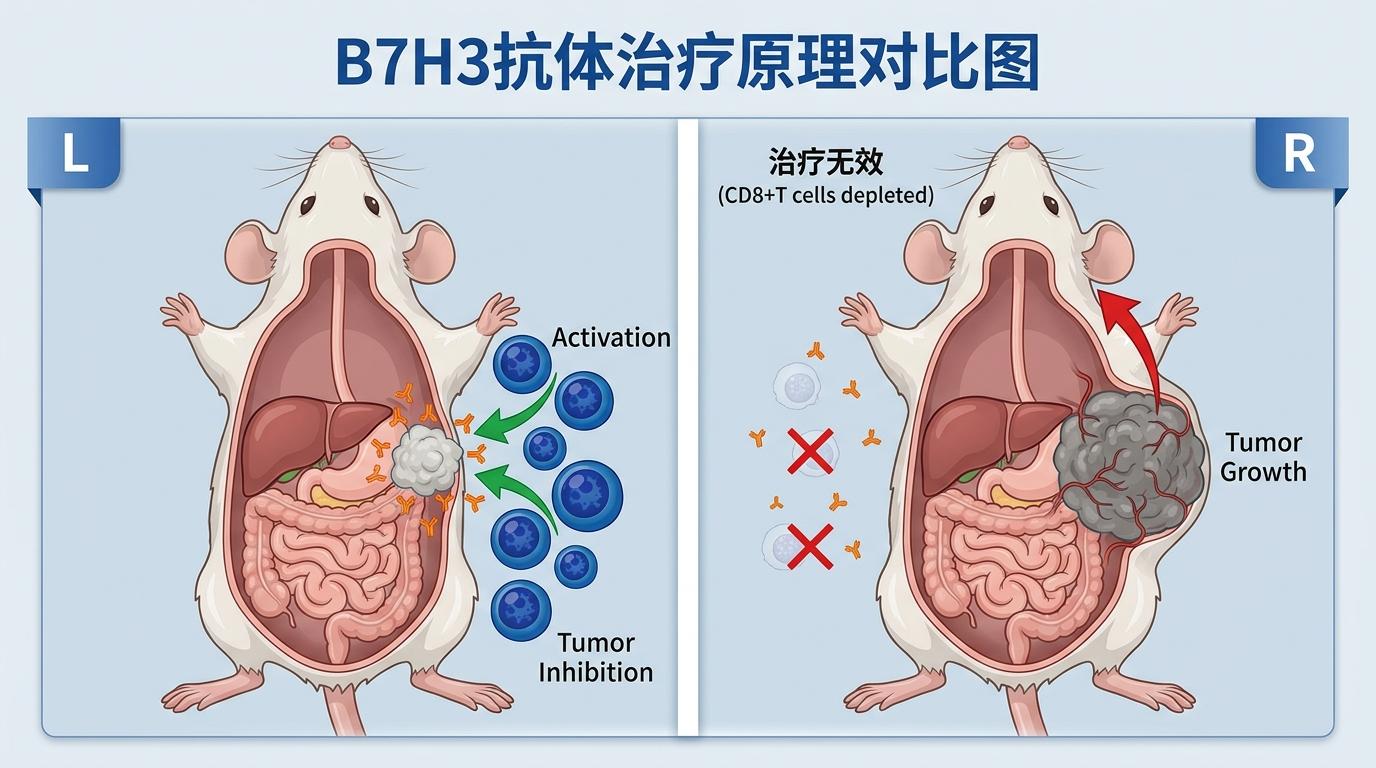
更值得关注的是,这项研究不仅破解了机制,还直接指向了精准治疗的方向:PTEN缺失的卵巢癌患者,恰好是抗B7H3疗法的最佳受益者。
目前针对B7H3的治疗药物已经进入临床试验阶段,包括单克隆抗体、抗体药物偶联物(ADC)等。其中ADC药物凭借「精准定位+强效杀伤」的特点,在B7H3高表达的肿瘤中展现出良好前景。不过研究也指出,单一的抗B7H3疗法可能会引发肿瘤的「补偿性逃逸」,比如PD-L1表达上调,因此未来联合抗PD-1/PD-L1疗法,或许能给PTEN缺失型卵巢癌患者带来更大的生存获益。
当然,这项研究也有局限:目前的结果主要来自临床样本和小鼠模型,还需要更大规模的临床试验来验证抗B7H3疗法在人类患者中的安全性和有效性;另外,如何通过简便的检测手段筛选出PTEN缺失的患者,也是临床转化需要解决的问题。
从20年前发现PTEN是抑癌基因,到今天终于搞清楚它缺失后如何通过分子连锁反应关闭抗肿瘤免疫,人类对卵巢癌的认知又往前迈了关键一步。
「找到锁,才能配出合适的钥匙」,这句话放在肿瘤治疗里再贴切不过。卵巢癌之所以成为「沉默的杀手」,很大程度上是因为我们一直没找对它的「锁孔」。而这项研究,不仅找到了PTEN缺失型卵巢癌的专属锁孔,还亲手打磨出了第一把钥匙——未来,或许会有更多被困在免疫囚笼里的患者,能通过这把钥匙重获生机。
点击充电,成为大圆镜下一个视频选题!