对抗知识焦虑,从看懂这条开始
App 下载
日本iPSC疗法上市:再生医学的曙光与豪赌?
京都大学|住友制药|ReHeart|Amchepry|iPSC疗法|再生医学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
京都大学|住友制药|ReHeart|Amchepry|iPSC疗法|再生医学|医学健康
一片仅有硬币大小、厚度不足0.1毫米的细胞薄片,在实验室的培养皿中微微搏动。它不是来自任何生命体,而是由人类皮肤细胞“逆转时光”后培育出的心肌细胞。当这片“生命补丁”被外科医生轻柔地贴上一颗衰竭的心脏时,一个曾被视为科幻的场景正在成为现实。这不仅是一场手术,更是一个时代的序幕。
2026年2月,全球再生医学领域迎来了一个历史性时刻。日本厚生劳动省专家小组有条件地批准了两款基于**诱导性多能干细胞(iPSC)**的再生疗法上市:
这是全球首次将iPSC技术从实验室的梦想,转化为货架上的商业化药品。它标志着人类终于能够“制造”出活的、功能性的细胞来修复受损的器官。然而,巨大的光环之下,是同样巨大的争议。这两款“神药”的获批,仅仅基于**“个位数”的临床试验患者数据,且缺乏严格的对照组。更令人咋舌的是,其治疗费用预计将高达数百万人民币**。一场关于希望、风险与伦理的全球大讨论,由此拉开帷幕。
这一切的源头,要追溯到2006年。那一年,日本京都大学的山中伸弥教授完成了一项“魔术”:他仅用四个基因,就成功将已经分化的成年体细胞“诱导”回了类似胚胎干细胞的“万能”状态,这就是iPSC。这项发现仿佛按下了细胞的“重置键”,让再生医学摆脱了长期困扰其发展的胚胎干细胞伦理争议。山中伸弥也因此在2012年摘得诺贝尔奖。
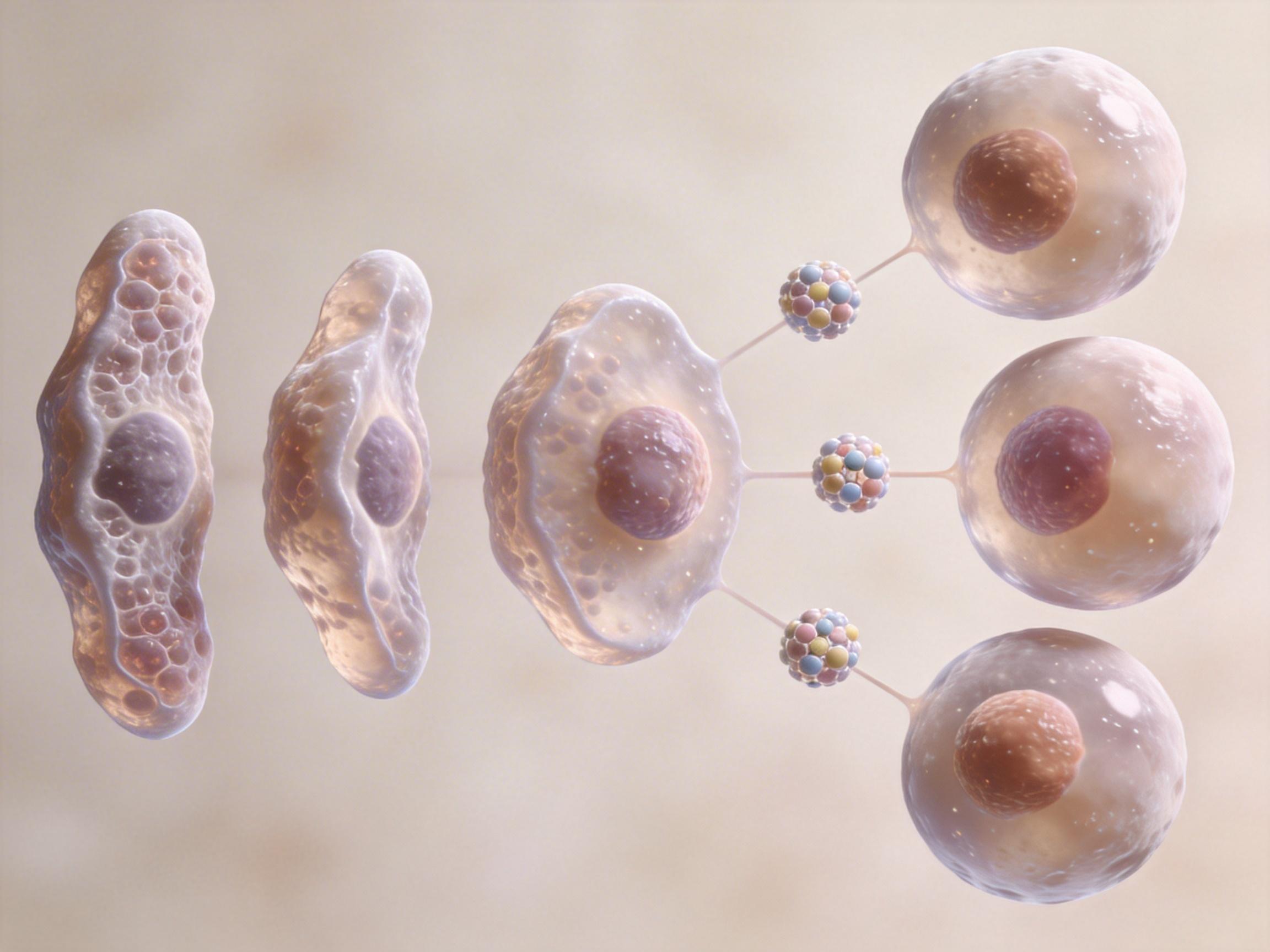
Amchepry疗法正是这一技术的直接应用。帕金森病患者大脑中生产多巴胺的神经元大量死亡,而Amchepry能在体外将iPSC分化为健康的多巴胺能神经前体细胞,通过手术植入患者大脑。这些“新生力量”将在大脑中继续成长,重建被疾病摧毁的神经网络。ReHeart则像一个“心肌创可贴”,将iPSC分化的心肌细胞贴在心脏上,帮助心肌功能恢复。这项从0到1的突破,花费了近二十年的时间。
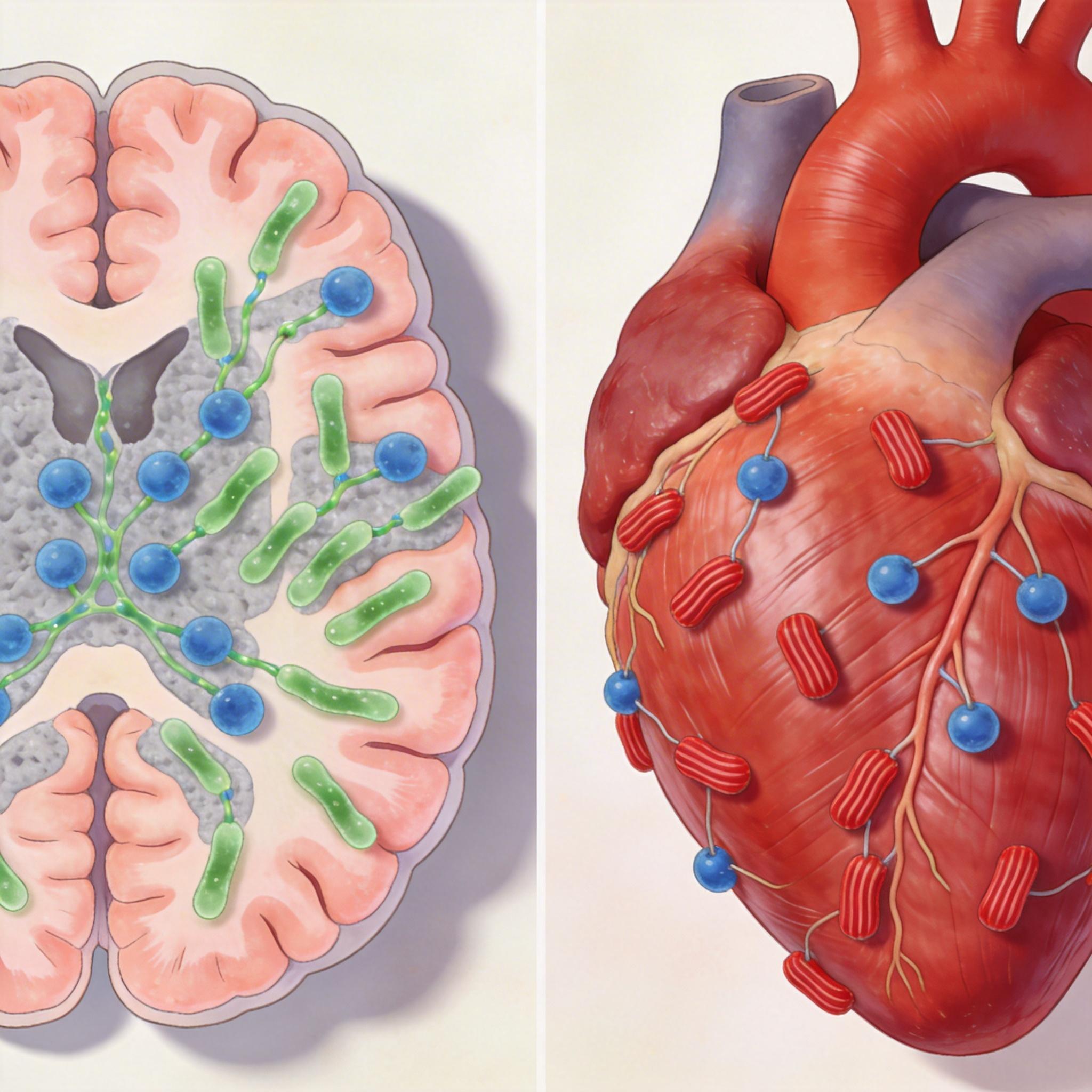
尽管前景诱人,但iPSC疗法并非没有阴影。其最大的安全隐患在于**致瘤性**。在复杂的细胞诱导和分化过程中,哪怕有极少数细胞没有完全分化,仍保持着“万能”的干性,它们进入体内后就可能像失控的种子一样,发展成畸胎瘤。此外,iPSC在重编程和体外培养过程中,基因组可能发生突变,增加癌变风险。
更核心的挑战在于证据的“薄弱”。加州大学戴维斯分校的干细胞研究员保罗·克诺普弗勒直言,这是一次“冒险的监管行为”。仅凭几名患者的改善数据,无法排除安慰剂效应,更不足以评估在更大人群中的安全性和有效性。科学的严谨性,在巨大的商业化诱惑和患者的迫切需求面前,正面临前所未有的考验。
日本此次的批准,采用的是其独特的**“附条件、附期限审批制度”**。这种被业界戏称为“先上车、后补票”的模式,允许创新疗法在证明初步安全性和“疗效趋势”后快速上市,但要求企业在未来7年内持续收集数据,以证明其真正的价值。否则,上市许可将被撤销。
这种模式的优点是显而易见的:它极大地加速了前沿疗法的落地,为无数绝望的患者带来了希望,也为日本抢占了再生医学产业的全球制高点。然而,其弊端也同样突出。它将本应在上市前完成的、耗资巨大的大规模临床试验成本,部分转移给了上市后的患者和国家医保系统。患者在承担高昂费用的同时,也在某种程度上成为了“付费的小白鼠”。
就在不久前,日本一家私人诊所发生的“干细胞注射”致死事件,更是为这种宽松监管环境敲响了警钟。与日本的“激进”形成鲜明对比的是,中国正走向另一个方向。从2026年5月起,中国将实施号称“史上最严”的细胞治疗监管条例,明确规定相关临床研究必须在三甲医院进行,且不得向受试者收费。这体现了两种截然不同的监管哲学:是优先速度,还是优先确定性?
日本的破冰之举,无疑为全球iPSC产业注入了一剂强心针。包括中国的士泽生物、艾尔普再生医学在内的一大批公司,以及美国的BlueRock、Vertex等企业,都在加速推进各自的iPSC疗法进入临床后期。一个由细胞定义的医药新时代,似乎触手可及。
然而,通往普惠的道路依然漫长。横亘在我们面前的,是几座必须翻越的大山:
日本的这次批准,与其说是一个确定的答案,不如说它向全世界提出了一个深刻的问题。它将iPSC技术推到了聚光灯下,迫使我们去直面那些交织在科学、商业、伦理与希望之间的复杂挑战。人类能否驾驭这股强大的生命“重编程”力量,不仅考验着科学家的智慧,更考验着整个社会的远见与责任。