
4 个月前

4 个月前
我们的身体由数万亿个细胞构成,每个细胞都是一座微缩的繁华都市。在这座都市里,线粒体是星罗棋布的发电厂,不知疲倦地为所有生命活动提供能量。然而,这些发电厂也会老化、受损。当它们的运转开始失灵,蛋白质生产线陷入混乱,整座城市便会逐渐失去活力,走向衰败——这便是衰老与疾病在细胞层面的缩影。长期以来,科学家们一直在追问:是什么在维系着这些发电厂的稳定?当警报拉响时,细胞内部的“应急维修系统”又是如何被精确调动的?答案或许就隐藏在细胞器之间一场无声而迅速的对话之中。
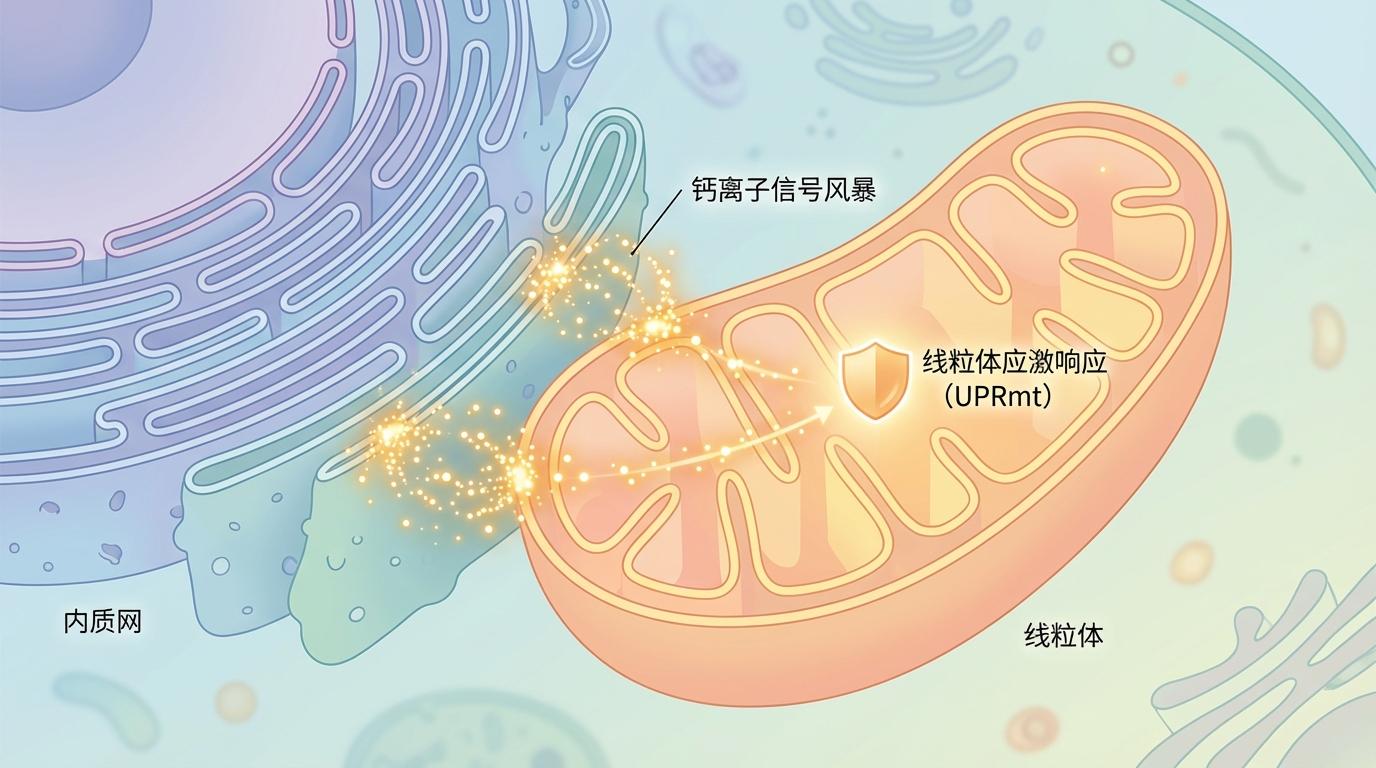
近日,中国科学院大学郭玉婷研究团队在《Protein & Cell》杂志上发表的一项研究,为我们揭开了这个谜团的一角。他们借助自主研发的高时空分辨率成像技术,首次“看清”了细胞内一个前所未见的景象:在线粒体(发电厂)与内质网(细胞的“中央工厂”与钙仓库)的接触点(MERCS),存在着纳米尺度的钙离子信号风暴。这些转瞬即逝的钙信号,如同一串串精准的密码,指挥着细胞启动一套名为“线粒体应激响应”(UPRmt)的古老防御程序。
UPRmt是细胞为维护线粒体健康的“王牌维修队”,一旦线粒体内部出现蛋白折叠错误等问题,这支队伍就会被激活,生产出大量的伴侣蛋白和蛋白酶,清理故障、修复损伤,从而维持稳定,甚至延长寿命。这一机制在从线虫到灵长类动物的生命中普遍存在,但它在哺乳动物细胞中究竟如何被激活,一直是困扰科学界的难题。郭玉婷团队的研究,正是捅破了这层窗户纸,他们发现,调控UPRmt的关键,就在于MERCS这个微小的接触点上那场精妙的钙离子“对话”。
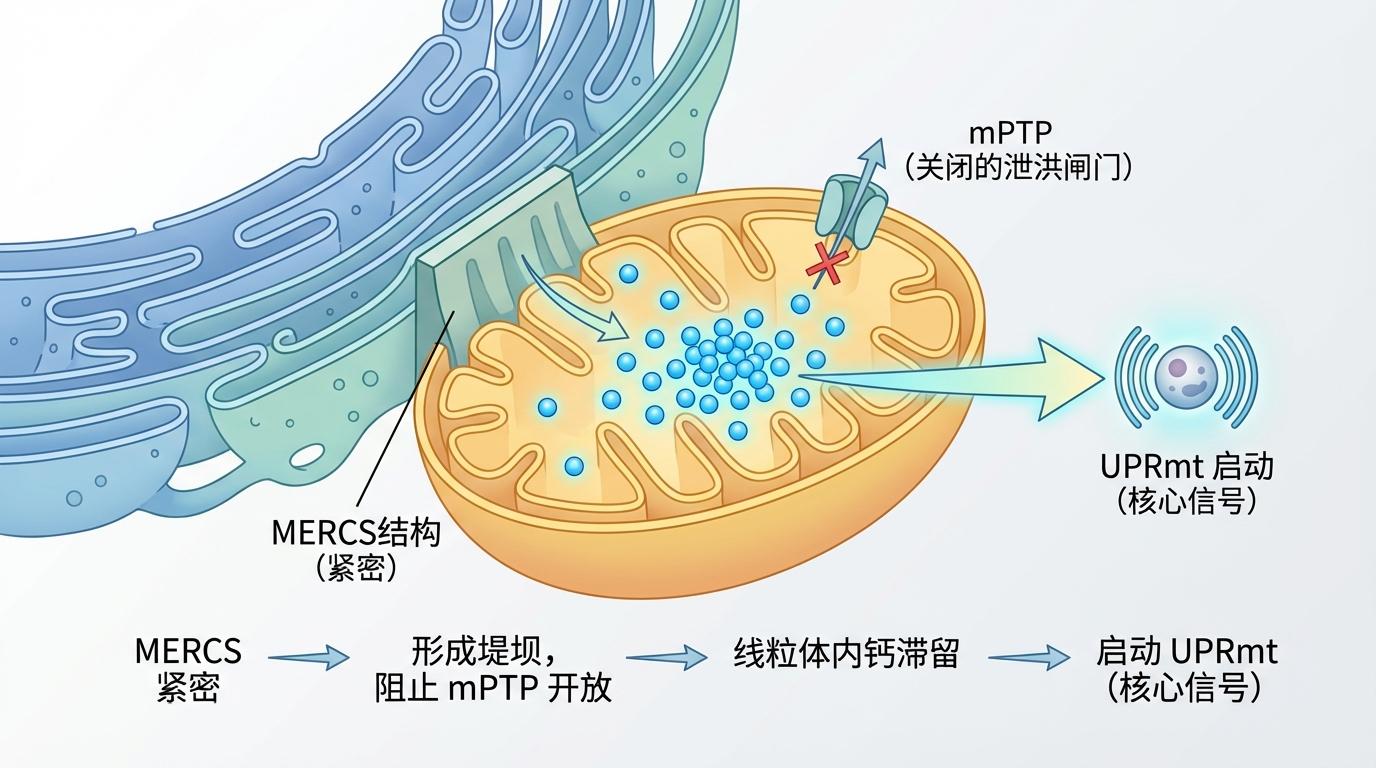
这项研究的精妙之处在于,它揭示了一个环环相扣、多层联动的复杂调控网络。研究人员发现,当MERCS结构紧密、功能增强时,它就像一道堤坝,限制了线粒体内的钙离子外流,阻止了一个名为mPTP的“泄洪闸门”的开放。这种线粒体内的“钙滞留”,正是启动UPRmt的核心信号。
这个信号随后兵分两路,以一种“双保险”的模式,向细胞核这个“总指挥部”传递警报:
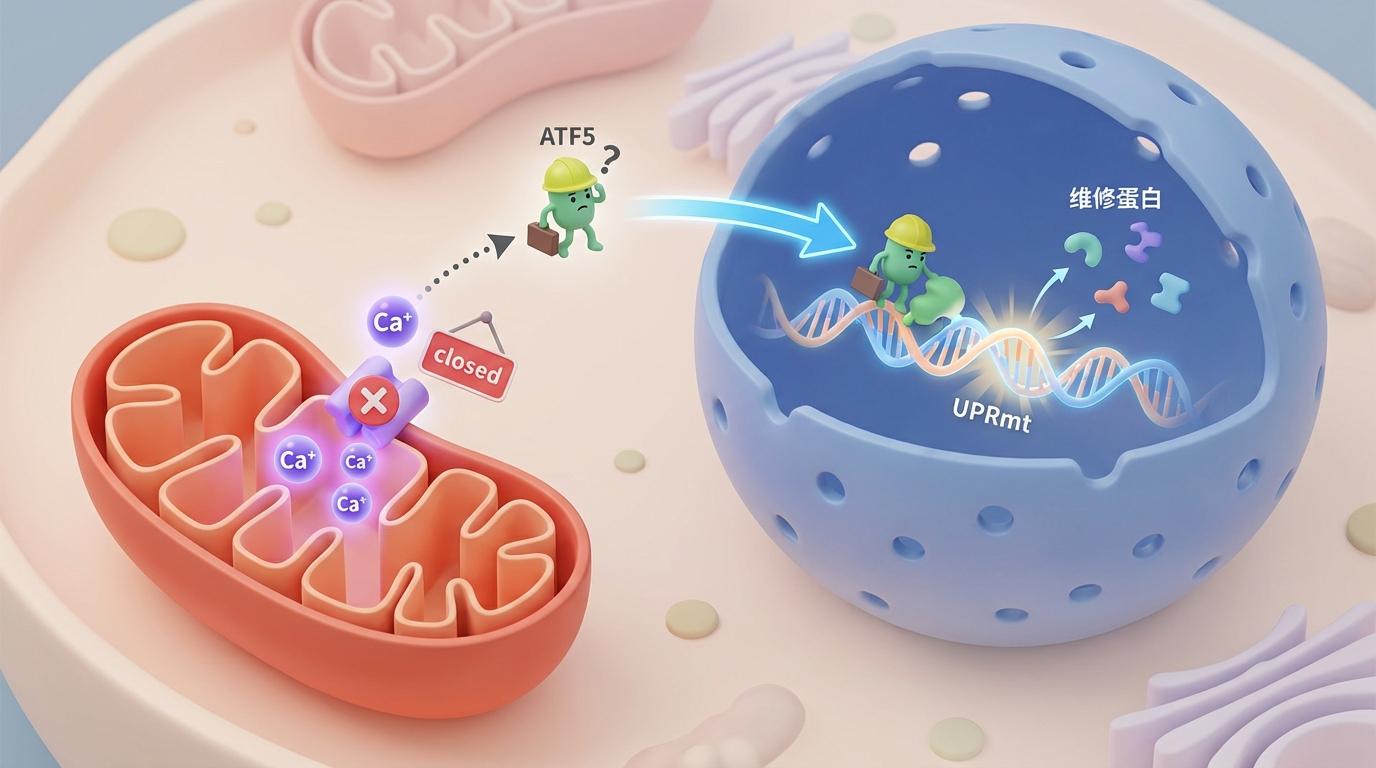
研究人员通过超高分辨率成像技术观察到,线粒体内钙离子水平升高,会阻碍一个名为ATF5的转录因子进入线粒体。ATF5原本是需要进入线粒体工作的“现场主管”,但现在路被堵死了。于是,这位“主管”被迫改变路线,掉头奔向细胞核。在那里,它摇身一变,成为启动UPRmt相关基因表达的“信使”,直接下达了生产维修蛋白的指令。
就这样,一个纳米尺度的钙信号,同时启动了转录层面的直接命令和表观遗传层面的全局许可,构成了一场精妙的“钙-转录-表观”三重奏,确保了细胞在面对线粒体压力时,能够做出快速而有力的反应。
这一发现的意义远不止于揭示一个基础生命过程。在阿尔兹海默症(AD)等神经退行性疾病中,错误折叠的蛋白质(如β-淀粉样蛋白Aβ)大量积累,对线粒体造成严重毒害,导致神经元能量衰竭和死亡。郭玉婷团队在AD细胞模型中验证了他们的发现。
他们发现,通过药物(如环孢菌素A)或基因手段,人为地关闭mPTP这个“泄洪闸门”,就能模拟MERCS增强时的钙滞留状态,从而成功激活UPRmt。结果令人振奋:这套被激活的内在防御系统,能有效缓解Aβ蛋白对线粒体的损伤,保护神经细胞免于凋亡。这表明,MERCS介导的钙信号通路,是干预AD病理进程的一个极具潜力的新靶点。
这项研究为我们描绘了一幅细胞内部通信网络的壮丽图景,它连接了从纳米尺度的离子流动到宏观尺度的衰老与疾病。它不仅深化了我们对细胞器间通讯的理解,也为开发针对蛋白质毒性疾病的新型疗法提供了明确的方向。过去,我们可能更关注如何清除有毒蛋白,而现在,我们或许可以另辟蹊径——通过增强细胞自身的线粒体修复能力来对抗疾病。
当然,前路依然漫长。这个“钙-转录-表观”调控轴在不同类型的细胞中是否存在差异?在真实的活体大脑中,它又是如何运作的?我们能否开发出足够精准且安全的药物,去微调MERCS的功能,从而“指挥”细胞启动自我修复?
解开这些谜题,需要更先进的成像技术和更深入的跨学科合作。但无论如何,这项发现已经为我们点亮了一盏新的明灯。它告诉我们,在与衰老和疾病的漫长抗争中,最强大的盟友,或许就隐藏在我们每一个细胞的深处,在那场由钙离子指挥的、维系生命和谐的古老交响之中。
点击充电,成为大圆镜下一个视频选题!