对抗知识焦虑,从看懂这条开始
App 下载
第七例艾滋病治愈:免疫重建颠覆CCR5神话
抗逆转录病毒药物|免疫重建|骨髓移植|CCR5Δ32突变|艾滋病治愈者|感染性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
抗逆转录病毒药物|免疫重建|骨髓移植|CCR5Δ32突变|艾滋病治愈者|感染性疾病|医学健康
在人类与艾滋病病毒(HIV)长达数十年的漫长战役中,治愈始终是一个遥不可及的梦想。全球近4000万HIV感染者,每日服用抗逆转录病毒药物(ART),维持着生命,却无法摆脱病毒的阴影。直到2007年,“柏林病人”蒂莫西·雷·布朗的出现,才像一道闪电划破夜空,首次点燃了治愈的希望。他因白血病接受了骨髓移植,奇迹般地不仅治愈了癌症,也清除了体内的HIV病毒。此后,医学界普遍相信,治愈的关键在于移植了携带罕见CCR5Δ32纯合突变的干细胞,这种突变能让免疫细胞天然关闭HIV入侵的大门。然而,这道“黄金法则”在2025年12月1日被一篇发表于《自然》杂志的重磅论文打破,第七位艾滋病“治愈者”的故事,正悄然改写着我们对艾滋病治愈机制的深刻认知。
这则突破性新闻的主角,是一位被称为“第二位柏林病人”(B2)的60岁德国男性。他于2009年被诊断出HIV感染,不幸的是,2015年又罹患急性髓系白血病。面对生命双重威胁,德国柏林夏里特医学院的Olaf Penack和Christian Gaebler团队决定为他进行异体造血干细胞移植。然而,与前五位治愈者不同,这次他们未能找到携带CCR5Δ32纯合突变的理想供体。最终,他们选择了一位仅携带CCR5Δ32杂合突变(即只有一个突变拷贝,细胞表面仍表达功能性CCR5受体)的无关捐赠者。
移植三年后,这位病人做出了一个大胆的决定——停止抗逆转录病毒治疗。在没有药物抑制的情况下,奇迹发生了:他的血浆HIV RNA病毒载量持续低于检测下限,这一无病毒状态已持续超过七年,长达七年零三个月,成为全球第七位被正式记录的艾滋病功能性治愈者。这一结果,连同此前“日内瓦病人”——一位接受完全不携带CCR5基因突变干细胞移植也实现长期病毒抑制的案例——共同向传统的“CCR5纯合缺失是治愈前提”的观点发出了强烈挑战。
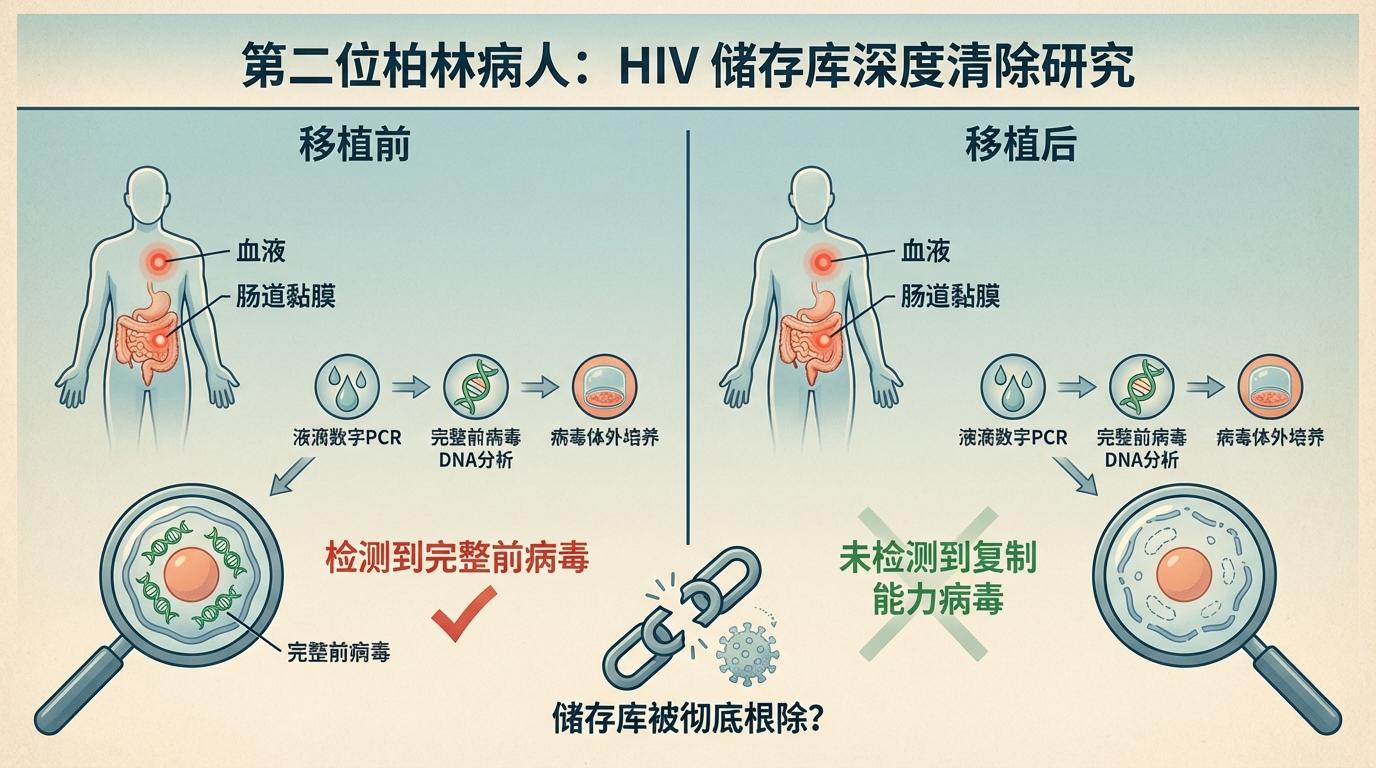
为了揭示“第二位柏林病人”治愈背后的秘密,研究团队进行了一系列深入而精密的检测。他们采用液滴数字PCR、改良的完整前病毒DNA分析法以及超高灵敏度病毒体外培养等技术,对患者血液和肠道黏膜组织中的HIV病毒储存库进行了地毯式搜索。结果令人振奋:移植前患者体内存在可检测到的完整前病毒,但移植后,这些具有复制能力的病毒竟无影无踪,这强烈提示病毒储存库已被深度清除,甚至可能被彻底根除。
免疫学证据进一步支持了这一结论。随着时间推移,患者体内HIV特异性抗体水平显著下降至极低或无法检测,其中和活性也显著衰退。同时,针对HIV蛋白的特异性CD4+或CD8+ T细胞反应也消失殆尽,而对巨细胞病毒、EB病毒等其他病原体的T细胞反应则保持正常。这表明免疫系统已不再遭遇HIV抗原的刺激,间接证实了病毒储存库的缺失。
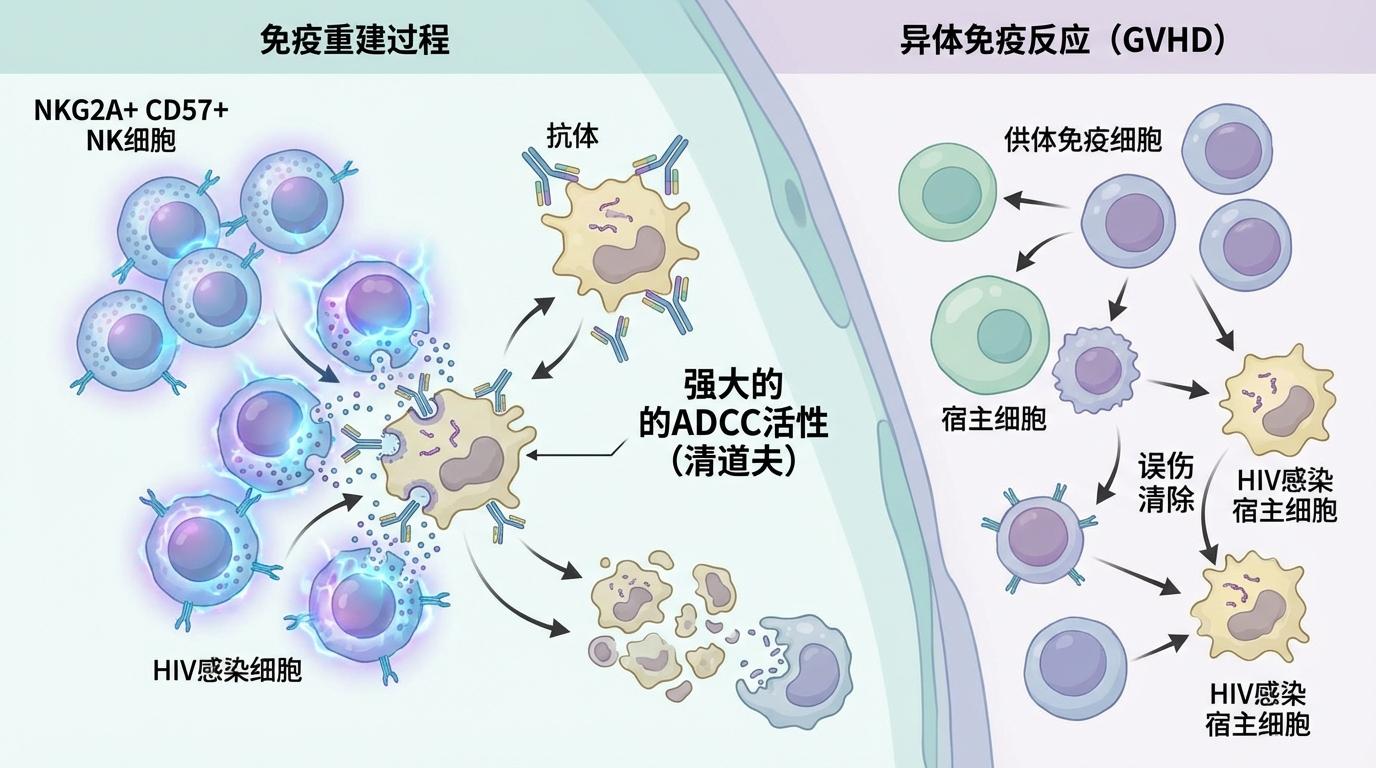
那么,在CCR5受体功能并未完全丧失的情况下,究竟是何种力量清除了顽固的病毒储存库?研究将焦点转向了移植后的免疫重建过程。一个关键发现是,在移植前后这一窗口期,患者体内一种独特的NK细胞亚群(NKG2A+ CD57+)显著扩增,并且其血浆介导的抗体依赖性细胞毒性作用(ADCC)活性异常强大。研究团队推测,这种强大的ADCC活性,就像一支由NK细胞组成的“清道夫”部队,精准识别并清除了最后残存的、被HIV感染的细胞,从而对病毒储存库的深度清除起到了至关重要的推动作用。此外,干细胞移植伴随的异体免疫反应,如移植物抗宿主病(GVHD),也可能在清除白血病细胞的同时,“误伤”并扫清了携带HIV的宿主细胞,无意中协助了病毒的清除。
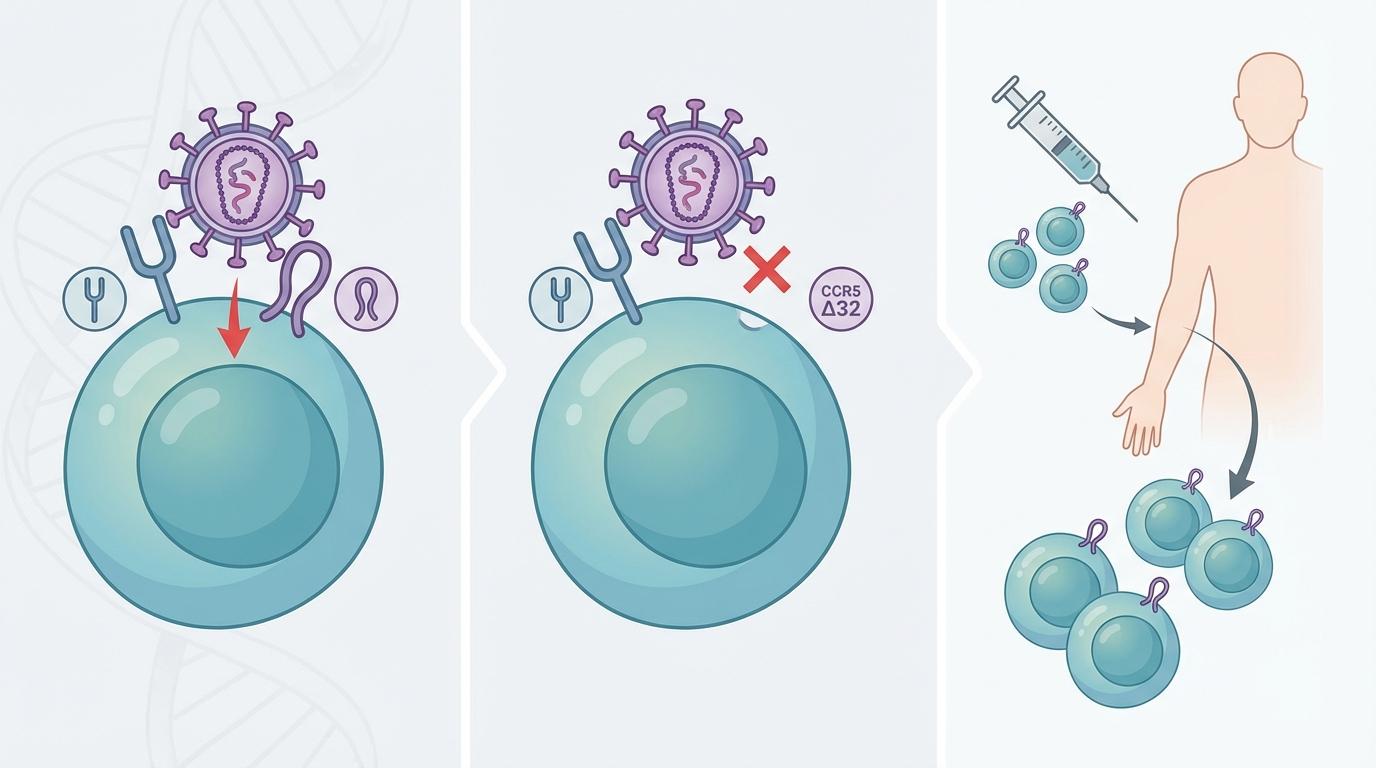
艾滋病病毒入侵人体细胞,需要CD4受体和辅助受体CCR5或CXCR4的协同作用。1996年,邓宏魁教授首次发现了CCR5基因,并证实其是HIV-1病毒入侵细胞的关键受体。紧接着,科学家们发现携带CCR5Δ32纯合突变的人对HIV-1感染具有天然抵抗力,这一发现犹如一道曙光,指明了治愈的可能方向。当“柏林病人”蒂莫西·雷·布朗因白血病接受了CCR5Δ32纯合突变供体的干细胞移植并成功治愈HIV后,CCR5缺失被奉为治愈艾滋病的“黄金法则”,成为医学界长期以来的共识。
然而,随着“日内瓦病人”和“第二位柏林病人”的相继出现,这一“黄金法则”正被颠覆。他们以实际案例证明,即使供体细胞并非完全关闭HIV入侵的大门,甚至完全不具备CCR5突变,通过干细胞移植实现的强大免疫重建和病毒储存库的深度清除,同样能够达到长期病毒缓解。这一范式转变意义重大,它拓宽了潜在的干细胞供体范围,为更多合并血液系统恶性肿瘤的HIV感染者带来了治愈的希望,也促使科学家们将目光从单一的病毒入侵阻断,转向更为复杂的免疫清除机制。
“第二位柏林病人”的成功治愈,无疑为全球艾滋病研究注入了新的活力。数学模型分析显示,该患者停药六年后仍不发生病毒反弹的概率极低,估算值仅为0.07%,这无疑为长期缓解的可持续性提供了理论支持。然而,造血干细胞移植仍是一种高风险、高侵入性且资源有限的治疗手段,目前仅适用于同时患有血液系统恶性肿瘤的HIV感染者,远未达到普遍推广的条件。
尽管如此,对免疫重建和病毒储存库深度清除机制的深入理解,正为开发更安全、更广泛适用的新型疗法指明方向。未来的研究将聚焦于:
此外,长效抗逆转录病毒药物(ART)和暴露前预防(PrEP)药物(如吉利德科学的Lenacapavir,每年只需注射两次)的持续发展,也在不断提升HIV的预防和管理水平。人类对艾滋病的终极目标——“功能性治愈”(无需服药即可长期控制病毒)乃至“绝对治愈”(彻底清除体内所有病毒)——正变得越来越清晰。
尽管希望之光闪耀,我们仍需清醒认识到艾滋病治愈之路上的重重挑战。造血干细胞移植的高风险性,包括移植物抗宿主病、严重感染和高死亡率,使其无法成为普遍的治愈方案。基因编辑技术虽然前景广阔,但“脱靶效应”的潜在风险、效率瓶颈以及围绕“基因编辑婴儿”事件的伦理争议,都提醒着我们必须审慎前行,确保科学研究在严格的伦理框架内进行。
全球艾滋病防治工作也面临资金短缺的严峻挑战,这可能延缓创新疗法的研发和推广。此外,“治愈误解”也可能导致患者对现有ART治疗产生动摇,从而带来公共卫生风险。科学的进步必须伴随着公众的理解和教育,才能真正造福人类。
“第二位柏林病人”的故事,不仅仅是医学上的一个里程碑,更是人类探索未知、挑战极限精神的生动写照。它告诉我们,艾滋病治愈的钥匙,或许并非仅仅在于关闭病毒入侵的大门,更在于唤醒和重建我们自身免疫系统的强大力量,让其成为清除病毒储存库的“清道夫”。从CCR5的“黄金法则”到免疫重建的广阔天地,我们正目睹一场深刻的范式转变。虽然通往普遍治愈的道路依然漫长且充满挑战,但每一次突破都像一束光,照亮了前行的方向。艾滋病治愈的希望之火,正以前所未有的姿态,在人类的科学征程中熊熊燃烧,激励着我们不断前行,直至终结艾滋病的时代。