对抗知识焦虑,从看懂这条开始
App 下载
给肺癌织一张网,精准捕杀还不伤及无辜
药物递送系统|联合治疗|AIE光敏剂|肺癌患者|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
药物递送系统|联合治疗|AIE光敏剂|肺癌患者|肿瘤学|医学健康
当医生告诉一位肺癌患者“已经转移到肺部”时,这句话的重量,远不止是病情通报——它意味着传统化疗的毒副作用会比疗效更突出,意味着靶向药可能很快耐药,意味着患者要在“杀敌一千自损八百”的困境里挣扎。
2026年春天,深圳的三个科研团队联手,把这个困境撕开了一道口子:他们给肺肿瘤织了一张看不见的“蛛网”,既能精准“粘住”癌细胞,又能同时用四种手段联合绞杀,还能让药物在肺部待足时间,不随便乱跑。
这张“蛛网”到底是什么?它怎么做到既精准又高效?
你可以把这张“蛛网”拆解成两个核心部件:一个是负责“发光+杀敌”的AIE光敏剂——简单说就是一种见光就“变身”的分子,既能发出近红外二区的光帮医生定位肿瘤,又能产生活性氧和热量直接杀癌细胞;另一个是负责“搭网+控场”的g-C₃N₄纳米片——一种像超薄石墨片的二维材料,轻、稳、生物相容性好,还能像支架一样撑住光敏剂。
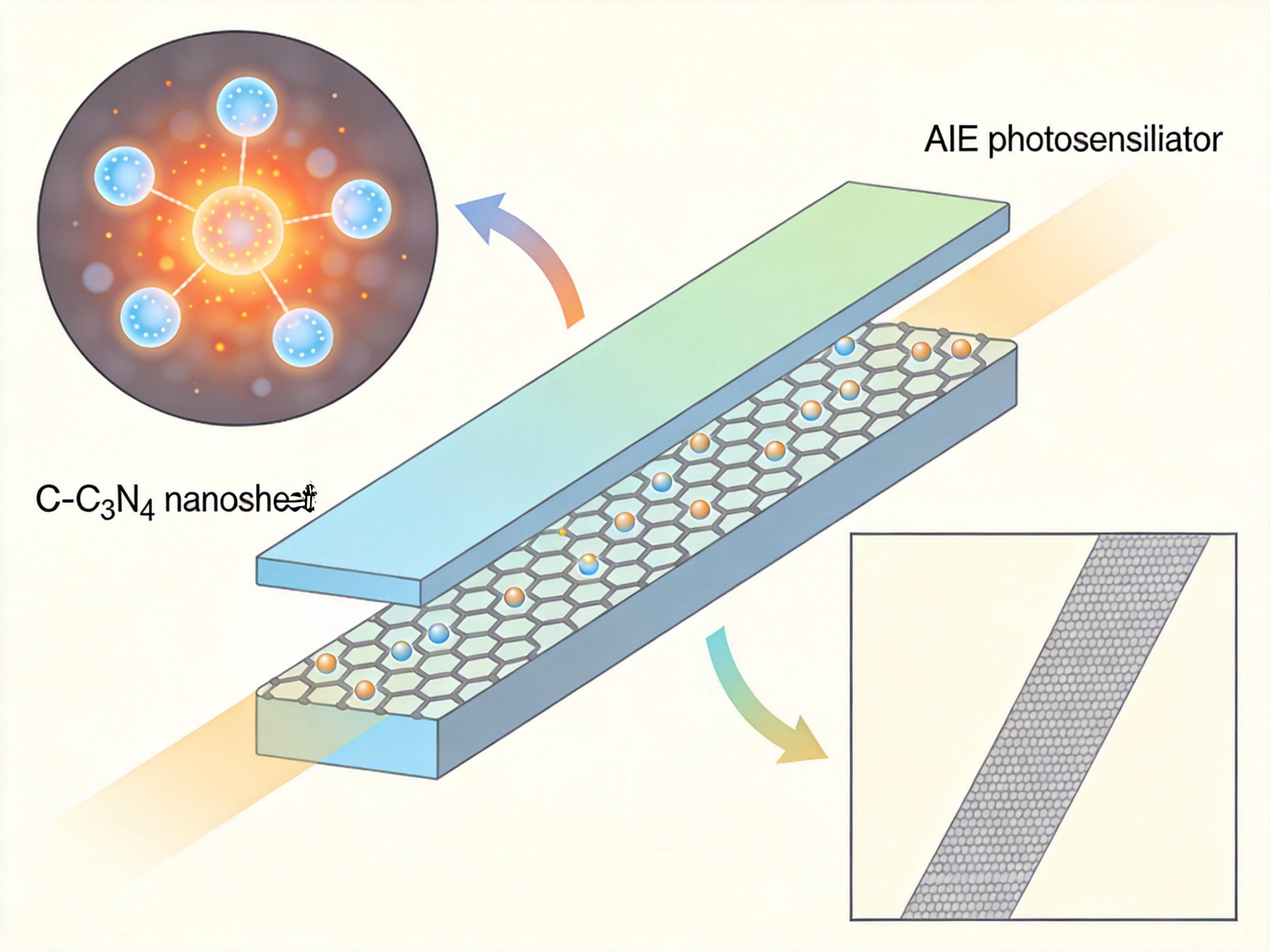
但真实的机制比这个类比更精确: 科研团队给AIE光敏剂设计了“三苯胺供体-苯并双噻二唑受体”的结构,再用噻吩类π桥连接,让它既能吸收近红外光,又能在聚集时反而发光更强——这解决了传统光敏剂一扎堆就“罢工”的问题。然后他们把带羧基的光敏剂通过静电作用“粘”在g-C₃N₄纳米片上,形成稳定的复合结构。
更关键的是,g-C₃N₄纳米片能像模具一样,把光敏剂的分子构象掰成特定角度。量子化学计算和分子动力学模拟显示:两者的结合能越高、分子二面角变化越显著,光敏剂的荧光就越亮,产生活性氧和热量的效率就越高。
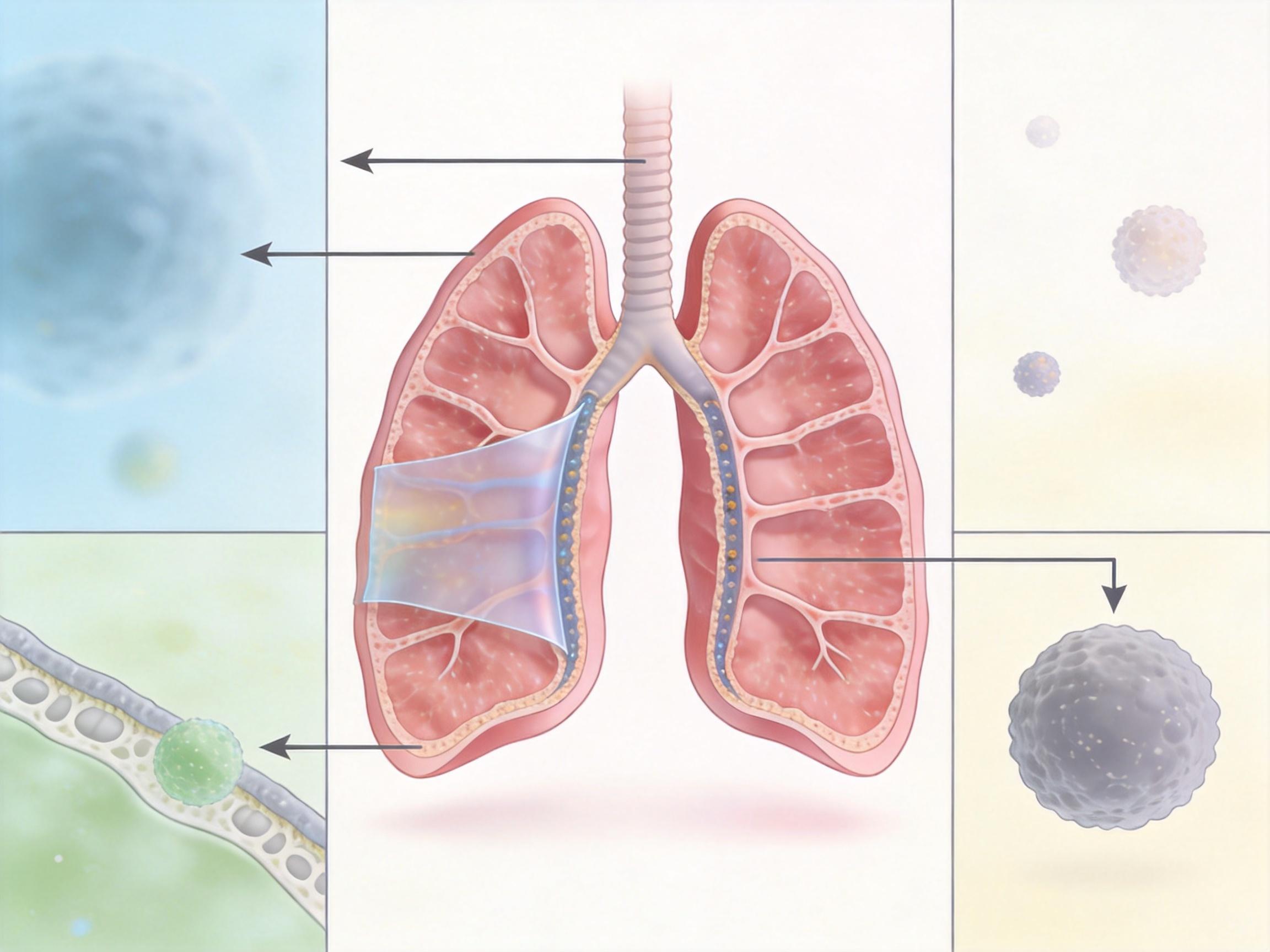
传统肺癌药物的最大痛点,就是“留不住”——要么一进血液就被肝肾代谢,要么被肺部的巨噬细胞当成“异物”吞掉,真正能到达肿瘤的药量不足1%。
而这张“蛛网”用了一个巧妙的办法:g-C₃N₄纳米片的二维结构和1-5微米的粒径,刚好能卡在肺泡的缝隙里,就像一张魔毯铺在肺部,既不会被黏液纤毛轻易扫走,也不会被巨噬细胞吞噬。实验显示,它在肺部的滞留时间比传统纳米粒子长得多,为后续治疗攒够了“弹药”。
当医生用660纳米的光纤把光精准送到肿瘤部位时,好戏才真正开始: AIE光敏剂被激活后,同时启动四种杀敌模式:光动力疗法产生活性氧直接氧化癌细胞,光热疗法把局部温度升到50℃“烫死”肿瘤,免疫原性细胞死亡释放肿瘤抗原唤醒自身免疫系统,还有g-C₃N₄纳米片催化产生的治疗性气体从内部瓦解肿瘤。
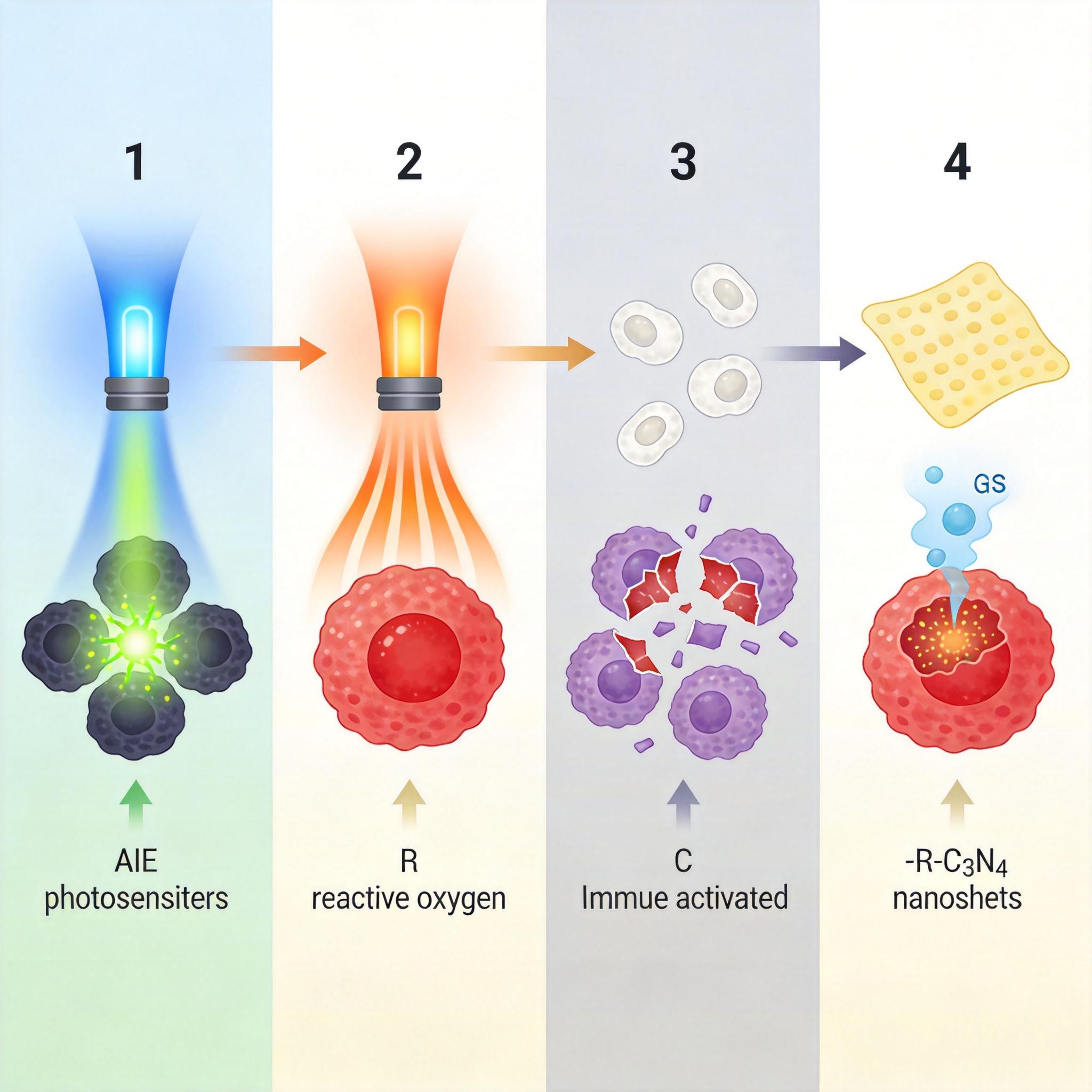
这种多模式协同的效果是1+1+1+1远大于4:动物实验显示,它能显著缩小肺转移瘤的体积,还不会对正常组织造成明显损伤。
当然,这张“蛛网”还不是完美的。
目前它还只在动物实验阶段,要走进临床,还得解决几个问题:比如怎么进一步提高对深层肿瘤的光照穿透性,怎么应对肿瘤内部的低氧环境——毕竟光动力疗法很依赖氧气;还有,长期留在肺部的g-C₃N₄纳米片会不会有潜在的毒性,也需要更长期的安全性评估。
不过科研团队已经有了方向:他们正在设计能适应低氧环境的Type I AIE光敏剂,打算把免疫检查点抑制剂也整合到“蛛网”里,让免疫系统能持续追杀漏网的癌细胞;还想用AI辅助设计更高效的光敏剂分子,优化纳米片的结构。
更值得关注的是,这种“蛛网捕蝶”的思路,不仅适用于肺癌,还能推广到其他肺部疾病——比如肺结核、肺纤维化,只要把“捕蝶”的靶点换成对应的病原体或病变细胞就行。
当我们谈论癌症治疗的未来时,真正的突破从来不是“发明一种更毒的药”,而是“找到一种更聪明的办法”——让药物像精准的猎手,只盯着目标,不伤害无辜。
这张给肺肿瘤织的“蛛网”,就是这种聪明办法的缩影:它把材料科学、分子生物学、光学和免疫学拧成了一股绳,用最温和的方式,实现了最有力的打击。
精准的温柔,才是对抗癌症的终极武器。
未来的某一天,肺癌患者可能不再需要承受化疗的痛苦,只要通过气管滴注这张“蛛网”,再用光纤照一照,就能让肿瘤悄悄消失——这不是科幻,是正在实验室里慢慢变成现实的希望。