
2 天前

2 天前
全球每年32.5万新发黑色素瘤患者里,近半数带着BRAF基因突变——这个靶点曾让医生们看到希望:靶向药能在几周内把肿瘤缩小大半。但残酷的是,90%的患者会在一年内耐药复发。过去所有人都默认,这是癌细胞在药物压力下慢慢攒出了新突变,就像小偷慢慢磨开了锁。直到西雅图系统生物学研究所的团队用高分辨率技术拍下了「分子电影」,才发现真相完全不是这样:癌细胞的耐药逃生,在吃药后的几小时内就已经启动了。这到底是怎么回事?
你可以把BRAF突变的黑色素瘤细胞想象成一群有固定职业的工人——它们本来是「黑色素细胞」,有着自己的专属技能和身份标记。当靶向药进来切断BRAF信号通路,就像突然断了工厂的电。
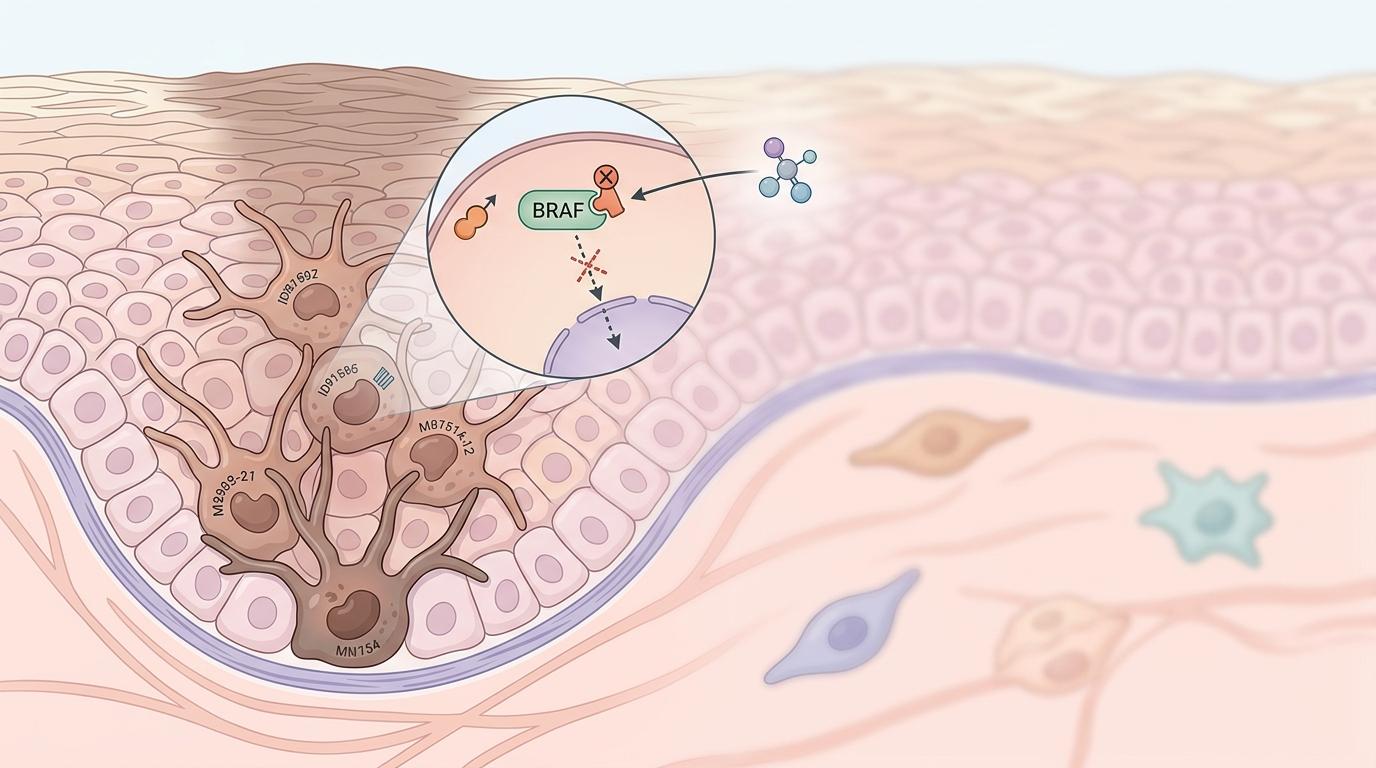
但这些工人没有坐以待毙。
药物进入细胞的几小时内,BRAF抑制剂会先破坏癌细胞的抗氧化防御系统,导致大量活性氧(ROS)堆积——就像工厂断电后引发了火灾。氧化应激信号立刻激活了细胞内的NF-κB通路,这个原本管炎症和应激的「应急指挥中心」,瞬间变成了癌细胞的「逃生总指挥」。
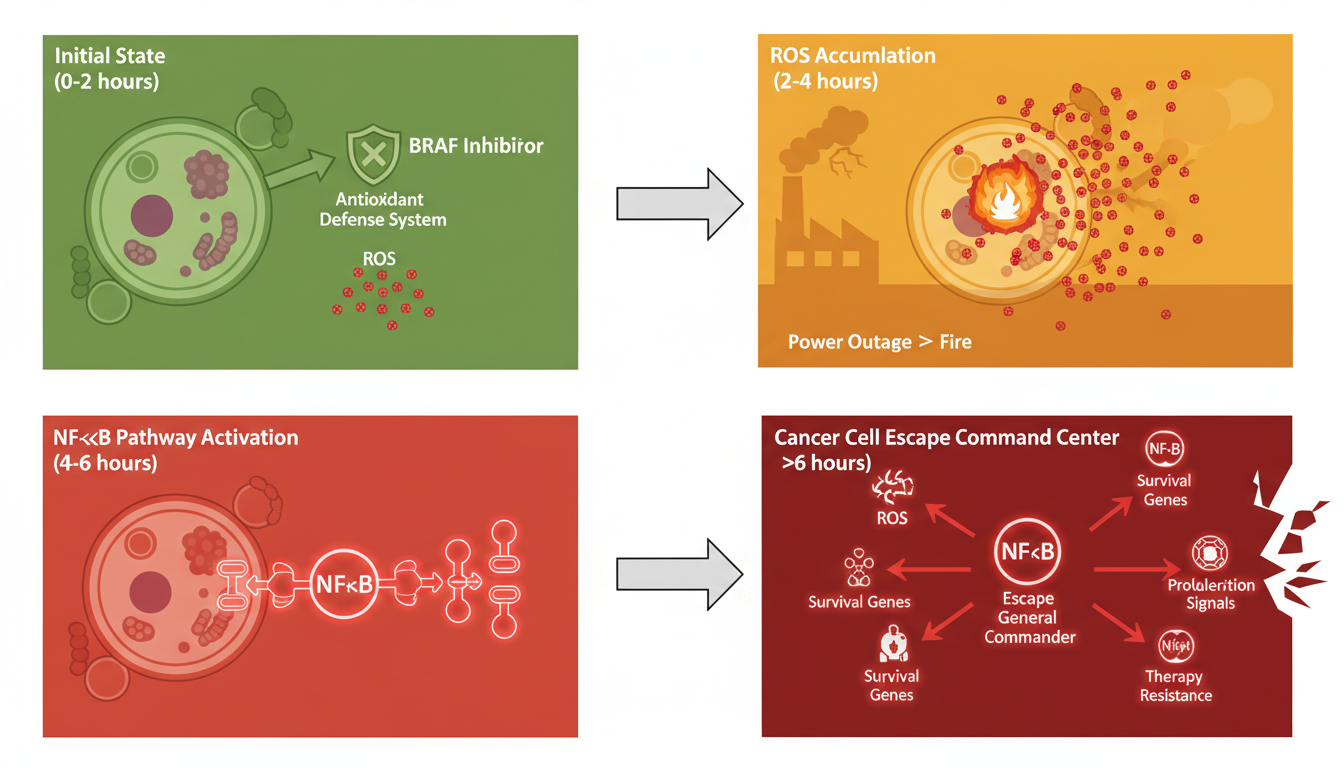
活化的NF-κB会招募KDM5B和HDAC1等表观遗传修饰酶,就像带着一群装修工冲进细胞核,开始「改装修饰」染色质:它们把维持黑色素细胞身份的关键基因(比如SOX10、MITF)的开关给焊死了,同时打开了原始干细胞基因的开关。
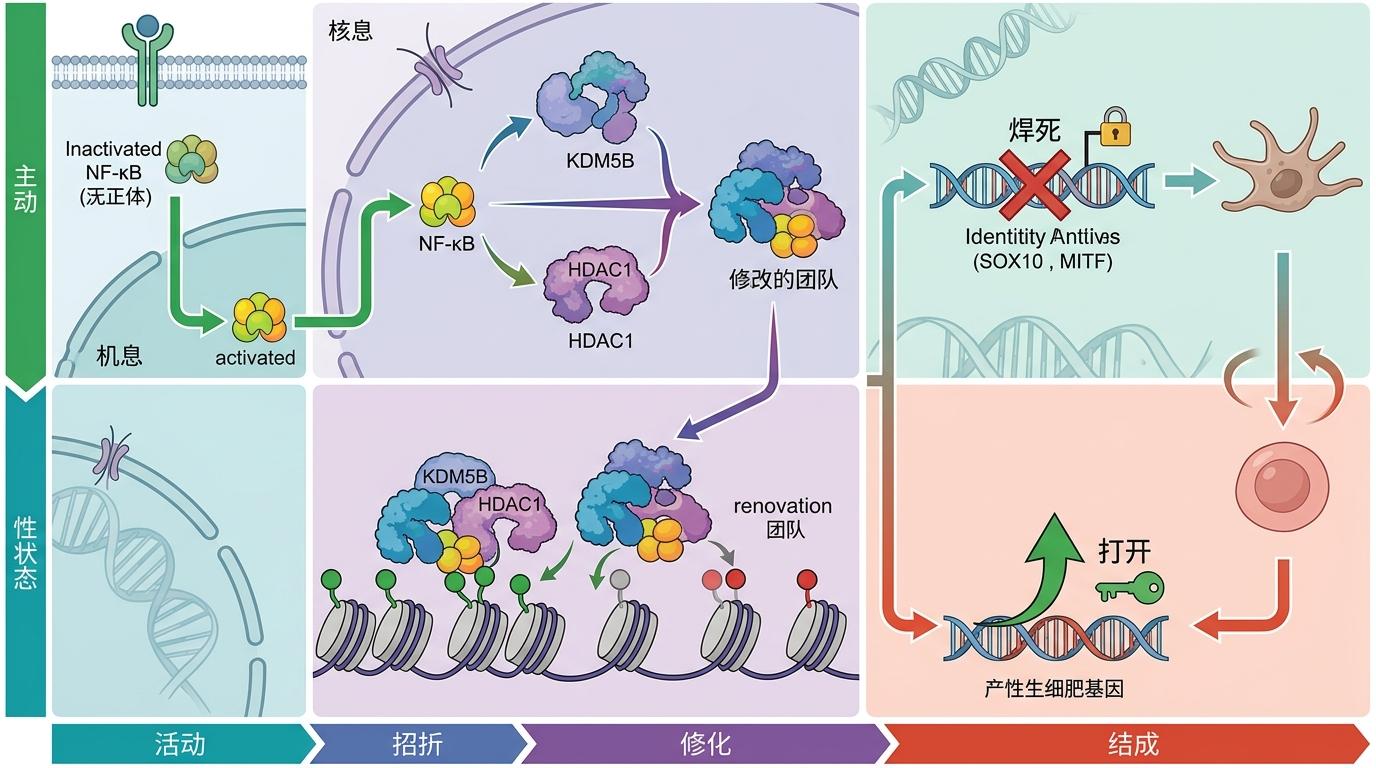
短短几天内,这些癌细胞就完成了去分化:丢掉黑色素细胞的所有特征,变成了一群没有固定职业、增殖缓慢但抗造能力极强的「流浪者」——也就是药物耐受持久态(DTP)。它们不会被靶向药杀死,只是暂时潜伏着,为后续攒出真正的遗传性耐药突变争取时间。
研究团队还发现,癌细胞的这次逃生不是临时抱佛脚,而是沿着一条精准规划好的「滞回」轨迹在走——就像你从家去公司走了一条路,下班回家却走了另一条,不会原路返回。
这条轨迹由两组紧密耦合的连续转录波驱动:第一波是应急反应,快速激活NF-κB通路;第二波是身份改造,启动去分化程序。更可怕的是,这次改造留下了「分子记忆」——哪怕停药,癌细胞也不会变回原来的黑色素细胞,而是会保留耐药相关的表观遗传印记。就像流浪者习惯了流浪生活,哪怕给了他原来的工作,也再也回不去了。
他们在黑色素瘤细胞系、小鼠模型甚至患者活检样本里都验证了这个过程:只要用BRAF抑制剂,就会快速诱导癌细胞去分化,获得耐药能力。更让人警惕的是,这个机制不是黑色素瘤独有——在EGFR突变肺癌、BRAF突变结肠癌里,氧化应激激活NF-κB通路,都是癌细胞进入药物耐受持久态的通用程序。
过去我们对付耐药的思路是「亡羊补牢」:等癌细胞耐药了,再换另一种靶向药。但这次研究彻底推翻了这个逻辑——癌细胞的逃生门,在我们吃药的第一天就已经打开了。
研究团队提出了新的治疗方向:与其等耐药后换药,不如在治疗初期就把逃生门堵上。他们做了实验:把BRAF靶向药和NF-κB通路抑制剂、表观遗传修饰药物联合使用,能显著增强抗肿瘤效果,甚至在多种癌症模型里都能阻断癌细胞的早期逃逸。
比如联合HDAC抑制剂,就能阻止NF-κB招募的「装修工」修改染色质,让癌细胞没法完成去分化;联合KDM5抑制剂,就能重新激活那些被沉默的分化基因,让癌细胞没法变成「流浪者」。
当然,这个策略还处于临床前阶段,还有很多问题要解决:比如如何精准控制药物剂量,避免过度抑制NF-κB带来的副作用;如何针对不同患者的癌细胞异质性,定制联合方案。但至少,我们终于从「被动等待耐药」,变成了「主动阻断逃生」。
过去我们总把癌细胞当成需要被消灭的「敌人」,以为它们只会在药物压力下慢慢进化出耐药突变。但这次研究让我们看到,癌细胞比我们想象的更狡猾——它们有提前规划的逃生程序,有能留下记忆的身份改造,甚至能跨癌种通用同一套逃生逻辑。
抗癌的本质,是和癌细胞的「时间赛跑」。当我们终于看清了它们在几小时内就启动的逃生计划,抗癌的战场就从「耐药之后」,提前到了「治疗之初」。未来的癌症治疗,或许不再是一次次换药的拉锯战,而是在癌细胞刚要逃跑时,就把逃生的门牢牢关上。
点击充电,成为大圆镜下一个视频选题!