对抗知识焦虑,从看懂这条开始
App 下载
克罗恩病新元凶?肠道噬菌体操控炎症的秘密被揭开
慢性炎症|肠道微生物|肠道噬菌体|克罗恩病|感染性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
慢性炎症|肠道微生物|肠道噬菌体|克罗恩病|感染性疾病|医学健康
人体肠道,宛如一个生机勃勃却又暗流涌动的微缩星球。数以万亿计的微生物在这里共生,构成了一个复杂而精密的生态系统。然而,当这个星球的秩序被打破,一场旷日持久的“内战”便可能爆发。克罗恩病(Crohn's disease),就是这样一场发生在肠道黏膜的慢性炎症战争,患者饱受腹痛、腹泻之苦,其病因复杂、炎症程度因人而异,长期以来如同一团迷雾,困扰着医学界。
科学家们一直在寻找这场战争的“幕后黑手”。过去,目光主要聚焦在细菌和免疫系统的失衡上。但现在,一个新的、曾被忽视的角色正从阴影中走出,它就是肠道噬菌体——一种专门感染细菌的病毒。作为肠道微生物世界中的“暗物质”,噬菌体的数量是细菌的十倍之多,它们究竟是和平的维护者,还是混乱的煽动者?这个问题的答案,或许正是解开克罗恩病炎症异质性之谜的关键。
近日,中山大学附属第六医院的左涛研究员团队在国际顶尖期刊《细胞·宿主与微生物》上发表了一项突破性研究,首次为肠道噬菌体在克罗恩病中的角色提供了清晰的画像。这项研究不再将噬菌体视为一个模糊的整体,而是通过对大量临床样本的分析,首次鉴定出两种截然不同的肠道黏膜“噬菌体肠型”,并将其命名为E1型和E2型。
这两种肠型,如同两种截然不同的军队部署,决定了肠道战场的局势。研究发现,E1型在健康人群中更为常见,代表着一种相对和平的微生态环境。而E2肠型的噬菌体多样性更高,其组成也与E1型显著不同,并且在克罗恩病患者中比例明显偏高。这一发现立刻将嫌疑指向了E2肠型——它是否就是点燃更猛烈炎症战火的那个火种?
为了验证这一猜想,研究团队进行了一项关键的噬菌体移植实验。他们将从人类肠道中分离的E1和E2型噬菌体分别移植到实验小鼠体内。结果惊人地一致:接受了E2噬菌体移植的小鼠,在后续的肠炎诱导模型中,表现出远比E1组更严重的炎症症状——体重下降更剧烈、结肠显著缩短、组织损伤触目惊心。这为E2肠型的“促炎”特性提供了强有力的因果证据。
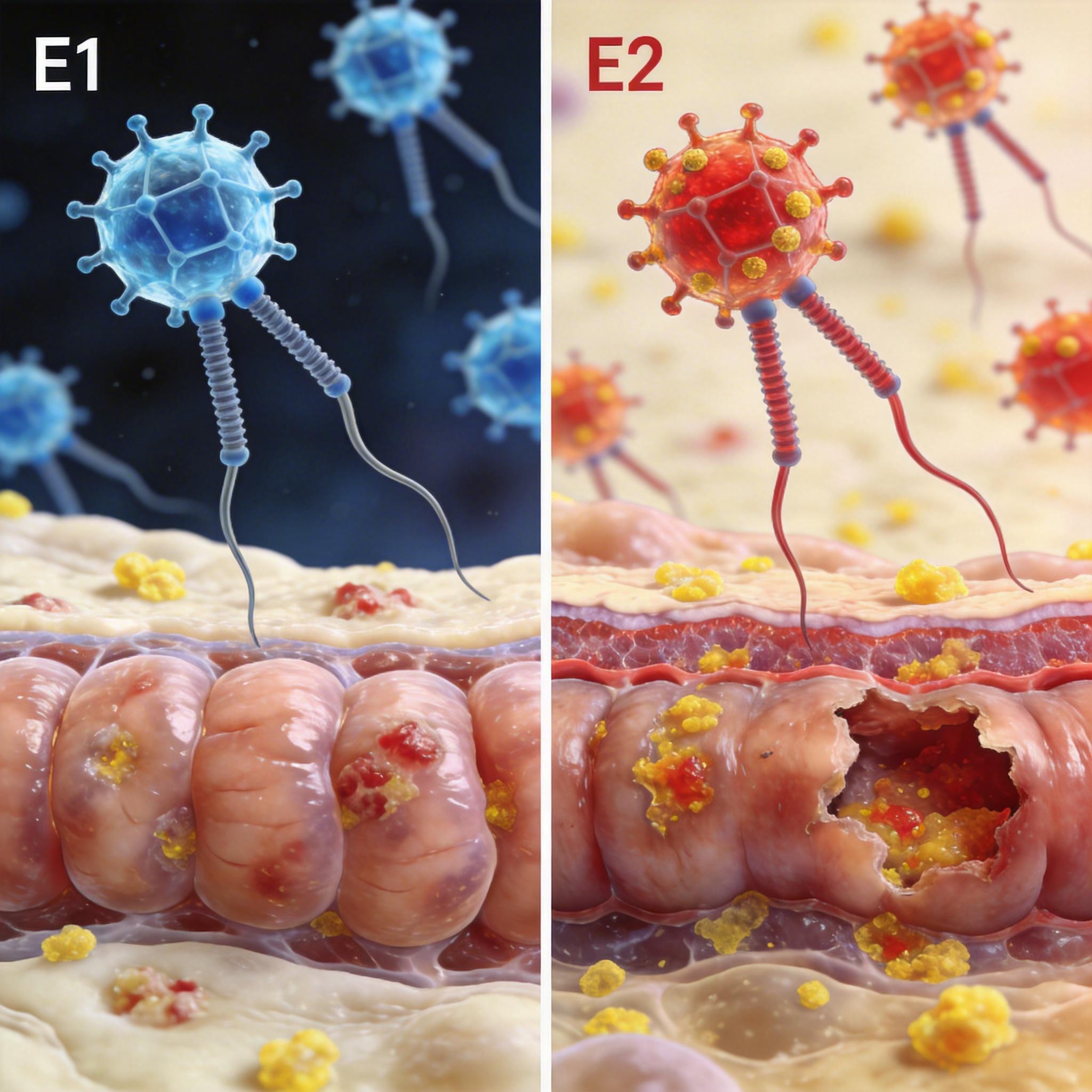
E2肠型究竟是如何煽动炎症的?左涛团队的深入探索,揭示了一场发生在微观世界里,涉及噬菌体、细菌和化学信使的“三国杀”。
研究人员在复杂的E2肠型中,锁定了一个关键的噬菌体角色——Wulfhauvirus。这个噬菌体并不直接攻击肠道细胞,而是选择性地感染一种名为多形拟杆菌(B. thetaiotaomicron)的肠道细菌。这并非传统的“捕食者-猎物”关系,而是一种更为狡猾的“溶源整合”。Wulfhauvirus像一名间谍,将自己的基因整合进宿主菌的基因组中,悄悄地改变着它的行为。
被“策反”的多形拟杆菌,开始大量分泌一种名为**鞘氨醇(sphingosine)的代谢物。鞘氨醇就像一个化学武器,它在肠道中弥散开来,精准打击另一种名为普通拟杆菌**(B. obeum)的有益共生菌。普通拟杆菌本是维护肠道和平的“卫士”,具有抗炎作用,但在鞘氨醇的攻击下,其数量锐减。
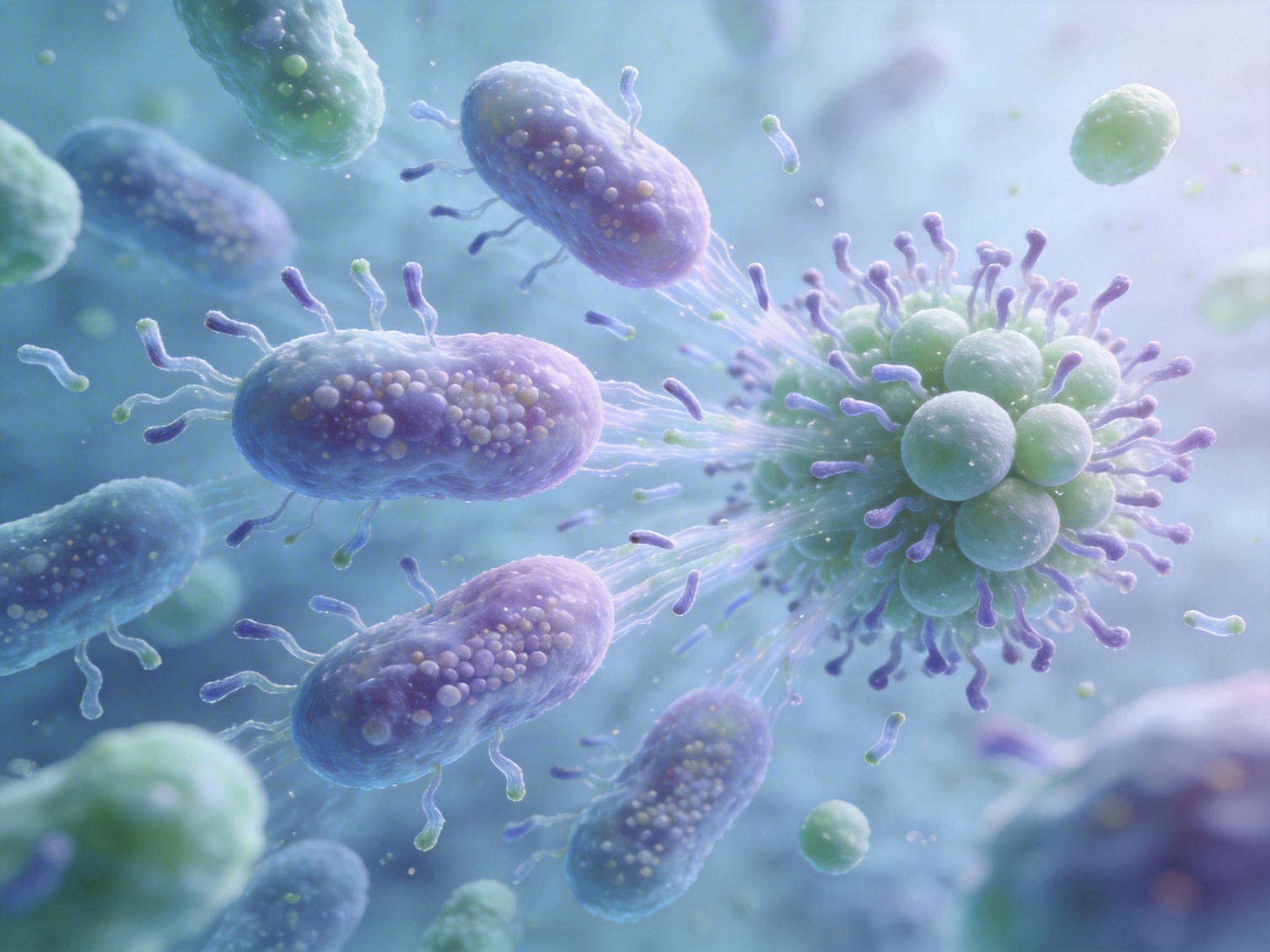
至此,一条完整的跨界级联调控链条浮出水面:“Wulfhauvirus噬菌体”通过调控“多形拟杆菌”,后者分泌“鞘氨醇”代谢物,进而抑制了“普通拟杆菌”,最终导致肠道屏障受损,炎症加剧。
这项研究的艺术化构想图生动地描绘了这一场景:在代表E1肠型的河流一侧,象征有益菌的仙鹤守护着郁郁葱葱的肠道稳态;而在代表E2肠型的对岸,由噬菌体操控的细菌化身为凶猛的老鹰,压制了仙鹤,导致万木凋零,一片炎症焦土。这正是克罗恩病患者体内正在上演的微观生态悲剧。
这项发现的深远意义在于,它彻底颠覆了我们对噬菌体作用的传统认知。过去,我们认为噬菌体主要通过裂解细菌(即杀死并吃掉它们)来调节菌群数量。而左涛团队的研究揭示了一种全新的、更为精妙的调控模式:温和噬菌体可以通过改变宿主细菌的代谢功能,间接重塑整个肠道菌群的生态格局。
这不再是简单的“捕食”,而是一种“操控”。噬菌体不再仅仅是猎手,更像是能够改写游戏规则的幕后玩家。它们通过影响细菌的“化工厂”(代谢通路),生产出特定的化学信号,从而在更广泛的尺度上影响菌群间的相互作用和肠道健康。这一“噬菌体-细菌-代谢物-肠道”的跨界调控网络,为我们理解复杂的肠道微生态系统提供了一个全新的、多维度的视角。
对于饱受折磨的克罗恩病患者而言,这一基础科学的突破带来了精准治疗的曙光。既然我们已经找到了导致炎症异质性的关键调控轴,那么就有可能通过干预这个轴上的任何一个环节,来熄灭炎症的火焰。
这项研究为克罗恩病的治疗提供了多个潜在的新靶点:
这些基于微生态的精准干预策略,有望摆脱传统免疫抑制剂“杀敌一千,自损八百”的困境,实现对肠道炎症的源头治理。通过鉴定患者的“噬菌体肠型”,未来或许可以实现真正的个性化治疗,为不同炎症表型的患者量身定制干预方案。
当然,从实验室的重大发现到临床的广泛应用,依然有很长的路要走。首先,当前的研究成果主要基于小鼠模型,其在人体中的有效性和安全性仍需通过严格的临床试验来验证。其次,肠道微生态系统极其复杂,任何干预都可能引发意想不到的连锁反应,如何精准调控而不引发新的失衡,是未来研究必须面对的挑战。
尽管如此,这项研究无疑为我们打开了一扇全新的大门。它所建立的“噬菌体肠型-功能验证-机制解析”的研究框架,不仅为克罗恩病的研究提供了范本,也为其他与微生物组相关的复杂疾病(如糖尿病、肥胖甚至神经系统疾病)的研究提供了宝贵借鉴。
我们有理由相信,随着对肠道“暗物质”——噬菌体的探索不断深入,人类将获得更多调控自身微生态的强大工具。那一天,我们或许不仅能预测克罗恩病的炎症风暴,更能从容地平息它,让肠道这个微缩星球重归和平与健康。