对抗知识焦虑,从看懂这条开始
App 下载
血管里的机械感受器,成了治腿疾的新靶点
侧支血管生成|外周动脉疾病|压力传感器|血管内皮细胞|GPR68蛋白|心脑血管疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
侧支血管生成|外周动脉疾病|压力传感器|血管内皮细胞|GPR68蛋白|心脑血管疾病|医学健康
当腿上的动脉被斑块堵死,有些人能靠身体自己长出新血管续命,有些人却只能面临截肢——这之间的差距,可能就藏在一个不起眼的分子里。中山大学的研究团队最近发现,血管内皮细胞上的GPR68蛋白,就像血管里的「压力传感器」,能精准捕捉血流变化的信号,召唤免疫细胞来帮忙打通侧支血管。如果把这个传感器关掉,小鼠腿上的缺血组织会快速坏死;而激活它,就能让血流恢复速度大幅提升。这个发现,给全球1.14亿外周动脉疾病患者,带来了新的希望。
你可以把外周动脉疾病想象成家里的水管堵了:主管道不通,只能靠细窄的备用小管维持供水。而动脉生成——也就是身体长出新侧支血管的过程——就像把备用小管拓宽成新的主管道。这个过程的启动信号,是血流突然改变时产生的剪切力,也就是血液在血管壁上蹭出的「摩擦力」。
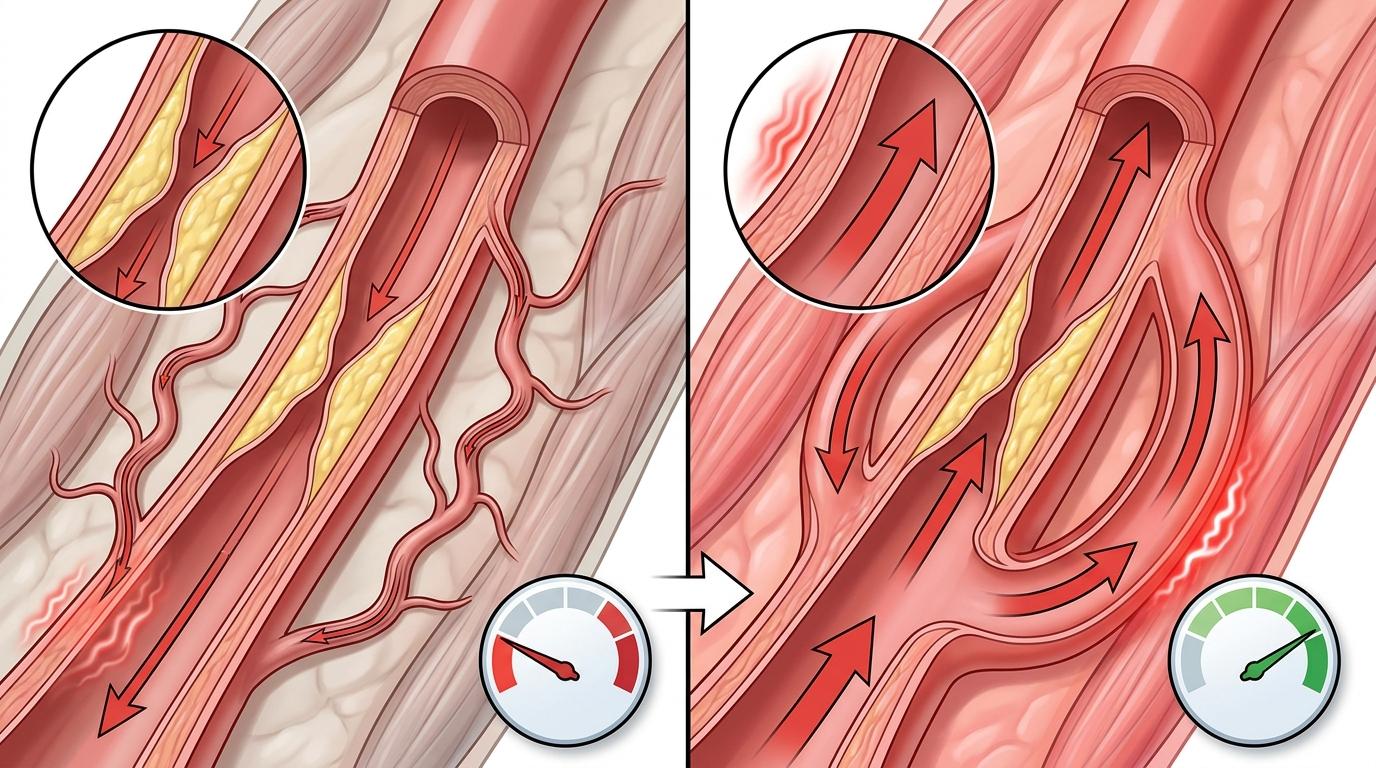
过去科学家们找了很久,都没找到血管内皮细胞上感知这个摩擦力的关键分子。直到这次,研究团队通过基因敲除小鼠实验才确认:GPR68就是那个「开关」。它是一种G蛋白偶联受体,专门长在小动脉的内皮细胞上,既能感知血流剪切力,还能对缺血导致的酸性环境敏感。
当主血管堵塞,侧支血管里的血流突然变快,剪切力骤增,GPR68就会被激活,随后触发一系列连锁反应:内皮细胞开始分泌趋化因子和黏附分子,像贴「寻人启事」一样召唤血液里的单核细胞。这些单核细胞跑到血管壁上变成巨噬细胞,分泌生长因子,一点点把侧支血管撑粗、打通。
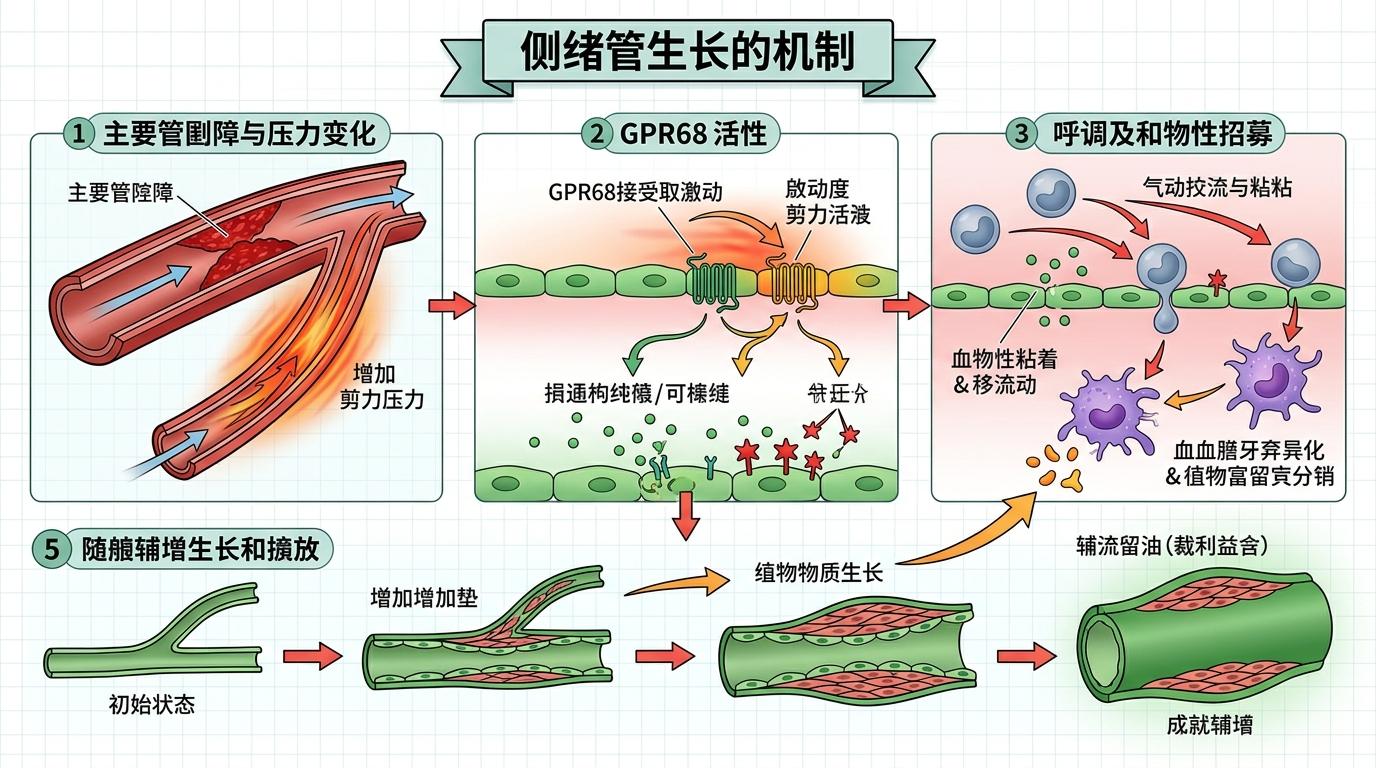
研究团队做了一组对比实验:给两组小鼠都做了腿动脉结扎,制造缺血模型,其中一组是内皮细胞特异性敲除GPR68的小鼠,另一组是正常小鼠。结果很明显:
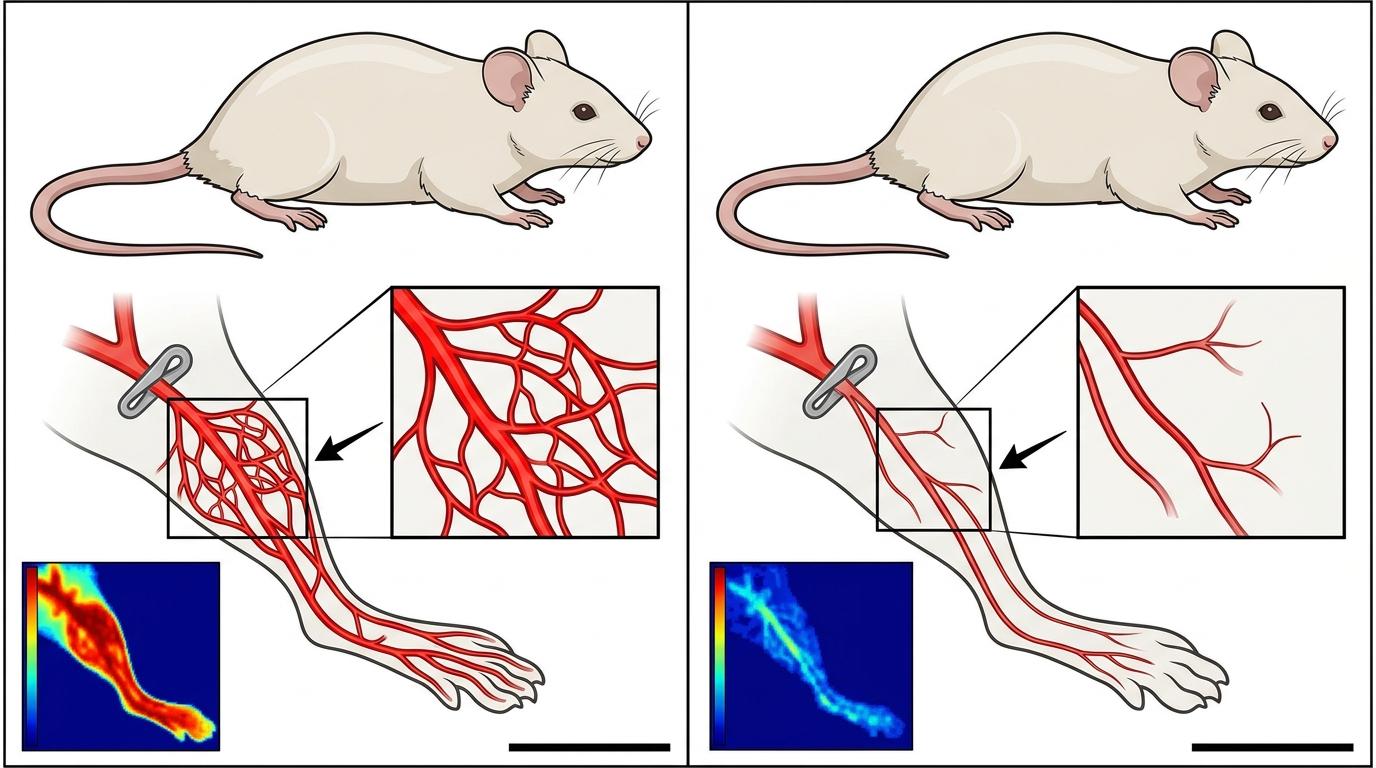
既然关掉开关会出问题,那打开开关呢?研究团队用GPR68的激动剂Compound 71做了验证:体外实验中,它能让单核细胞黏附内皮细胞的能力提升1.6倍;体内实验里,注射了Compound 71的小鼠,血流恢复速度明显加快,肌肉损伤也减轻了70%。这种激活方式,相当于给血管的自救系统踩了一脚油门。
不过,这个新靶点要真正用到患者身上,还有几个问题得解决。
首先是特异性。GPR68不仅在血管内皮细胞上表达,在脑、骨骼、免疫细胞里也有分布,激活它会不会带来其他副作用?目前的动物实验显示,Compound 71对GPR68的选择性很高,暂时没发现明显毒性,但还需要更长期的安全性验证。
其次是个体差异。人类全表型组关联研究显示,GPR68基因附近的变异会增加外周动脉疾病的发病风险,这意味着不同患者的GPR68活性可能天生有差异,用药剂量和效果也会不同。未来可能需要结合基因检测,实现个体化治疗。
最后是药物优化。目前的Compound 71虽然效果不错,但还需要进一步优化结构,提升生物利用度和体内稳定性,才能真正走向临床。
从血管里的分子信号,到病床前的治疗方案,这中间隔着无数次实验和验证,但这次的发现,已经为外周动脉疾病的治疗打开了一扇新门。过去我们治疗血管堵塞,要么通血管,要么搭桥,都是「外力介入」;而GPR68靶点的意义,在于激活身体本身的自救能力——这是一种更精准、更温和的治疗思路。
机械信号感知分子的发现,让我们对血管的理解又深了一层:血管不只是输送血液的管道,更是一个能感知、能调节、能自救的智能系统。「激活内在自救,比外力介入更持久」,这或许是这个研究带给我们最有价值的启示。