对抗知识焦虑,从看懂这条开始
App 下载
颠覆认知:神经元“门禁”失灵或为AD发病起点
大脑物质交换|膜相关周期性骨架|神经元内吞|阿尔茨海默病|神经退行性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
大脑物质交换|膜相关周期性骨架|神经元内吞|阿尔茨海默病|神经退行性疾病|医学健康
我们的一千亿个神经元,如同一个个戒备森严的微型城邦,时刻都在与外界进行着物质交换。这个过程被称为“内吞”,相当于城邦的“海关”,负责精准地放行信号分子、营养物质,同时回收废旧的膜碎片。这是学习记忆与神经功能维护的基石。然而,任何一个高效的系统都暗藏风险。如果“海关”失控,让不该进入的“货物”蒙混过关,一场灾难便可能悄然酝酿。多年来,科学家们一直在寻找阿尔茨海默病(AD)的源头,而一场关于大脑“海关”的危机,正将我们的视线引向一个意想不到的角落。
长期以来,神经元细胞膜下方一层名为**膜相关周期性骨架(Membrane-associated Periodic Skeleton, MPS)**的结构,被认为是支撑细胞形态的静态“脚手架”。它由肌动蛋白丝构成的环和血影蛋白四聚体连接而成,形成间距约190纳米的规整“防护网”,覆盖在神经元的轴突和树突之下。
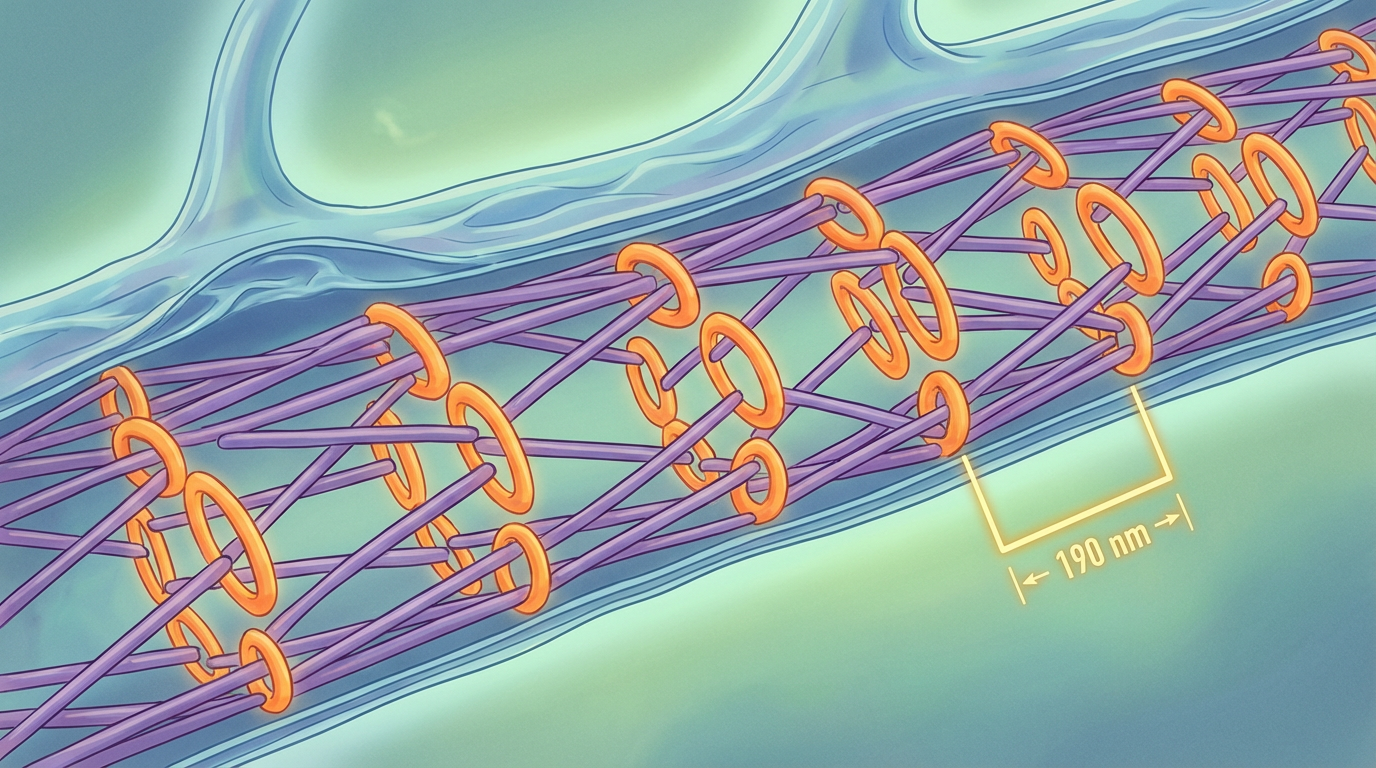
然而,宾夕法尼亚州立大学的科学家们借助STORM、SIM等超分辨率显微镜技术,得以在纳米尺度下窥探这层结构的真实面目。发表在《Science Advances》上的研究彻底颠覆了传统认知:MPS远非一个被动的“脚手架”,而是一道动态可调的“智能门禁”,是神经元内吞活动的最高指挥官。
研究团队追踪了神经元中四种核心的内吞通路,包括网格蛋白介导内吞(CME)和快速内吞蛋白介导内吞(FEME)等。结果惊人地一致:几乎所有的内吞活动,都被严格限制在MPS晶格之间的“空白地带”,仿佛所有进港的船只都必须通过指定的狭窄航道。这表明,MPS本身就是一道物理屏障,是内吞活动的天然“刹车”。
这道“门禁”的智能之处,在于它并非一成不变,而是拥有“物理阻挡+信号响应解体”的双重密码。
物理阻挡:这是它的默认状态。规整的MPS晶格结构像一张致密的渔网,物理性地限制了细胞膜的大幅度形变,从而抑制了内吞囊泡的形成。为了验证这一点,研究人员通过shRNA技术敲低了关键蛋白βII-血影蛋白,破坏了MPS的完整性。结果,神经元的基础内吞活性显著增强,四种内吞通路的效率均大幅提升。这有力地证明了MPS是调控内吞的核心“关卡”。
信号响应解体:更令人意外的是,这道“门禁”还能主动“开门”。当神经元接收到强烈信号,需要大量“进食”时,会激活细胞外信号调节激酶(ERK)信号通路。这条通路像一个指令官,会唤醒细胞内的两把“分子剪刀”——钙蛋白酶(calpain)和半胱天冬酶(caspase)。这两把剪刀会精准地切割构成MPS的血影蛋白,导致MPS局部解体,“空白地带”扩大,为内吞活动敞开大门。
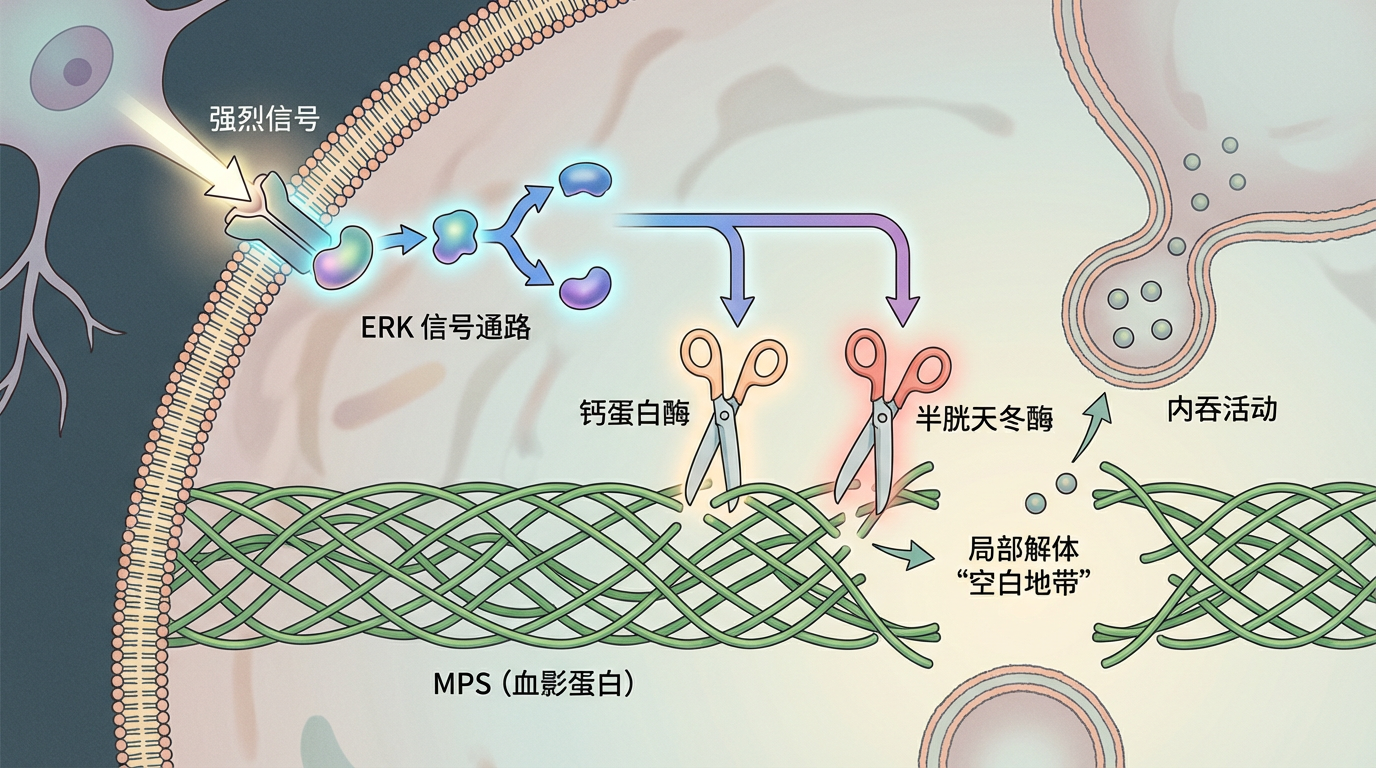
这就形成了一个高效的正反馈循环:内吞活动激活信号 → MPS解体 → 内吞更顺畅 → 信号进一步激活。这套精妙机制确保了神经元能够根据生理需求,快速、高效地完成物质交换,不多也不少。
这套高效机制的B面,却隐藏着通往阿尔茨海默病的致命风险。研究团队发现,当MPS的完整性因衰老或病理刺激受损时,这道智能门禁便会“失守”。
此时,一种名为淀粉样前体蛋白(APP)的分子会趁虚而入。正常情况下,MPS会限制APP的内吞数量,防止其过量进入细胞。然而,当“门禁”失灵,APP便会如潮水般涌入神经元内部。在细胞内,过量的APP会被β-分泌酶和γ-分泌酶依次切割,生成大量具有神经毒性的Aβ₄₂片段。
这些毒性片段在细胞内堆积,会激活**胱天蛋白酶3(caspase-3)**,这是一种执行细胞凋亡(程序性死亡)的关键蛋白。研究数据显示,MPS破坏越严重,Aβ₄₂的积累和凋亡信号就越强,形成了一个无法逆转的死亡螺旋。
这一发现,石破天惊地串联起了一个困扰学界十年的谜题。此前,科学家们早已在衰老的神经元和AD患者的尸检样本中观察到MPS的断裂和缺失,但一直将其视为细胞衰败的“结果”。而这项新研究证实,MPS的失灵,很可能是AD病理进程的“起点”。它在Aβ斑块形成之前,就提前为毒性蛋白打开了“入侵之门”,启动了Aβ₄₂生成的恶性循环。我们对AD发病机制的理解,正从关注下游的“斑块清理”,转向追溯上游的“门禁失修”。
阿尔茨海默病之所以被称为“沉默的杀手”,核心在于其漫长的无症状病理进程。当患者出现明显的认知障碍时,大脑中往往已是Aβ斑块遍布,大量神经元死亡,治疗为时已晚。
这项研究的最大意义,在于揭示了一个极具潜力的AD早期干预靶点。MPS的完整性,成为了一个比Aβ斑块更早出现的“预警信号”。这意味着,我们或许不再需要等到“城墙”(神经元)倒塌后才去清理“废墟”(Aβ斑块),而是可以在“城门”(MPS)出现裂缝时就及时修复。
未来的治疗策略充满了新的想象空间:
从一个静态的细胞骨架,到一个动态的智能门禁,再到一个关乎生死的疾病开关,我们对MPS的认知之旅,恰恰反映了生命科学的魅力——在最微观的结构中,往往隐藏着最深刻的生命法则与疾病奥秘。修复这道大脑的“智能门禁”,可能就是我们撬动阿尔茨海默病这座冰山的下一个支点。