对抗知识焦虑,从看懂这条开始
App 下载
mRNA的隐藏指令:化学修饰m¹Ψ竟能调控蛋白生产速度?
核糖体翻译|蛋白质合成调控|m¹Ψ|mRNA化学修饰|分子细胞生物学|生命科学
生命工厂的变速齿轮
在细胞这个精密无比的生命工厂里,蛋白质的生产遵循着一条经典的流水线法则:DNA作为总设计蓝图,被转录成信使RNA(mRNA)这份移动作业指导书,最终由核糖体这位“工匠”读取并组装成蛋白质。长久以来,我们认为这份指导书上的信息是固定不变的,核糖体只需匀速读取即可。然而,如果这份指导书上,除了可见的碱基序列,还用“隐形墨水”标注了特殊指令,告诉工匠在某些步骤“减速慢行”,甚至“稍作停顿”呢?
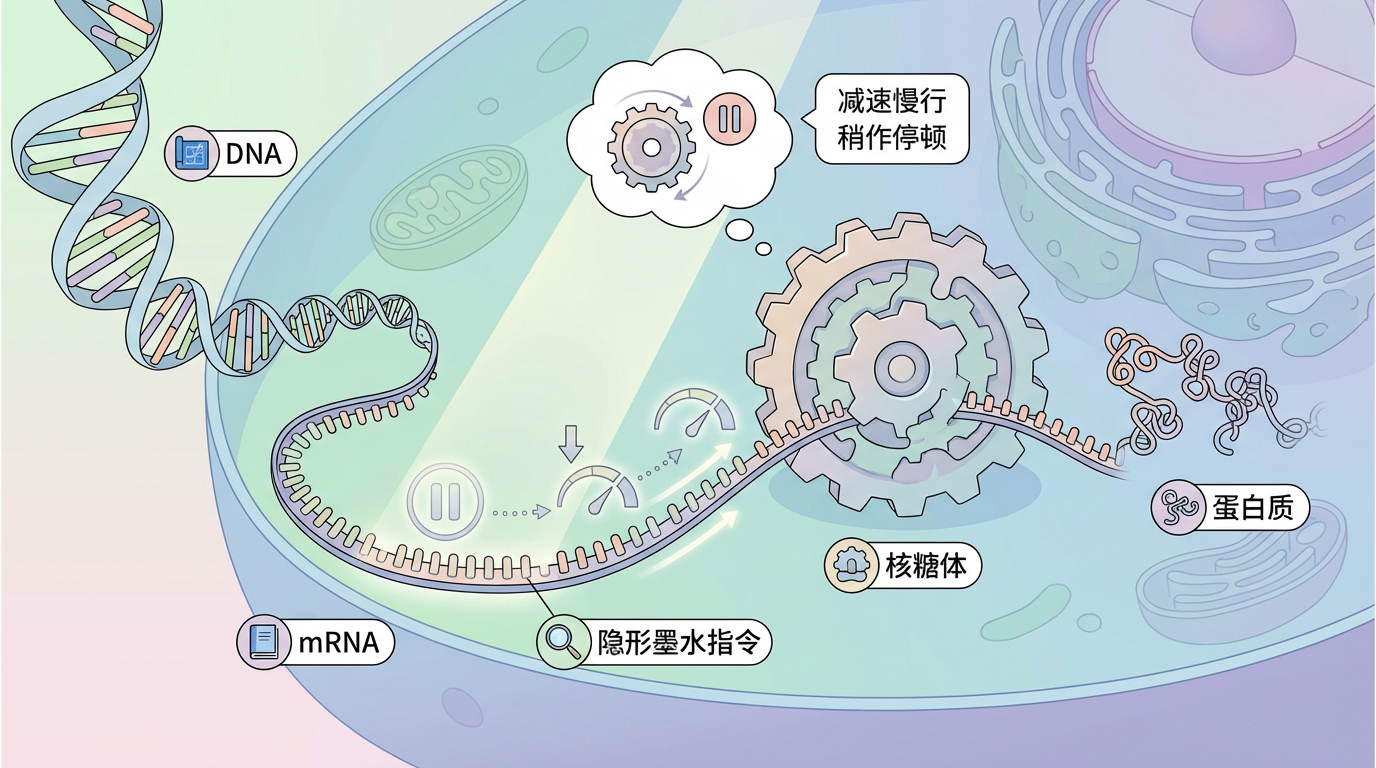
这并非科幻,而是正在上演的生物学革命。一种名为N¹-甲基假尿苷(m¹Ψ)的RNA化学修饰,正是这样一种“隐形墨水”。它因在新冠mRNA疫苗中的关键作用而声名鹊起,我们曾以为它的角色是“伪装者”和“加固剂”——降低免疫原性以躲避免疫系统攻击,并提升mRNA分子的稳定性。但一个更深层次的问题萦绕在科学家心头:m¹Ψ的魔力,仅此而已吗?它会不会直接与生产蛋白质的工匠——核糖体——对话,从而主动调控生产过程的节奏?
破译“隐形墨水”:一场颠覆认知的实验
最近,以色列魏茨曼科学研究院的Noam Stern-Ginossar团队在顶尖期刊《Nature》上发表的研究,为这个问题提供了决定性的答案。他们设计了一场堪称“分子生物学控制变量法典范”的实验,彻底剥离了免疫反应和mRNA稳定性这两个“干扰项”。
研究团队构建了一系列mRNA分子,它们的碱基序列、长度完全一致,唯一的区别在于:一部分mRNA在特定位点将天然的尿苷(U)替换为了m¹Ψ修饰。随后,他们将这些mRNA放入一个高度纯化的体外翻译系统中,这里没有免疫细胞,分子的稳定性也被严格控制。如此一来,任何蛋白质产量的差异,都只能归因于m¹Ψ本身对翻译过程的直接影响。
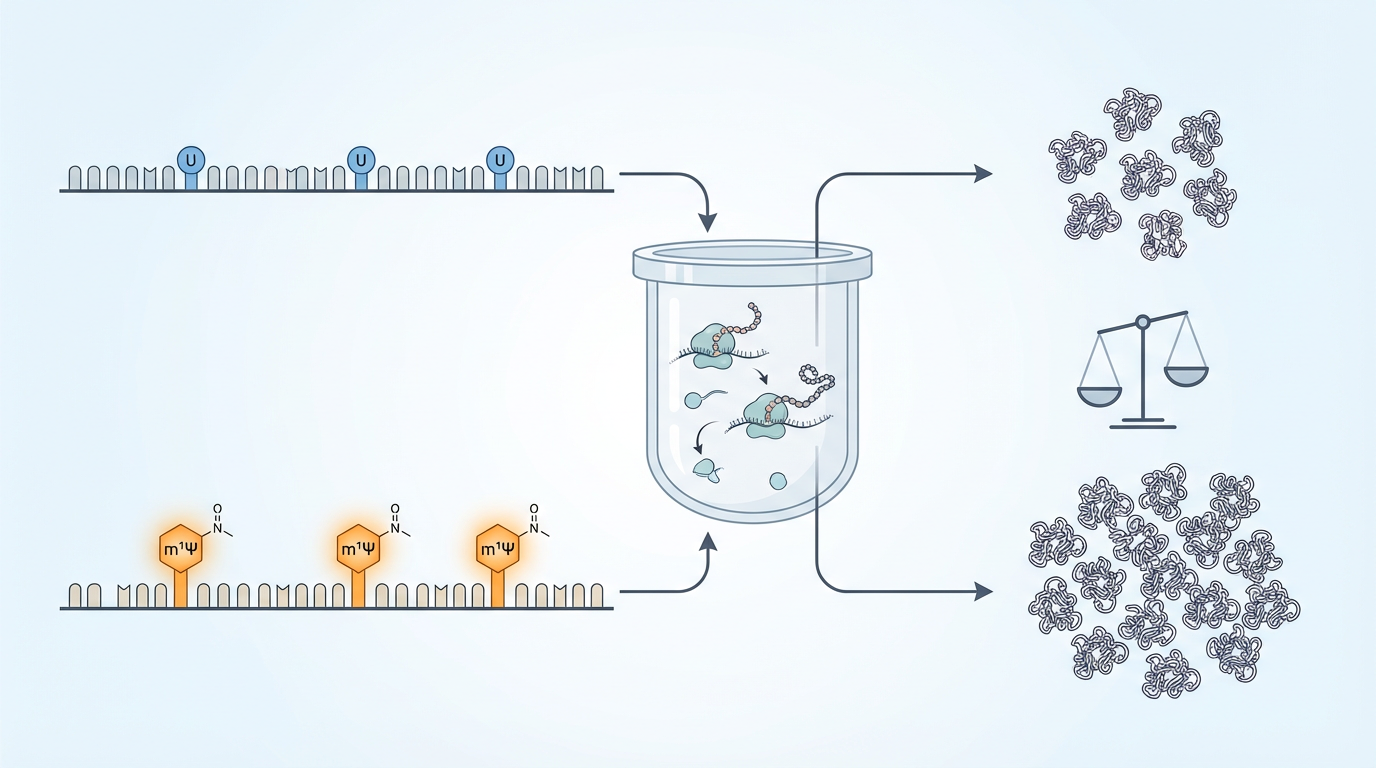
借助亚密码子分辨率的核糖体测序技术,他们以前所未有的精度“直播”了核糖体在mRNA链条上移动的全过程。结果令人震惊:
- m¹Ψ是翻译路上的“减速带”:在含有m¹Ψ的位点,核糖体的移动速度确实变慢了,造成了局部的“交通拥堵”。这种减速效应并非随机发生,而是在特定的序列背景下尤其明显,特别是在那些本就不太“顺口”的非最佳密码子区域。
- 核糖体能“感知”修饰:这直接证明了,核糖体这位工匠,能够直接“触摸”并“感知”到m¹Ψ这种化学修饰,并据此调整自己的工作节奏。m¹Ψ不再是消极的背景板,而是主动参与翻译调控的功能性信号。
这项发现彻底改变了游戏规则。它揭示了基因表达调控的一个全新层次:翻译动力学调控。原来,生命蓝图的信息深度,远超我们的想象。mRNA不仅编码了“生产什么”,还通过化学修饰编码了“如何生产”——生产的快慢、节奏与韵律。
暗影中的双刃剑:移码风险与安全警示
然而,正如许多重大科学发现一样,m¹Ψ对翻译节奏的调控也呈现出“双刃剑”的特性。就在不久前,剑桥大学的另一项《Nature》研究揭示了这枚硬币的另一面。
研究发现,m¹Ψ在减缓核糖体速度的同时,有时会让这位“工匠”在“减速带”上不慎“打滑”——发生**+1核糖体移码**。这意味着核糖体在读取密码子时会向前错移一个碱基,导致后续的氨基酸序列完全错乱,从而产生出乎意料的“脱靶”蛋白。据估计,这种情况的发生率约为10%。
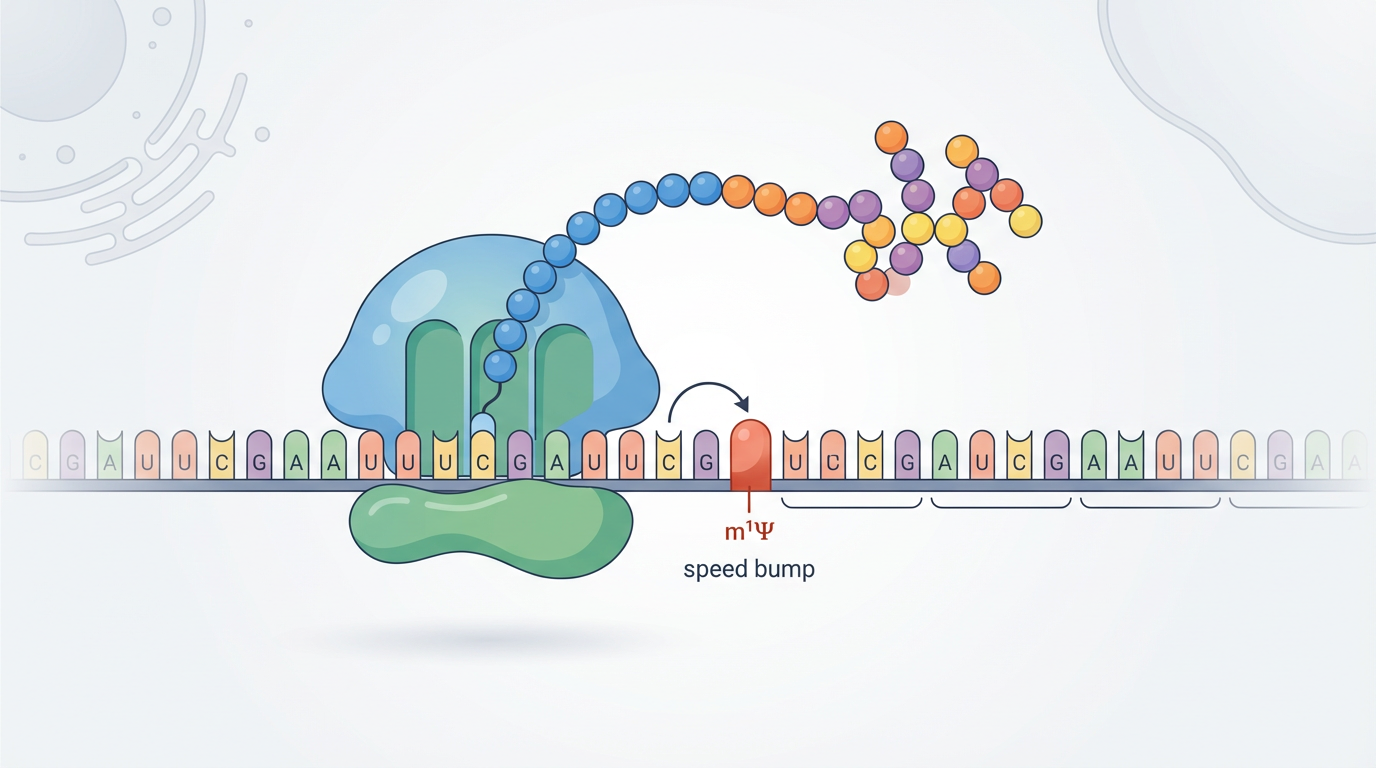
更关键的是,研究人员在接种了mRNA新冠疫苗的人体样本中,检测到了由这种移码错误产生的蛋白质,以及针对这些“不速之客”的免疫反应。虽然目前没有证据表明这些脱靶蛋白会造成严重的健康问题,但这一发现为mRNA药物的安全性敲响了警钟。它解释了为何mRNA疫苗的免疫副反应有时会高于其他类型的疫苗,并强调了在药物设计中必须考虑翻译保真度的重要性。
精准编程的蓝图:通往未来医药的新航道
m¹Ψ的“双面性”非但没有给mRNA技术蒙上阴影,反而为其开启了一扇通往“精准编程”时代的大门。理解了其调控翻译动力学和引发移码的机制,科学家们便能化挑战为机遇。
- 优化蛋白质量与产量:对于一些结构复杂、需要时间精细折叠的蛋白质,我们可以通过在mRNA上策略性地布置m¹Ψ“减速带”,人为地让核糖体在关键节点放慢速度,给予新生肽链充分的折叠时间,从而提高功能性蛋白的产率和质量。
- 规避安全风险:针对移码风险,科学家可以利用密码子的简并性(即多个密码子可以编码同一种氨基酸),通过“同义密码子重编码”的策略,替换掉那些容易让核糖体“打滑”的序列。这相当于在设计图纸时,就提前铺设好“防滑路面”,在不改变最终蛋白质产品的前提下,大幅提升生产过程的安全性。
- AI赋能药物设计:结合人工智能算法(如RiboDecode、LinearDesign),研究人员可以开发出更智能的mRNA序列设计平台。这些平台不仅能优化序列以提高稳定性和表达量,还能整合翻译动力学的规则,预测并规避移码风险,为特定细胞类型和治疗需求“量身定制”最优的mRNA药物。
从癌症疫苗、罕见病基因替代疗法,到再生医学,这种对蛋白质生产节奏的精准控制能力,将使mRNA技术成为驱动精准医疗发展的新引擎。
未来的地平线:解码完整的“表观转录组”语言
m¹Ψ的故事只是冰山一角。在细胞的RNA世界里,存在着超过170种不同的化学修饰,它们共同构成了一个复杂的信息网络——“表观转录组”。m⁶A、m⁵C、ac⁴C……每一种修饰都可能是一种独特的“标点符号”或“语法规则”,共同谱写着蛋白质合成的交响乐。
我们面临的挑战是巨大的。如何用纳米孔直接测序等先进技术,在单分子、单细胞水平上实时读取并解码这些复杂的修饰语言?不同修饰之间是否存在协同或拮抗的“语法规则”?由移码产生的微量脱靶蛋白,其长期的生物学影响究竟是什么?
回答这些问题,需要我们不断磨砺技术的“眼睛”,深入探索这个隐藏在经典遗传密码之下的新世界。我们正从仅仅阅读生命之书的文字,过渡到理解其精妙的排版、标点和韵律。每一次对RNA修饰的深入洞察,都让我们离真正掌握生命语言、随心所欲地编写治疗程序的目标更近一步。这场由m¹Ψ开启的认知革命,预示着一个我们可以通过调控翻译节律来精准治疗疾病的医学新纪元的到来。