对抗知识焦虑,从看懂这条开始
App 下载
小分子SK-129,能截停大脑的蛋白风暴
阿尔茨海默病|帕金森病|折叠体分子|α-突触核蛋白|SK-129|神经退行性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
阿尔茨海默病|帕金森病|折叠体分子|α-突触核蛋白|SK-129|神经退行性疾病|医学健康
当帕金森患者的手指开始不受控震颤,当阿尔茨海默病人认不出至亲,他们的大脑里正发生一场沉默的风暴——原本各司其职的神经元蛋白,像被打乱的积木般错误折叠、抱团聚集,一点点蛀空神经通路。过去几十年,我们只能给这场风暴递上止疼片,直到SK-129出现。它不是来缓解震颤或健忘的,它是来拆风暴中心的。
纽约大学阿布扎比分校和丹佛大学的团队,花了数年打磨出这颗小分子。它属于一种叫“折叠体”的人工合成分子——简单说,就是模仿蛋白质天然结构的“替身演员”,能精准钻进致病蛋白的关键结合位点。SK-129的目标是α-突触核蛋白(αS),这种蛋白的错误聚集是帕金森、路易体痴呆的核心病因。它像个尽职的“拆弹员”,死死攥住αS的N端关键序列,把它稳定在不会聚集的α-螺旋构象里,连带着还能拦住它和阿尔茨海默相关的tau蛋白“狼狈为奸”。
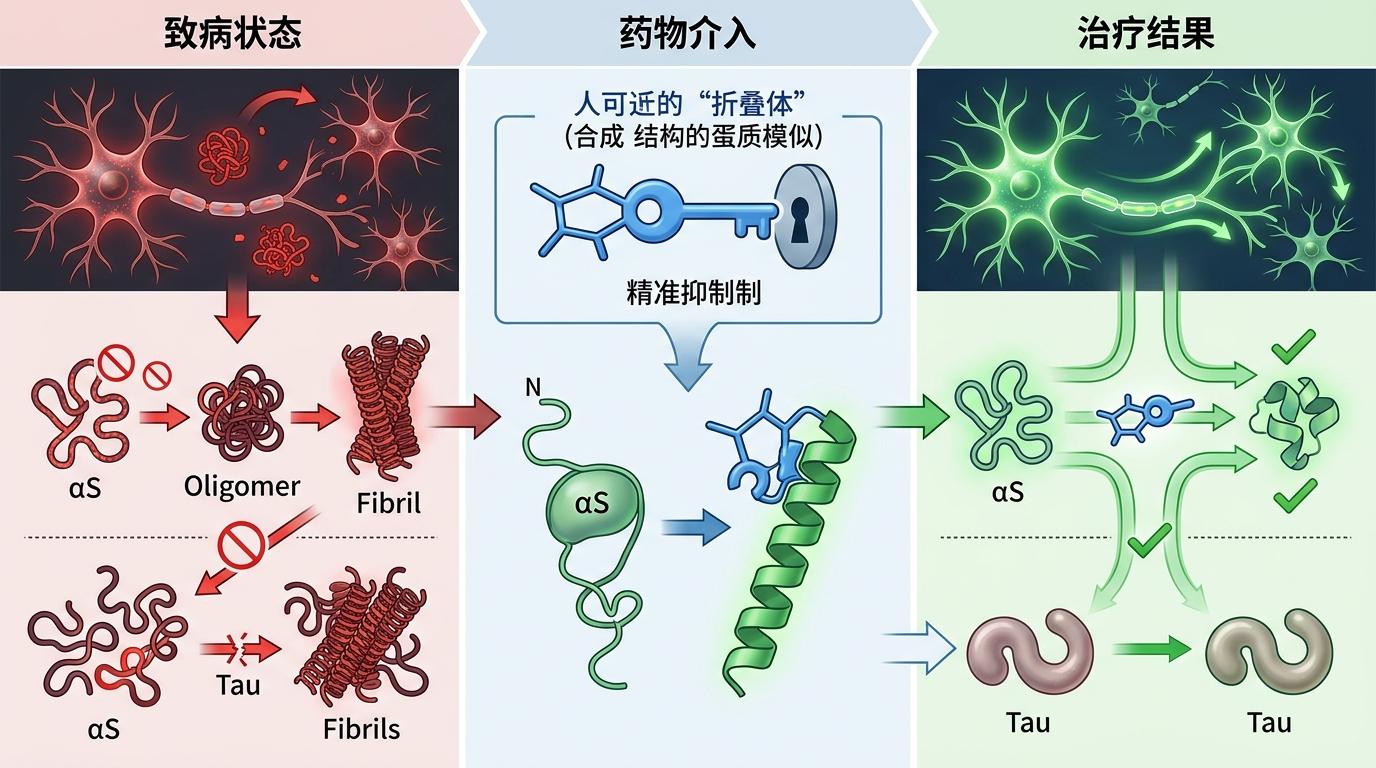
最让人振奋的,是它能闯过血脑屏障。这层包裹大脑的“防火墙”,曾把98%的候选药物挡在门外,无数神经疾病疗法都折戟于此。SK-129却能顺利穿透,在小鼠模型里把脑内的病理损伤拦腰砍断。团队在人类细胞、患者组织甚至线虫模型里反复测试,它都能精准减少蛋白聚集的毒性,还没显出明显副作用。
但我们得清醒——这不是终点,只是风暴眼里透出的光。SK-129的口服生物利用度还得优化,长期用药的安全性需要更严苛的验证,甚至它对不同患者体内αS聚集的“亚型”是否都有效,还得打个问号。神经退行性疾病的病因从来不是单一蛋白作乱,炎症、线粒体损伤、神经通路崩溃是缠在一起的死结,单一药物很难一锤定音。
更值得关注的是SK-129背后的逻辑:我们终于从“缓解症状”转向“掐断病因”。过去我们给帕金森患者开左旋多巴,给阿尔茨海默病人开胆碱酯酶抑制剂,都是在给已经受损的神经通路“补润滑油”,而SK-129是直接去拧紧蛋白错误折叠的“开关”。这种思路的转变,比一个候选药物的出现更有意义。
未来的路还长,从实验室到病床,至少还要2到3年的临床试验,还要跨越监管、生产、定价的重重关卡。但至少现在,我们手里有了一根能伸进风暴中心的杠杆。
拦得住蛋白聚集,才挡得住大脑的崩塌。