对抗知识焦虑,从看懂这条开始
App 下载
缺个受体,为什么会让脓毒症找上门
免疫调控|中国药科大学|巨噬细胞|雌激素受体β|脓毒症|感染性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
免疫调控|中国药科大学|巨噬细胞|雌激素受体β|脓毒症|感染性疾病|医学健康
每年全球有4890万人被脓毒症盯上,1100万人因此离世——这是比癌症更悄无声息的杀手。它可能始于一次肺炎、一场尿路感染,甚至只是皮肤破了个小口子,却能在几天内让全身器官彻底罢工。医生们一直困惑:为什么同样是感染,有的人能扛过去,有的人却被拖进鬼门关?中国药科大学的研究团队给出了一个意想不到的答案:你体内一个叫雌激素受体β(ERβ)的蛋白质,可能正悄悄决定着你和脓毒症的距离。
你可以把ERβ想象成免疫细胞里的「抗炎指挥官」——它平时驻守在巨噬细胞中,一旦身体遭遇感染,就会发出指令,抑制过度的炎症反应,同时指挥巨噬细胞精准吞噬细菌。但研究人员在脓毒症患者的血液样本里发现,这些患者体内的ERβ水平几乎降到了谷底,而且病情越重,ERβ就越少。
为了确认这个关联,团队做了一组对比实验:把小鼠体内的ERβ基因完全敲除,再用同样的细菌诱导脓毒症。结果惊人:ERβ缺失的小鼠存活率不到30%,而正常小鼠的存活率超过70%。解剖后发现,缺失ERβ的小鼠体内,负责吞噬细菌的巨噬细胞死了一大半,细菌在肝脏、脾脏里疯狂繁殖,器官像被强酸浸泡过一样布满炎症坏死灶。
更关键的是,这种差异和性别有关。女性体内的ERβ天然比男性更充足,这也解释了为什么临床数据里,男性脓毒症的发病率和死亡率都比女性高出一截——就像少了一层天然的免疫防护罩。
ERβ的缺席,到底是怎么把巨噬细胞推向死亡的?答案藏在细胞的「能量工厂」里。
正常情况下,巨噬细胞靠「脂肪酸氧化」获取能量,维持吞噬细菌的能力。但当ERβ缺失时,这条代谢通路就像被踩了油门的汽车,疯狂运转起来——脂肪酸氧化的关键酶CPT1活性翻了好几倍,细胞内的乙酰辅酶A(一种代谢中间产物)越积越多。
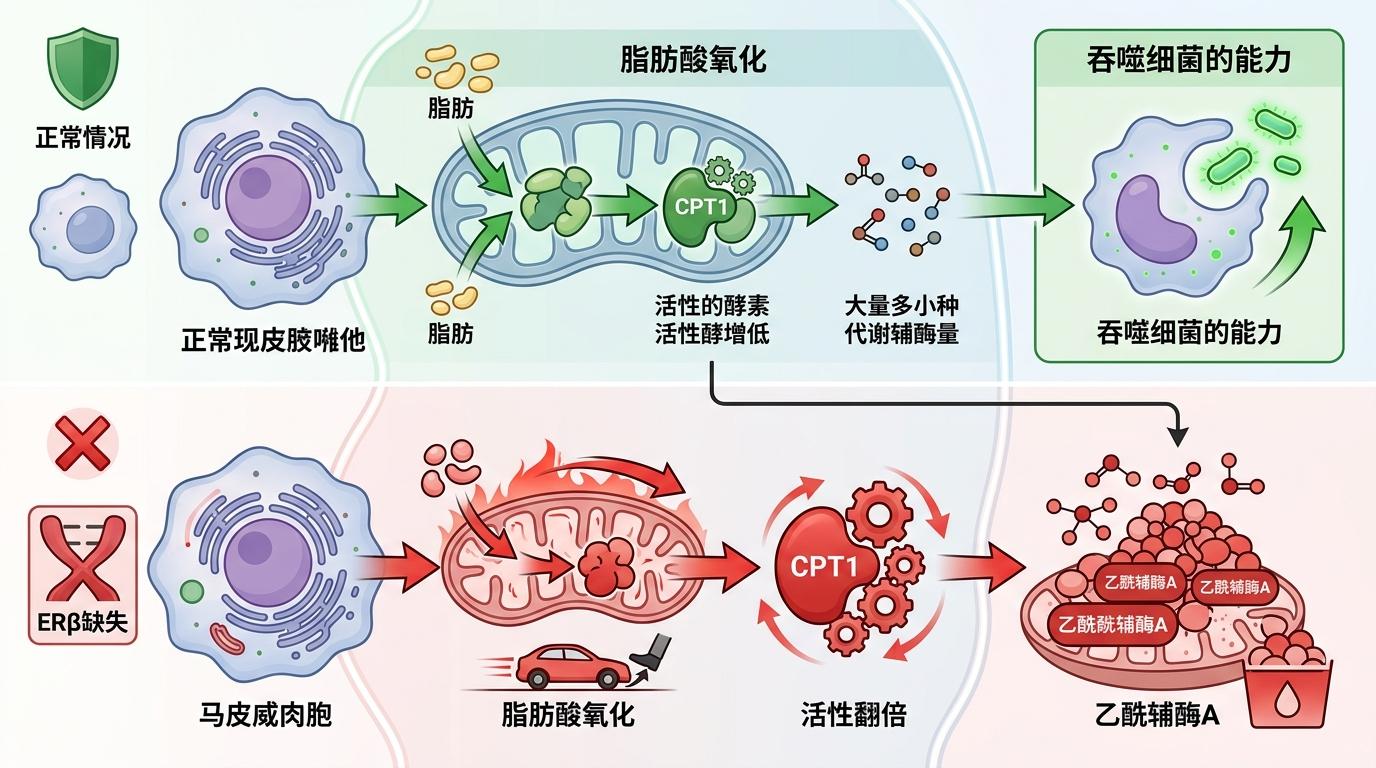
这就触发了一个致命的连锁反应:过量的乙酰辅酶A会给一种叫Stoml2的线粒体蛋白「贴标签」——在它的K221位点加上一个乙酰基。原本Stoml2的工作是维持线粒体膜的稳定,被乙酰化后,它就像被点了穴的士兵,彻底失去了功能。线粒体膜开始渗漏,大量活性氧(ROS)从里面跑出来,直接激活了细胞内的「死亡开关」——NLRP3炎症小体。
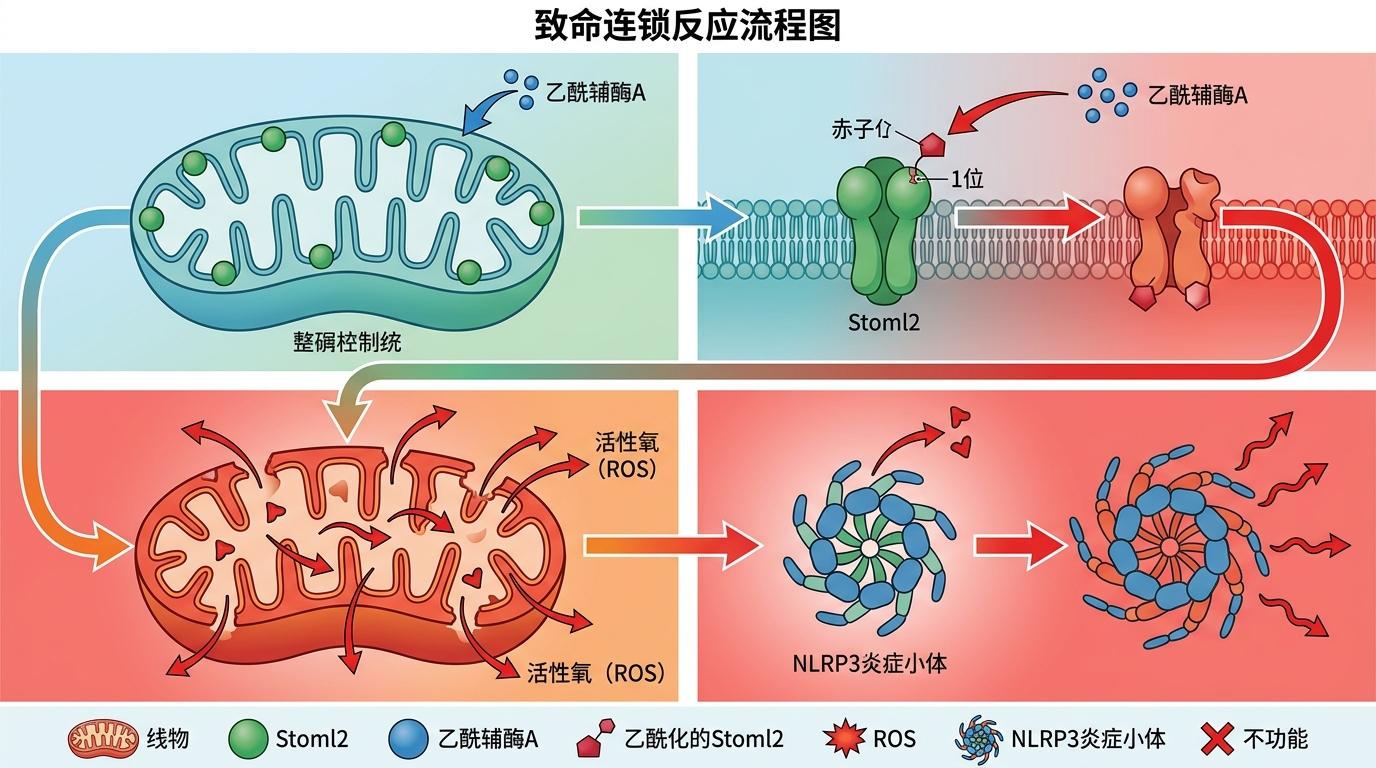
炎症小体一旦激活,就会让巨噬细胞发生「焦亡」:细胞膜上被戳出无数孔洞,细胞内容物连同大量促炎因子一起喷涌而出,不仅自己死了,还会引发更剧烈的全身炎症反应。就像一个失控的免疫细胞,临死前还要在体内投下一颗炎症炸弹。
团队做了一个验证实验:把Stoml2的K221位点突变,让它无法被乙酰化,再把这些修改后的巨噬细胞移植回ERβ缺失的小鼠体内。原本活不过3天的小鼠,有一半撑过了一周,体内的细菌数量也降到了原来的1/10。
这个发现不止是在分子层面补全了脓毒症的发病拼图,更给临床治疗带来了新的方向。
目前针对脓毒症的治疗,大多还停留在抗生素抗感染和器官支持阶段,缺乏精准的靶向药物。而ERβ信号通路、脂肪酸氧化通路,还有Stoml2的乙酰化位点,都是潜在的治疗靶点。比如用ERβ激动剂「唤醒」沉睡的抗炎机制,用脂肪酸氧化抑制剂「踩刹车」,或者直接研发能阻断Stoml2乙酰化的小分子药物。
但从实验室到病床,还有不少坎要跨。比如脂肪酸氧化抑制剂Etomoxir,在动物实验里效果显著,但因为会影响心脏和肝脏的正常代谢,一直无法进入临床。而ERβ激动剂的使用也需要考虑性别差异:男性患者可能需要更高的剂量,女性患者则要避免过度激活带来的副作用。
更重要的是,脓毒症的遗传易感性不止ERβ一个。之前的研究已经发现,TNF2基因携带者、IL1RN*2基因携带者,都会比普通人更容易患上脓毒症。未来的诊疗,可能需要像查基因图谱一样,先检测患者的易感基因,再量身定制治疗方案——这才是真正的精准医疗。
当我们把脓毒症的发病机制拆解到一个个蛋白质、一个个分子位点时,会发现人类的免疫系统就像一台精密的机器——哪怕只是一个小零件的缺失,都可能引发连锁故障,让整台机器彻底停摆。
「免疫的平衡,藏在分子的细节里。」这个发现不仅让我们离脓毒症的精准治疗更近了一步,也让我们意识到:那些看似无关的基因差异,那些隐藏在细胞深处的代谢变化,可能就是决定生死的关键。未来的医学,终将从「治疗疾病」走向「调节平衡」——而这,正是生命最精妙的地方。