
10 天前

10 天前
你有没有想过,视力模糊和反复咳嗽可能是同一个病根?有这样一群患者,他们从小就看不清暗处的东西,视野一天天缩窄,同时还被慢性鼻炎、肺炎缠上,肺功能逐年下降——这不是两种独立的病,而是同一个基因出了问题。香港科技大学刘振团队联合海外研究者,在最新研究里揭开了这个秘密:RPGR基因的缺失,会同时破坏眼睛的感光纤毛和呼吸道的运动纤毛,而背后的关键,是被搅乱的F-肌动蛋白动态。为什么一个基因能影响两个完全不同的器官?这得从纤毛的秘密说起。
你可以把纤毛想象成细胞表面伸出的小天线——有的负责「接收信号」,比如视网膜里的感光纤毛,专门捕捉光信号,是视觉的基础;有的负责「主动运动」,比如呼吸道里的运动纤毛,像无数小刷子一样同步摆动,把黏液和病菌扫出体外。
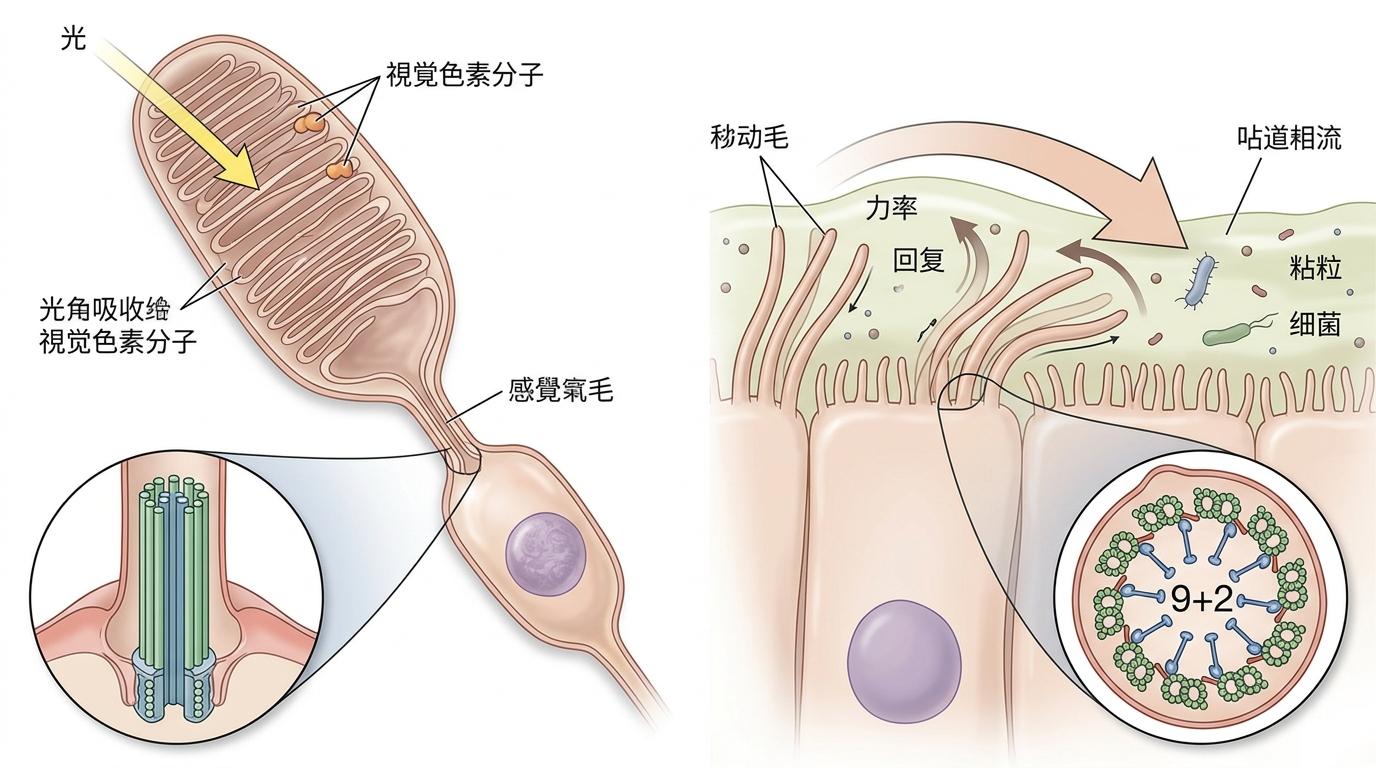
但真实的机制比这更精确:感光纤毛是单个的「信号接收器」,几乎遍布所有细胞,光感受器的外节就是特化的感光纤毛,每天要更新10%的膜盘,靠的就是纤毛内的精准运输;运动纤毛是成片的「动力装置」,呼吸道上皮细胞上长着200到300根,每秒摆动10到20次,形成的黏液纤毛清除系统,是肺部的第一道防线。
RPGR基因就管着这些天线的「正常运转」。它编码的蛋白定位在纤毛的过渡区——相当于天线的「信号门」,负责调控哪些蛋白能进入纤毛。一旦这个基因缺失,「信号门」失灵,两种纤毛都会出问题。
研究者用CRISPR技术敲除了呼吸道细胞里的RPGR基因,结果一目了然:
你可以把F-肌动蛋白想象成细胞里的「脚手架」,正常情况下它会不断组装和解聚,维持细胞的形态和物质运输。但RPGR缺失后,调控肌动蛋白解聚的Gelsolin蛋白水平下降,「脚手架」拆不掉,越堆越多,直接挡住了纤毛的生长通道,还搅乱了纤毛的摆动节奏。
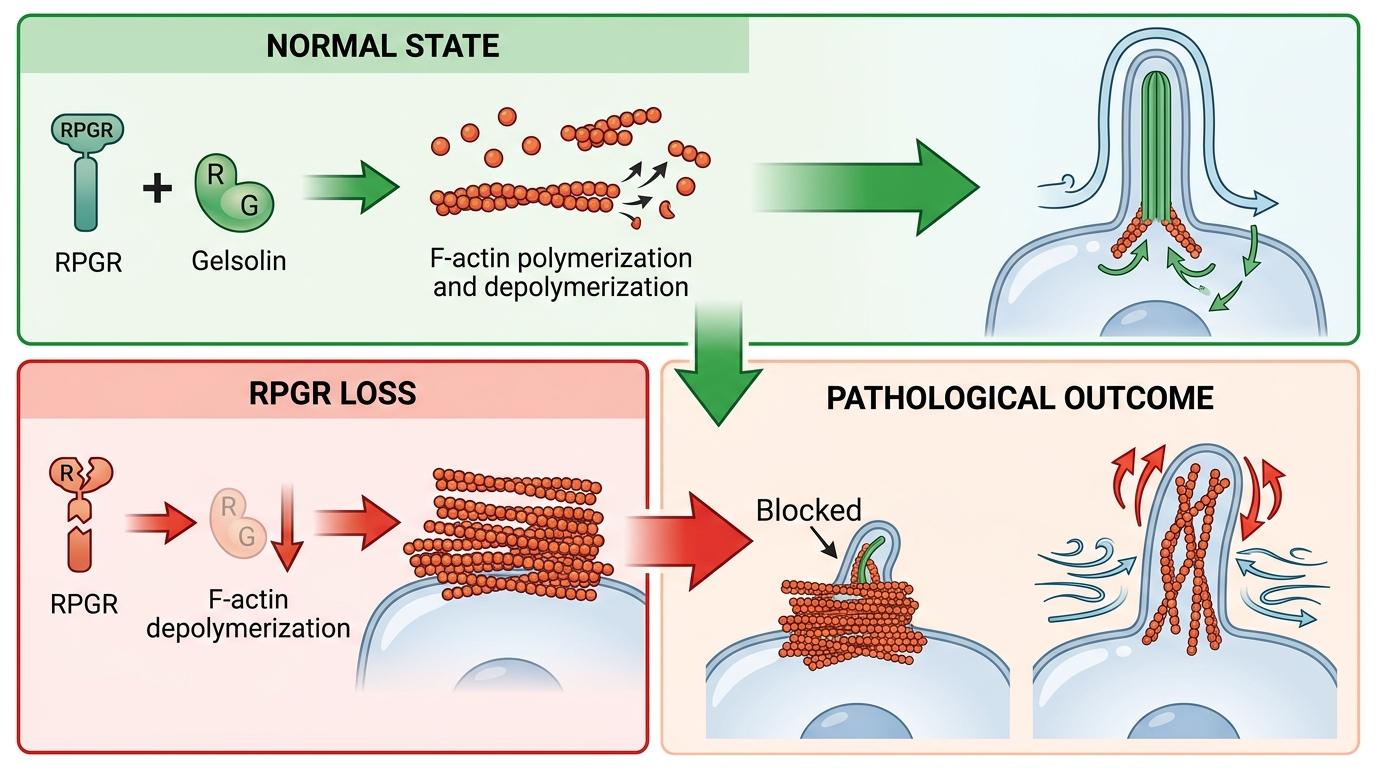
更关键的是,这个机制同时适用于眼睛和呼吸道:在视网膜的光感受器里,肌动蛋白的异常稳定会导致膜盘形成受阻,旧的膜盘排不出去,最终造成光感受器退化;在呼吸道里,就是纤毛摆不动,病菌排不出去,反复引发感染。
有意思的是,用肌动蛋白聚合抑制剂Latrunculin A处理这些缺陷细胞,乱掉的「脚手架」被拆开,纤毛的长度和摆动居然能部分恢复——这也给治疗指了一条路。
RPGR相关的原发性纤毛运动障碍(PCD),是一种很容易被漏诊的病。
普通PCD患者的纤毛超微结构会有明显异常,比如动力臂缺失,但RPGR缺陷的患者,纤毛的「9+2」微管结构看起来完全正常,只是数量少、摆不动。更麻烦的是,这类患者的鼻腔一氧化氮水平可能接近正常——而这是PCD筛查的常用指标。
研究者发现,不是所有RPGR变异都会引发PCD:只有同时影响两个主要剪接异构体的变异,才会导致严重的呼吸道症状;如果只影响视网膜特异性的异构体,患者可能只有视力问题,没有呼吸症状。同一家族里携带相同变异的兄弟,也可能因为CEP290等修饰基因的存在,一个出现PCD,一个只患视网膜色素变性。
这意味着,对于有视网膜色素变性的患者,尤其是男性,医生得多问一句:你有没有反复咳嗽、鼻塞的毛病?而基因检测,才是确诊这类「隐形」PCD的关键。
我们总把人体的器官当成独立的零件,却忘了它们共享着一套底层的分子逻辑。RPGR基因的故事,就是最好的例子:一个基因的缺失,同时影响了眼睛的「信号接收」和肺部的「垃圾清理」,背后是同一个被搅乱的肌动蛋白动态。
更值得深思的是,这类「跨系统纤毛病」的诊断和治疗,才刚刚起步。基因编辑和肌动蛋白调控药物的探索,给患者带来了希望,但我们还需要更精准的诊断工具,更深入的分子机制研究。
纤毛虽小,却是生命的「晴雨表」。 它的每一次摆动、每一次信号传递,都关乎着我们能不能看清世界,能不能顺畅呼吸。
点击充电,成为大圆镜下一个视频选题!