对抗知识焦虑,从看懂这条开始
App 下载
小细胞肺癌迎来新武器:口服环状肽精准杀癌
化疗耐药|TP53基因|RB1基因|口服环状肽药物|小细胞肺癌|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
化疗耐药|TP53基因|RB1基因|口服环状肽药物|小细胞肺癌|肿瘤学|医学健康
一位62岁的广泛期小细胞肺癌患者,在经历了铂类化疗耐药后,几乎已经走到了无药可用的地步——这种被称为“癌症之王”的肺癌亚型,5年生存率不足7%,且长期缺乏有效的靶向治疗手段。直到2025年,哈佛医学院团队的一项研究为这类患者撬开了希望的缝隙:他们开发出一种口服环状肽药物,能精准瞄准小细胞肺癌的致命弱点,在化疗耐药的患者肿瘤模型中显著抑制病灶生长。这种药物究竟是如何突破小细胞肺癌的治疗僵局的?
要理解这种新药的作用,得先看清小细胞肺癌的“命门”——几乎所有患者体内的RB1和TP53基因都发生了失活突变,这两个基因就像细胞周期的“刹车闸”,一旦失效,细胞就会失去G1-S检查点的调控,疯狂增殖。
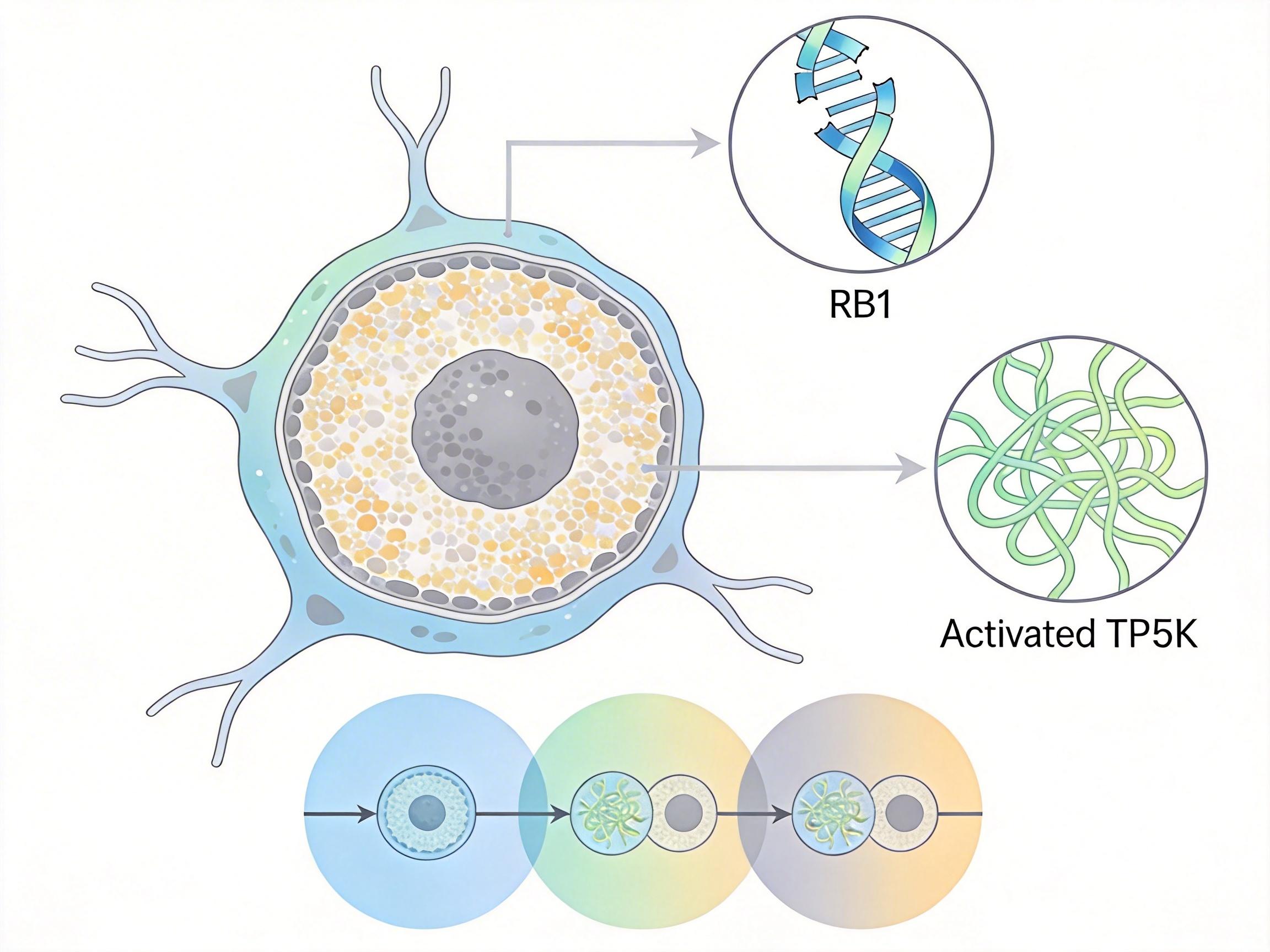
你可以把细胞周期想象成一列按点运行的火车,G1-S检查点就是站台的检票员,只有拿到“放行信号”的细胞才能进入DNA复制的S期。而RB1基因编码的Rb蛋白,就是攥着检票权的人——它会牢牢绑定E2F转录因子,不让它启动细胞增殖的程序。但当RB1突变失活,E2F就会彻底失控,不仅驱动细胞无限分裂,还会因为过度激活触发细胞凋亡,这恰恰成了治疗的突破口。
过去,科学家们尝试过多种方法靶向E2F通路,但都卡在了一个关键节点:细胞周期蛋白A会通过一个叫RxL基序的结构绑定E2F,限制它的活性。这个RxL界面就像一个光滑的平面,传统小分子药物根本无法有效结合,成了公认的“不可成药靶点”。
哈佛团队的突破,在于找到了环状肽这种“新型钥匙”。
不同于线性肽易被降解、难以穿透细胞膜的缺点,环状肽通过首尾成环的结构,拥有更强的稳定性和细胞渗透性,还能像一把定制的扳手,精准卡住细胞周期蛋白A/B的RxL结合界面。它的作用机制分两步:一方面阻断细胞周期蛋白A与E2F的结合,让原本被限制的E2F彻底失控,引发DNA复制压力和损伤;另一方面阻断细胞周期蛋白B与MYT1的结合,促使细胞周期蛋白B和CDK2形成异常复合物,激活纺锤体组装检查点,让癌细胞停滞在有丝分裂阶段,最终启动凋亡程序。
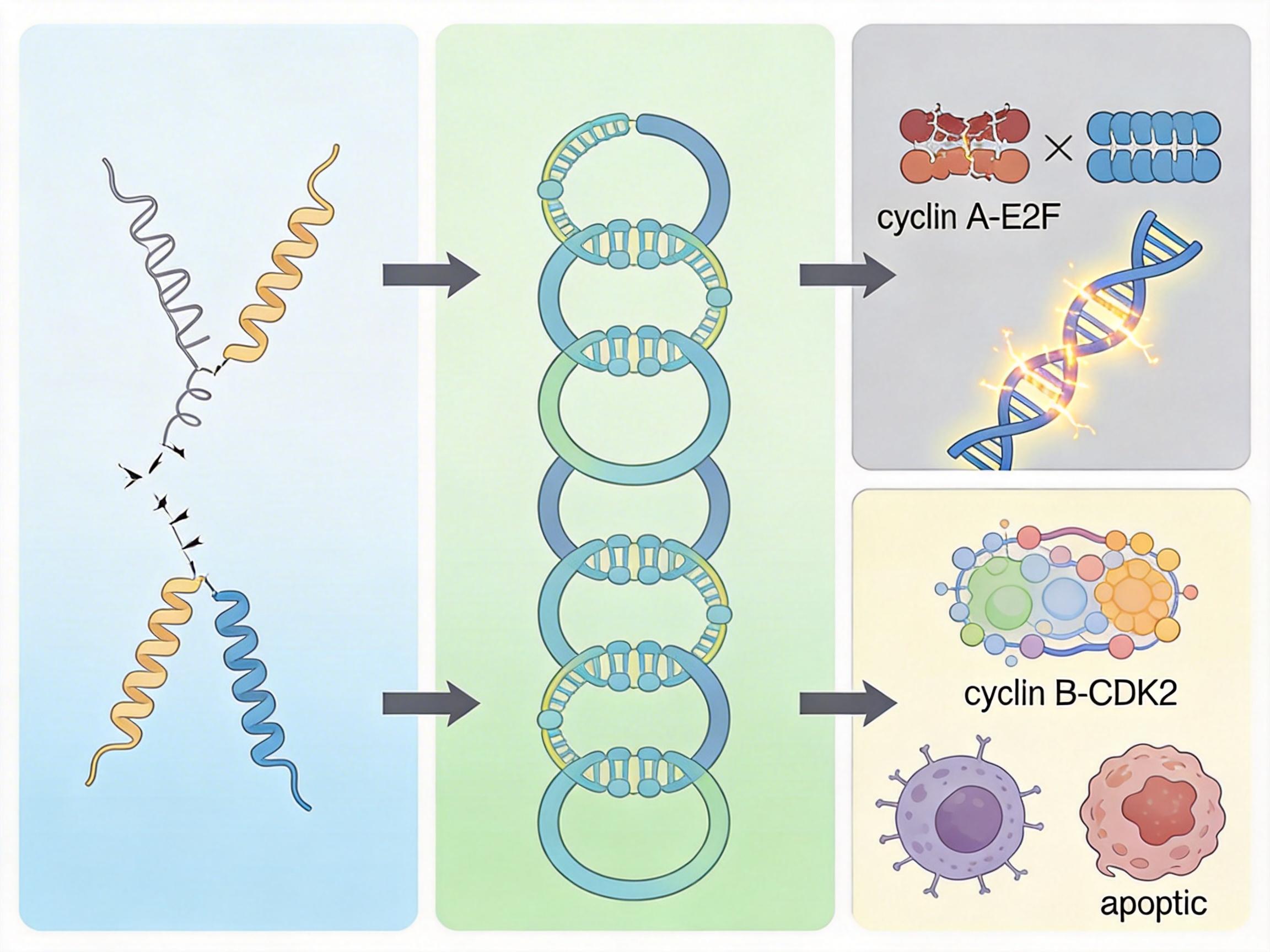
在46种小细胞肺癌细胞系的测试中,这种环状肽表现出了纳摩尔级别的杀伤效力,而对正常细胞的毒性极低——它就像一枚精准制导导弹,只盯着E2F过度活跃的癌细胞。更关键的是,它是口服生物可利用的,患者不用再频繁往返医院输液,这在癌症治疗中是极大的便利。
在化疗耐药的小细胞肺癌患者来源异种移植模型中,口服环状肽展现出了显著的肿瘤抑制效果,甚至能让部分肿瘤缩小。但这并不意味着它能立刻成为“治愈神药”。
首先,环状肽的长期稳定性和体内代谢仍需优化——虽然它比线性肽稳定,但在复杂的体内环境中,依然面临着被酶解、清除的风险。其次,肿瘤的异质性可能导致耐药:部分癌细胞可能会通过突变细胞周期蛋白的结合位点,或者激活其他旁路通路,躲避药物的打击。此外,如何将这种药物与现有的免疫治疗、化疗方案联合使用,实现1+1>2的效果,也需要更多的临床试验数据支持。
更值得关注的是,这种环状肽的成功,打破了“蛋白-蛋白相互作用不可成药”的传统认知。未来,它不仅可能用于小细胞肺癌,还能拓展到其他E2F驱动的癌症,比如部分膀胱癌、三阴性乳腺癌等,为更多难治性癌症患者带来希望。
从“不可成药”到精准靶向,环状肽的出现,就像在癌症治疗的黑暗隧道里点亮了一盏新灯。它不仅是小细胞肺癌患者的新希望,更是药物研发领域的一次范式革新——当我们不再局限于传统小分子的框架,转而拥抱环状肽、PROTAC等新型分子,更多曾经的“不治之症”,或许终将被逐一攻克。
精准瞄准弱点,让癌细胞自毁程序重启。这不仅是环状肽的作用逻辑,也是未来癌症治疗的核心方向:不再是无差别地杀伤细胞,而是利用癌细胞自身的缺陷,引导它们走向终结。