
3 个月前

3 个月前
对于多发性骨髓瘤患者而言,这场战争始于无声。骨髓深处,本应是守护免疫系统的浆细胞,却悄然“叛变”,开始疯狂、无序地增殖。它们如同沉默的蛀虫,侵蚀着人体的根基——骨骼,引发剧痛,污染血液,攻击肾脏。很长一段时间里,这个诊断都意味着一个残酷的判决:无法治愈。
近年来,CAR-T细胞疗法的问世,如同一道划破暗夜的曙光。医生们从患者体内提取出T细胞,在体外将其改造为装备了“导航系统”(即CAR,嵌合抗原受体)的“生物导弹”,再回输体内。这些改造后的细胞能精准识别并摧毁癌细胞表面的特定“旗帜”——BCMA蛋白。无数患者因此获得了生命的延长和高质量的缓解。
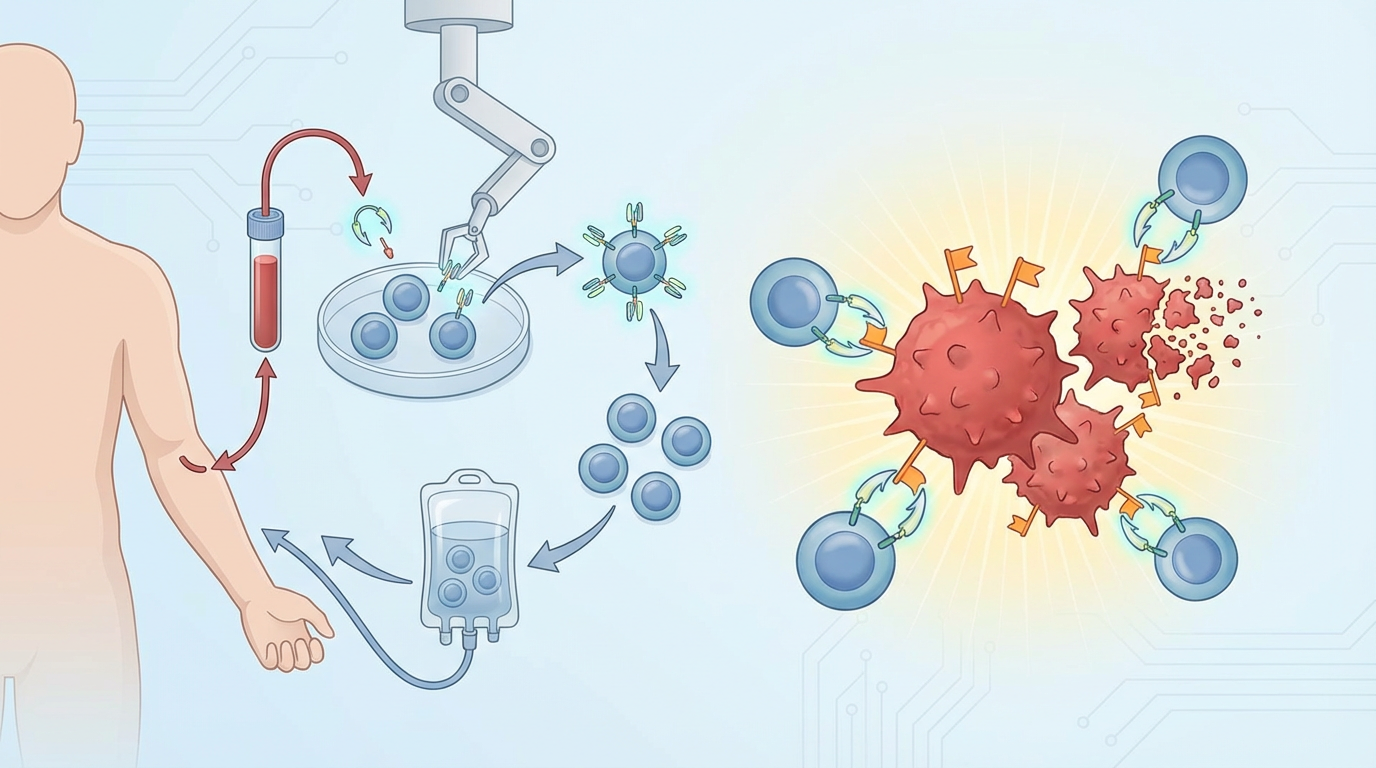
然而,胜利的喜悦往往短暂。癌细胞,这个狡猾的敌人,很快学会了新的生存伎俩。“在一些患者中,治疗根本不起作用。而在另一些患者中,复发迟早会发生,”马克斯·德尔布吕克中心(Max Delbrück Center)的Armin Rehm博士沉重地描述道,“而这种复发,通常会迅速导向终点。”癌细胞通过丢弃或隐藏那面名为BCMA的“旗帜”,玩起了“隐身术”,让耗资百万、精心打造的“生物导弹”瞬间失去了目标,最终导致疾病卷土重来。这场战争,似乎又回到了原点。
就在不久前,这场看似陷入僵局的战争迎来了新的转机。由Armin Rehm博士领导,联合柏林夏里特医学院等机构的一个国际研究团队,在国际顶尖期刊《Molecular Therapy》上公布了一项突破性成果。他们开发出一种更智能、更强大的“生物导弹”——一种能够同时识别两个靶点的“双特异性”CAR-T细胞。
这项研究的核心,是为CAR-T细胞安装了第二套“导航系统”。除了原有的BCMA靶点,科学家们通过单细胞RNA测序、免疫组织化学和流式细胞术等多种高精尖技术“侦查”,在恶性浆细胞上找到了另一个独特的“旗帜”——BAFF-R(B细胞激活因子受体)。
“BAFF-R在复发的多发性骨髓瘤患者细胞上尤其丰富,”该研究的第一作者Agnese Fiori博士解释道,“更关键的是,它常常出现在那些已经‘脱掉’BCMA外衣、对常规治疗产生抗性的癌细胞上。”
这意味着,新型的双靶点CAR-T细胞拥有了“双重保险”。无论癌细胞是悬挂BCMA旗帜,还是BAFF-R旗帜,甚至两者兼有,都无法逃脱被识别和摧毁的命运。这套“双重锁定”系统,从根本上破解了癌细胞的“隐身术”,有望彻底解决由单一靶点丢失导致的耐药与复发难题。
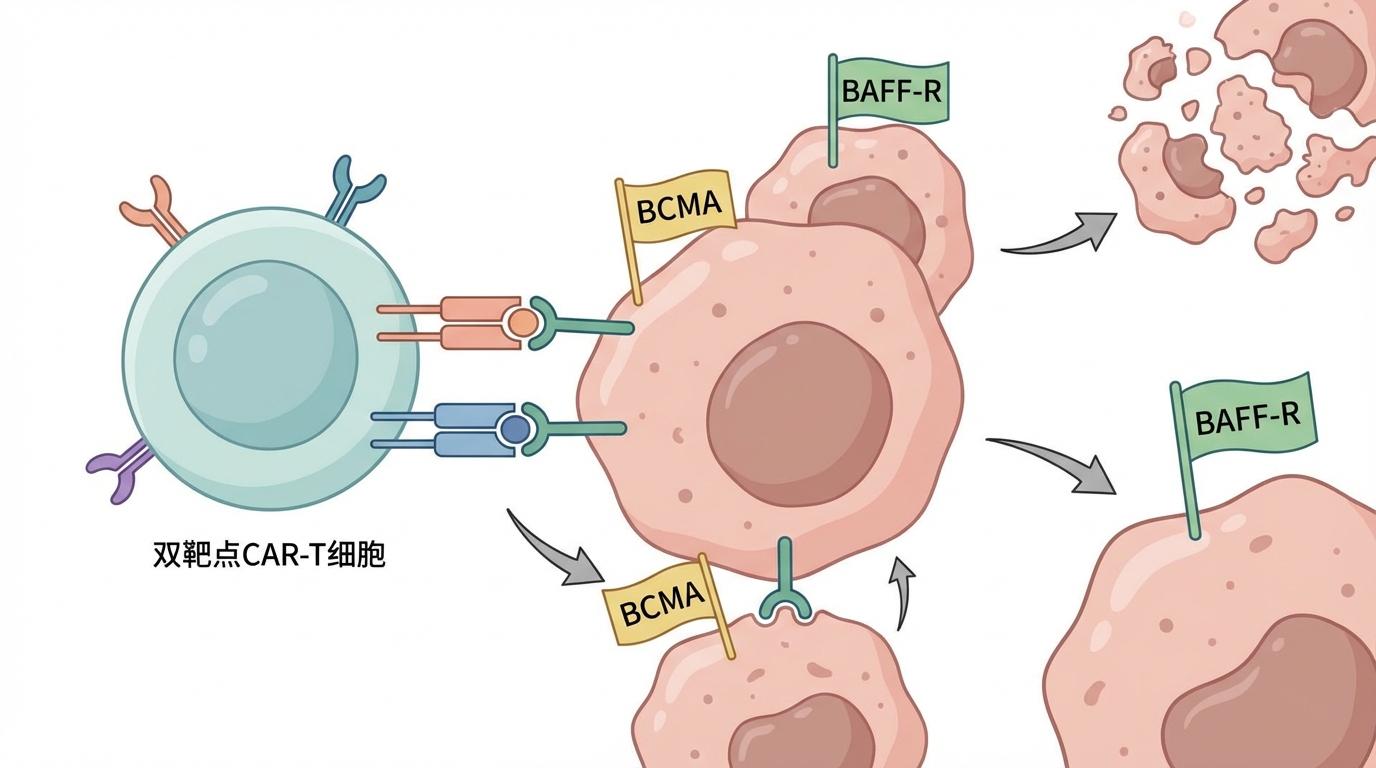
要理解这次突破的深刻意义,我们需要深入细胞战争的微观战场。
传统的BCMA CAR-T疗法,是一种典型的**“单点打击”策略。它高效、精准,但其成败完全系于BCMA这一个靶点之上。癌细胞的生存本能驱使其不断变异。在强大的免疫压力下,部分癌细胞会通过基因突变等方式,停止表达BCMA蛋白。这种现象被称为“抗原逃逸”**,是CAR-T治疗失败的最主要原因之一。就像一支只认识一种敌军军服的特种部队,一旦敌人换装,整个军队就会束手无策。
而Rehm博士团队的“双靶点”策略,则是将“单点打击”升级为一张**“天罗地网”**。这张网由两个关键节点构成:
这种设计具有双重战略意义:
在实验室中,研究团队用多发性骨髓瘤细胞系和直接取自患者的骨髓细胞进行了验证。“在我们所有的实验中,”Rehm博士总结道,“即使BCMA靶点缺失或因治疗而丢失——也就是在单靶点CAR-T治疗失败的场景下——我们改进后的CAR-T细胞依然能高效地完成任务。”
这项发表在《Molecular Therapy》上的研究,不仅仅是一次技术上的迭代,它为一部分陷入绝境的多发性骨髓瘤患者带来了切实的希望。Rehm博士估计,大约有5%到30%的多发性骨髓瘤患者,特别是那些经历复发的患者,可以直接从这种双靶向方法中受益。
更重要的是,这种疗法具备实现个体化精准治疗的潜力。通过在治疗前对患者的肿瘤细胞进行简单的筛查,医生就能判断其是否同时表达BCMA和BAFF-R,从而精准地为他们匹配这种“升级版”的CAR-T疗法。这种筛查技术在目前的临床实践中完全可行,操作简便。
当然,从实验室的成功走向临床的广泛应用,还有一段路要走。“为了真正评估我们方法的潜力,现在迫切需要进行一项初步的临床试验,”Rehm博士补充道。他希望这种优化的CAR-T细胞能尽快进入临床,真正惠及患者。
这场围绕多发性骨髓瘤的战争,因“双靶点”CAR-T的出现而进入了一个新的阶段。它标志着肿瘤免疫治疗的思路正在从“寻找一个好靶点”向“构建一个智能的、多维度的攻击网络”转变。这不仅可能延长许多患者的生命,更有可能在未来,将“无法治愈”的多发性骨髓瘤,真正变为一种可以被长期控制甚至治愈的疾病。
科学的每一次前行,都在为生命的战场增添新的武器。双靶点CAR-T的出现,正是这样一件锋利的兵器,它让我们有理由相信,在与癌症这场漫长而艰苦的博弈中,人类的智慧与坚韧,终将迎来胜利的曙光。
点击充电,成为大圆镜下一个视频选题!