
12 天前

12 天前
当医生给晚期癌症患者用上免疫检查点抑制剂时,总有一部分人会出现“免疫耐药”——药物明明激活了T细胞,可它们就是打不动肿瘤。直到最近,圣犹达儿童研究医院的团队才揭开这个隐秘的真相:问题出在免疫系统的“传令兵”身上。
这群叫cDC1的树突状细胞,本该把肿瘤抗原递交给T细胞,像吹响冲锋号一样启动免疫攻击。但在肿瘤微环境里,它们的“能量工厂”线粒体已经悄悄罢工,连自己都活成了“哑炮”,更别说指挥T细胞作战。为什么线粒体的状态能决定免疫治疗的生死?这背后藏着一套被肿瘤破解的能量密码。
你可以把cDC1想象成一个带着情报的侦察兵,线粒体就是它的随身电池——只有电量充足,它才能把肿瘤抗原完整“打包”,送到T细胞面前激活杀伤反应。
研究人员在肿瘤里发现了两类cDC1:一类是“满电状态”的极化线粒体cDC1,它们的线粒体膜电位稳定、体积饱满,能高效激活CD8+T细胞;另一类是“亏电状态”的去极化线粒体cDC1,线粒体皱缩、能量代谢紊乱,递交给T细胞的抗原要么残缺不全,要么干脆没有。
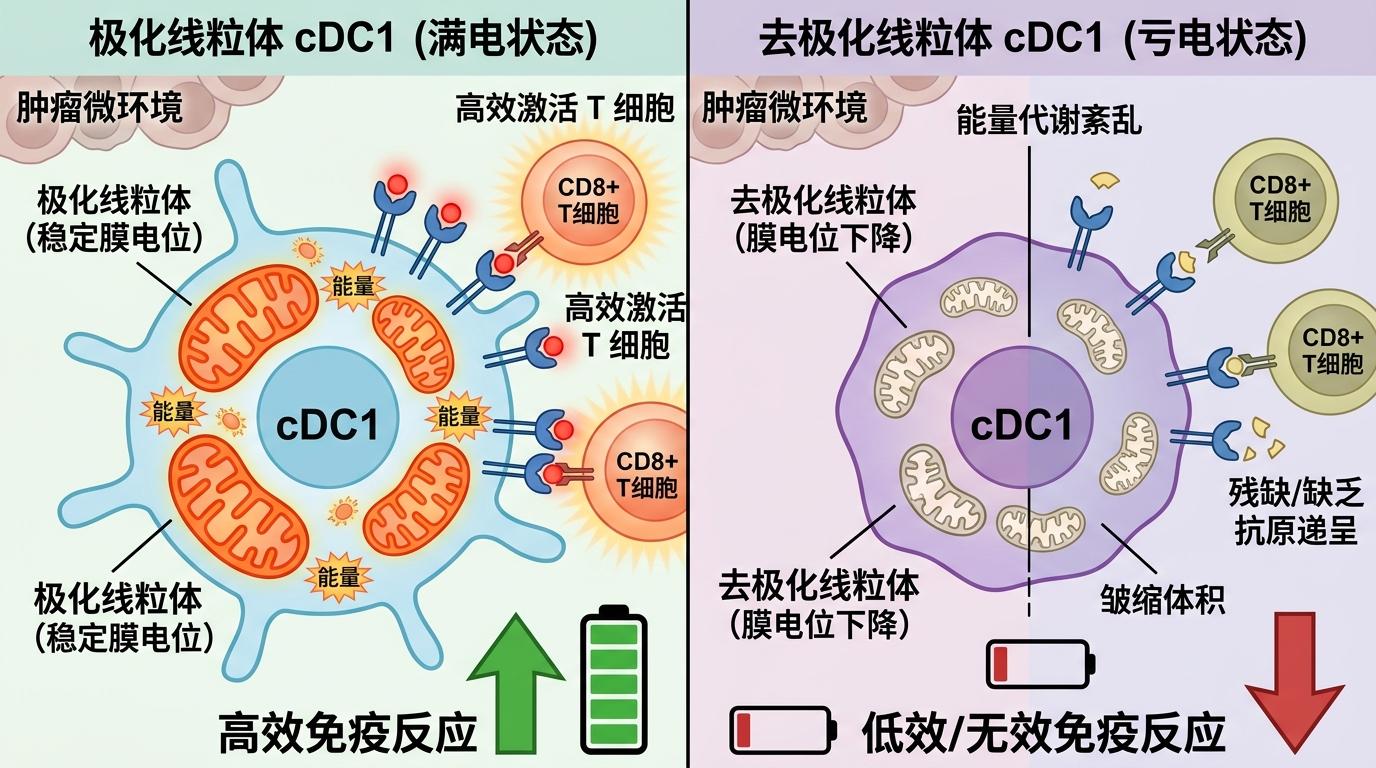
而掌控这个开关的,是线粒体内膜上的OPA1蛋白。它像一个“线粒体维修工”,不仅维持线粒体的融合状态,还能激活核内的NRF1因子,保证电子传递链完整,让线粒体持续输出能量和维持NAD+/NADH的氧化还原平衡。一旦OPA1水平下降,线粒体就会快速“掉电”,cDC1的抗原呈递功能直接瘫痪。
肿瘤早就摸透了这套机制,它在自己的地盘里布下了一张“能量绞杀网”:靠糖酵解疯狂消耗葡萄糖,让cDC1没了“口粮”;分泌的乳酸和酸性环境,直接损伤线粒体膜结构;随着肿瘤进展,cDC1里的OPA1-NRF1信号通路会持续减弱,线粒体体积缩小、膜电位下降,最终彻底失去功能。
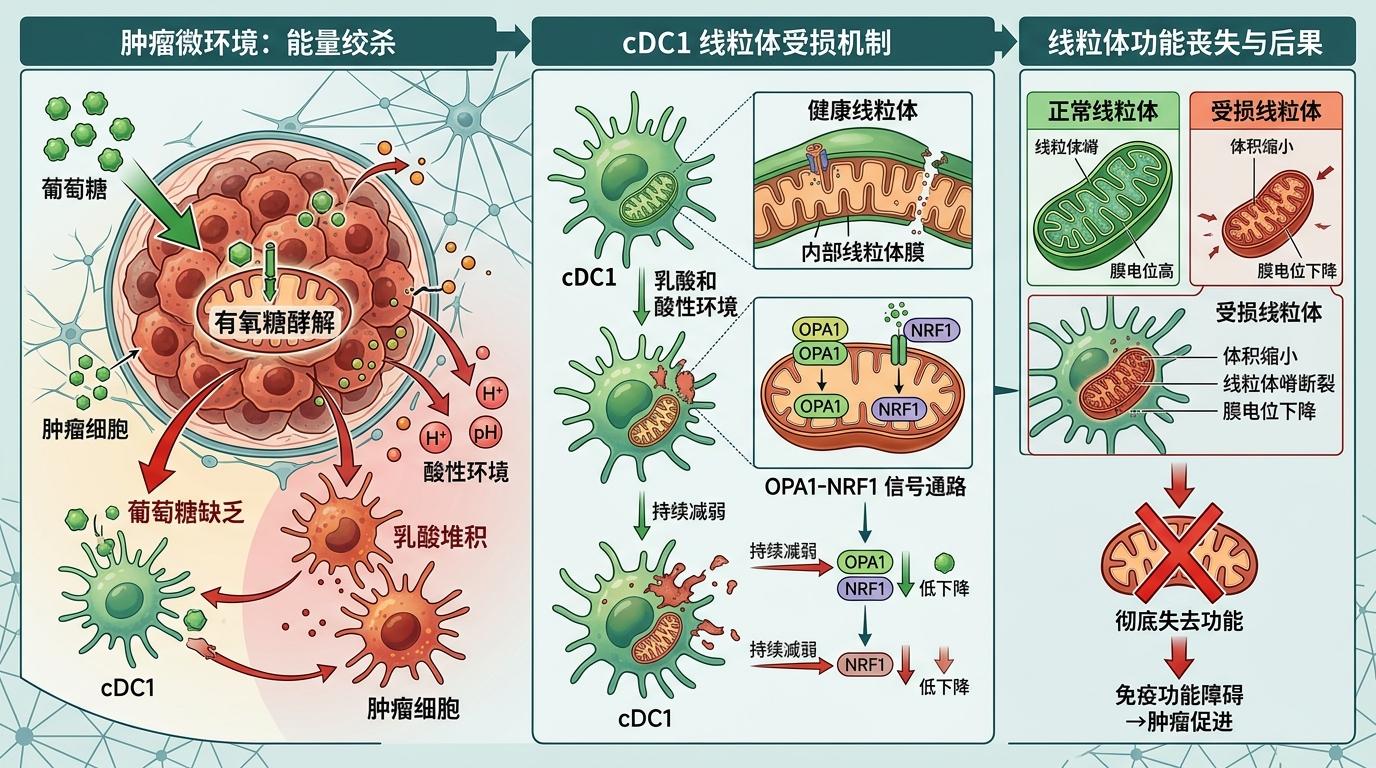
研究团队做了一个对照实验:给荷瘤小鼠注射极化线粒体的cDC1,单独使用就能减缓肿瘤生长;如果再联合免疫检查点抑制剂,居然有部分小鼠的肿瘤被完全清除,还产生了持久的免疫记忆——就算再接种肿瘤细胞,免疫系统也能快速发起攻击。
更关键的是,当cDC1的线粒体被“充能”后,它不仅能高效激活T细胞,还能抑制自噬对MHC-I分子的降解,相当于给T细胞配备了精准的“肿瘤识别雷达”,让免疫攻击不再漫无目的。
现在看来,给cDC1的线粒体“充电”,是突破免疫治疗瓶颈的新方向,但真正走到临床,还有不少难题要解决。
首先是精准激活的问题:如何只给肿瘤里的cDC1“充能”,而不影响正常细胞的线粒体功能?目前研究里用的是体外培养后回输的细胞疗法,但这种方法成本高、个性化要求强,很难大规模推广。
其次是肿瘤微环境的干扰:就算cDC1被激活,肿瘤里的乳酸、低氧环境依然会持续损伤线粒体,所以需要同时配合靶向肿瘤代谢的药物,比如抑制乳酸生成的抑制剂,才能保住cDC1的“战斗力”。
最后是个体差异:不同患者的肿瘤微环境对cDC1的抑制程度不同,如何找到能预测疗效的生物标志物,比如肿瘤里OPA1的表达水平,是实现精准治疗的关键。
过去我们总把免疫治疗的希望寄托在T细胞上,给它们“松绑”、给它们“加油”,却忽略了cDC1这个“传令兵”的状态。就像一场战争,前线战士再勇猛,没有准确的情报和指挥,也打不赢一场胜仗。
线粒体不再只是一个“能量工厂”,它是免疫细胞的“战斗力开关”,更是肿瘤和免疫系统博弈的核心战场。给免疫细胞充能,让“哑炮”重新吹响冲锋号,这或许就是未来破解癌症免疫耐药的关键。毕竟,再强大的战士,也需要一个能准确传递情报的侦察兵。
点击充电,成为大圆镜下一个视频选题!