对抗知识焦虑,从看懂这条开始
App 下载
肾癌耐药的死循环,被解放军总医院团队破解了
耐药机制|死亡受体5|解放军总医院|舒尼替尼|肾癌|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
耐药机制|死亡受体5|解放军总医院|舒尼替尼|肾癌|肿瘤学|医学健康
想象一下:医生给晚期肾癌患者开了救命的靶向药舒尼替尼,起初肿瘤确实缩小了,但几个月后,癌细胞像突然解锁了防御buff,药物彻底失效。更棘手的是,近30%的患者从一开始就对这款药天然耐药。
这不是科幻场景,而是每年成千上万肾癌患者的真实困境——靶向药耐药,是横在他们和活下去之间的一道高墙。直到最近,解放军总医院的研究团队在《Cell Death & Differentiation》上发表的成果,终于撬开了这道墙的缝隙:他们揪出了癌细胞用来躲避免疫和药物攻击的「死循环」,还找到了打破它的钥匙。
死亡受体5(DR5),光听名字就知道它的本职工作:接到指令后诱导癌细胞凋亡,是个自带「正义属性」的蛋白。但解放军总医院的团队发现,在肾癌组织和对舒尼替尼耐药的癌细胞里,DR5的含量异常高——它不仅没在杀敌,反而成了癌细胞的「保护伞」。
你可以把DR5和癌细胞的关系,想象成一个叛变的卧底:它原本是来触发自杀程序的,结果反而和癌细胞的生存信号勾搭上了。团队通过基因编辑实验证实,只要把耐药癌细胞里的DR5敲除,原本对舒尼替尼无动于衷的癌细胞,会重新对药物敏感;反过来,如果给敏感癌细胞过量表达DR5,它们很快就会变成耐药细胞。
但真实的机制比这更精确:DR5并不是直接对抗药物,而是通过调控一条关键的细胞信号通路——NF-κB,来给癌细胞「续命」。
要搞懂这个「死循环」,得先拆解三个关键角色:DR5、p65(NF-κB通路的核心蛋白),还有负责给蛋白「贴标签」的E3泛素连接酶复合体。
你可以把E3泛素连接酶复合体想象成细胞里的「垃圾处理站」,它会给没用的蛋白贴上「销毁」标签,让蛋白酶体把它们降解。p65原本是这个「垃圾站」的处理对象——正常情况下,它会被定期销毁,避免NF-κB通路过度激活。
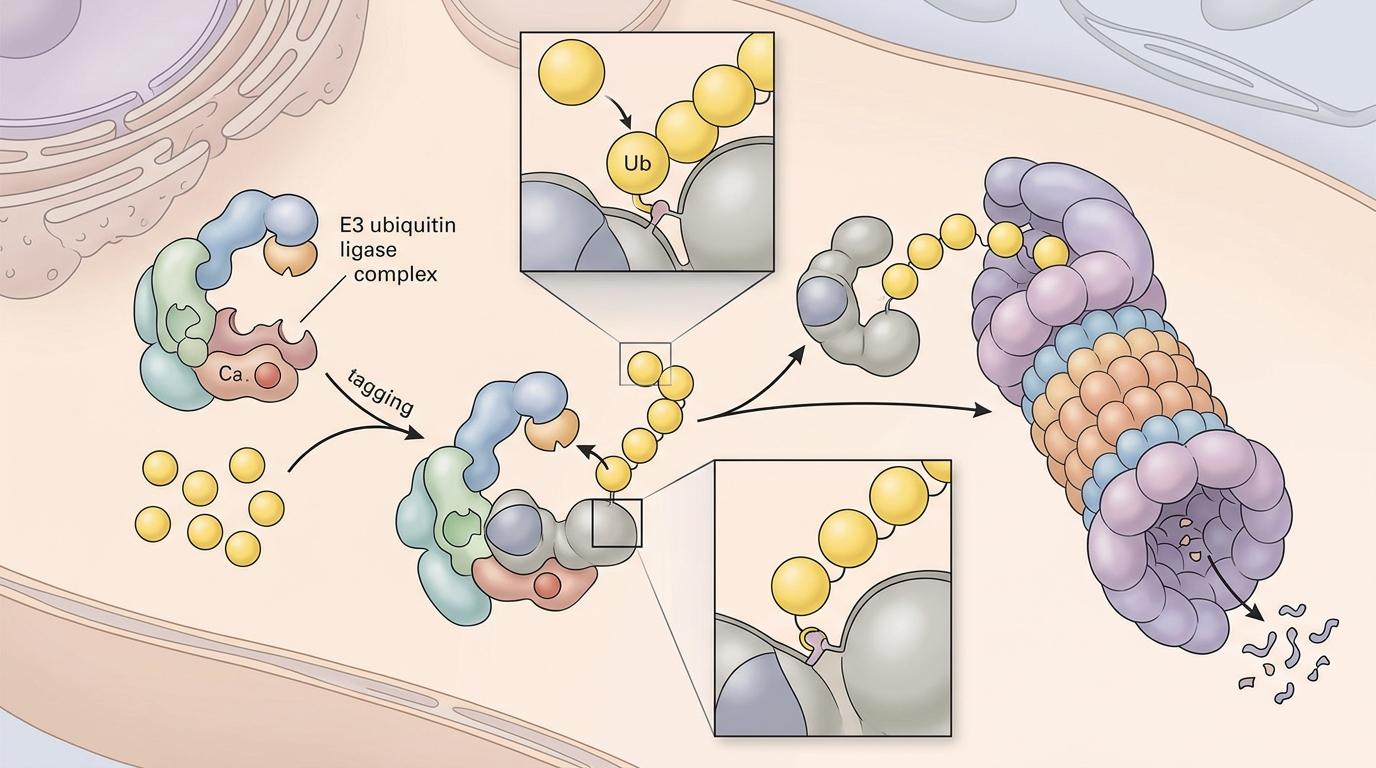
但在耐药癌细胞里,叛变的DR5会抢先和「垃圾处理站」的接头蛋白WDR12结合,把p65从「销毁名单」里拽出来。活下来的p65会进入细胞核,激活NF-κB通路,干两件事:一是下令生产更多DR5,二是促进抗凋亡蛋白BCL2的表达。
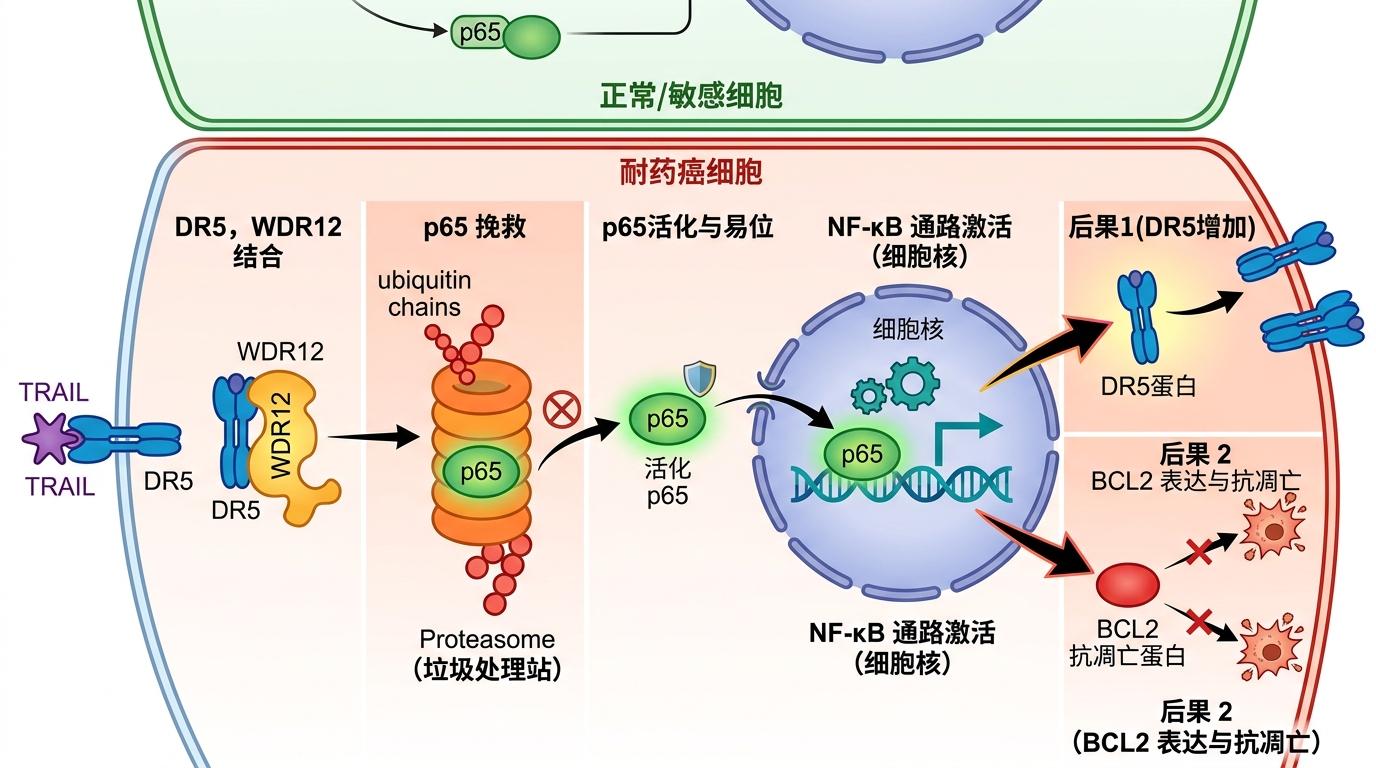
这就形成了一个完美的死循环:
更要命的是,舒尼替尼的治疗反而会强化这个循环——药物压力下,癌细胞会主动上调DR5的表达,让自己变得更「耐打」。
既然找到了耐药的核心机制,团队很快就验证了破解方案:只要靶向DR5/NF-κB/BCL2这条轴,就能把癌细胞从「耐药buff」里拽出来。
在细胞实验和小鼠模型里,他们用DR5抑制剂联合舒尼替尼治疗,原本耐药的肿瘤明显缩小;用NF-κB通路抑制剂阻断p65的激活,也能让癌细胞重新对舒尼替尼敏感。临床数据也支持这个结论:DR5高表达的肾癌患者,对舒尼替尼的治疗反应明显更差,而靶向这条通路的联合治疗,能让这部分患者重新获益。
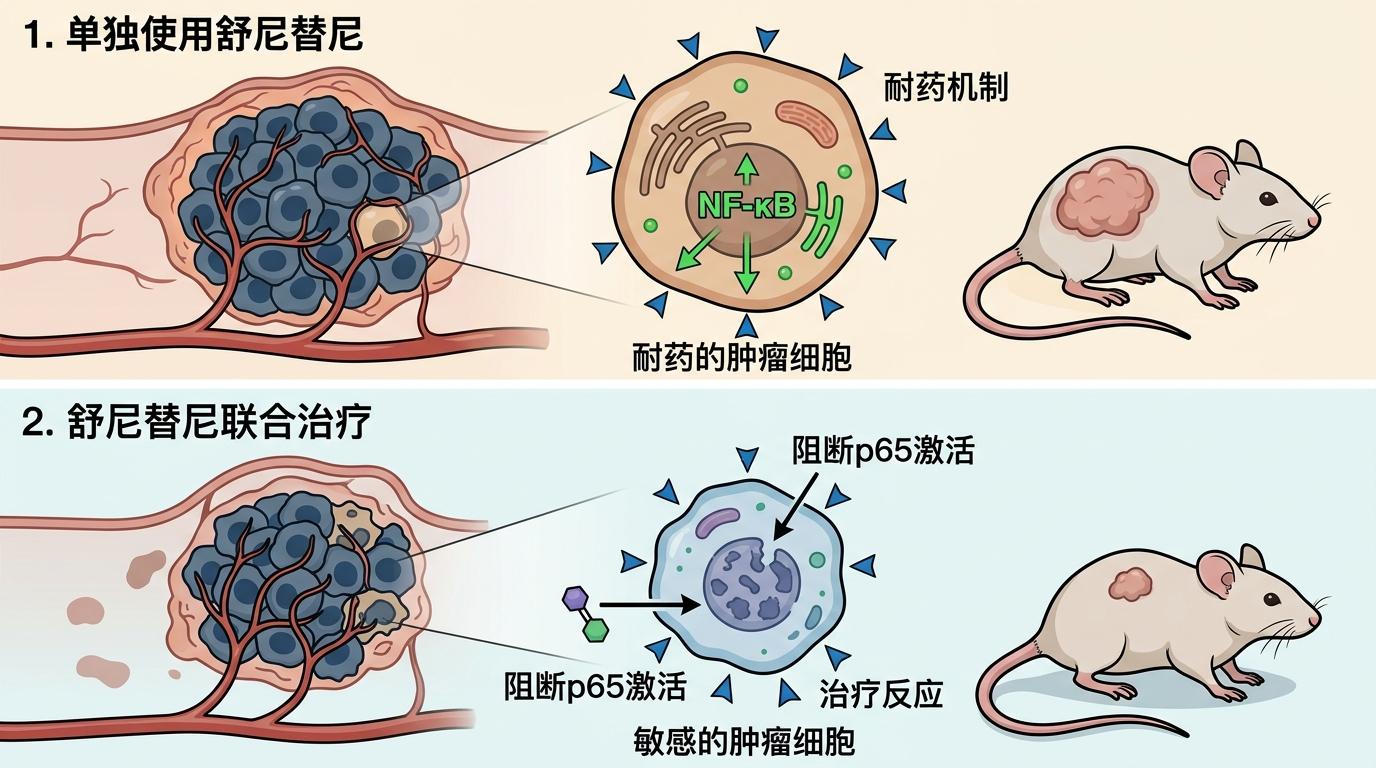
当然,研究也留下了待解的问题:比如不同患者的DR5表达水平差异很大,如何精准筛选适合联合治疗的患者?如何避免靶向NF-κB通路带来的副作用?但不可否认的是,这个发现给那些对舒尼替尼耐药的患者,打开了一扇新的窗。
癌症的耐药性,本质上是癌细胞在药物压力下的「进化」——它们会不断找到新的生存策略,躲开人类的攻击。而解放军总医院的这项研究,就像是在癌细胞的进化路径上,找到了一个致命的「bug」。
「靶点不是单一的,而是一场动态的博弈。」这句话或许能概括癌症治疗的未来:我们不能只盯着癌细胞的某个弱点,还要看懂它们的生存逻辑,才能找到破解的办法。
对于那些在耐药困境中挣扎的肾癌患者来说,这个发现不仅是一个科学突破,更是实实在在的希望——毕竟,每多找到一个耐药机制,就意味着多给了患者一次活下去的机会。