对抗知识焦虑,从看懂这条开始
App 下载
华南鼻咽癌高发:基因与病毒的致命组合
病毒突变|中山大学|HLA基因|EB病毒|鼻咽癌|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
病毒突变|中山大学|HLA基因|EB病毒|鼻咽癌|肿瘤学|医学健康
全球95%的人都感染过EB病毒,但只有不到千分之一的人会患上鼻咽癌——而中国华南地区,却用2%的人口扛下了全球近一半的病例。这个困扰医学界几十年的“南方之谜”,终于在2026年有了答案:不是病毒太凶,也不是人的基因太弱,而是当特定的病毒突变遇上特定的人体基因,风险会飙升17倍。中山大学、新加坡基因组所等多国团队在《Nature》上的这项研究,第一次把鼻咽癌的发病密码,拆解成了宿主与病毒的“双人舞”。为什么偏偏是华南?这对致命组合又是如何形成的?
你可以把人体的HLA基因想象成一个“免疫安检站”——它会把入侵病毒的蛋白质碎片“举起来”给T细胞看,一旦识别出危险,T细胞就会立刻动手清除被感染的细胞。而EB病毒就像个擅长伪装的偷渡者,大部分时候能躲安检站的检查,但当它发生85841G突变时,就会露出一个特殊的“破绽”。
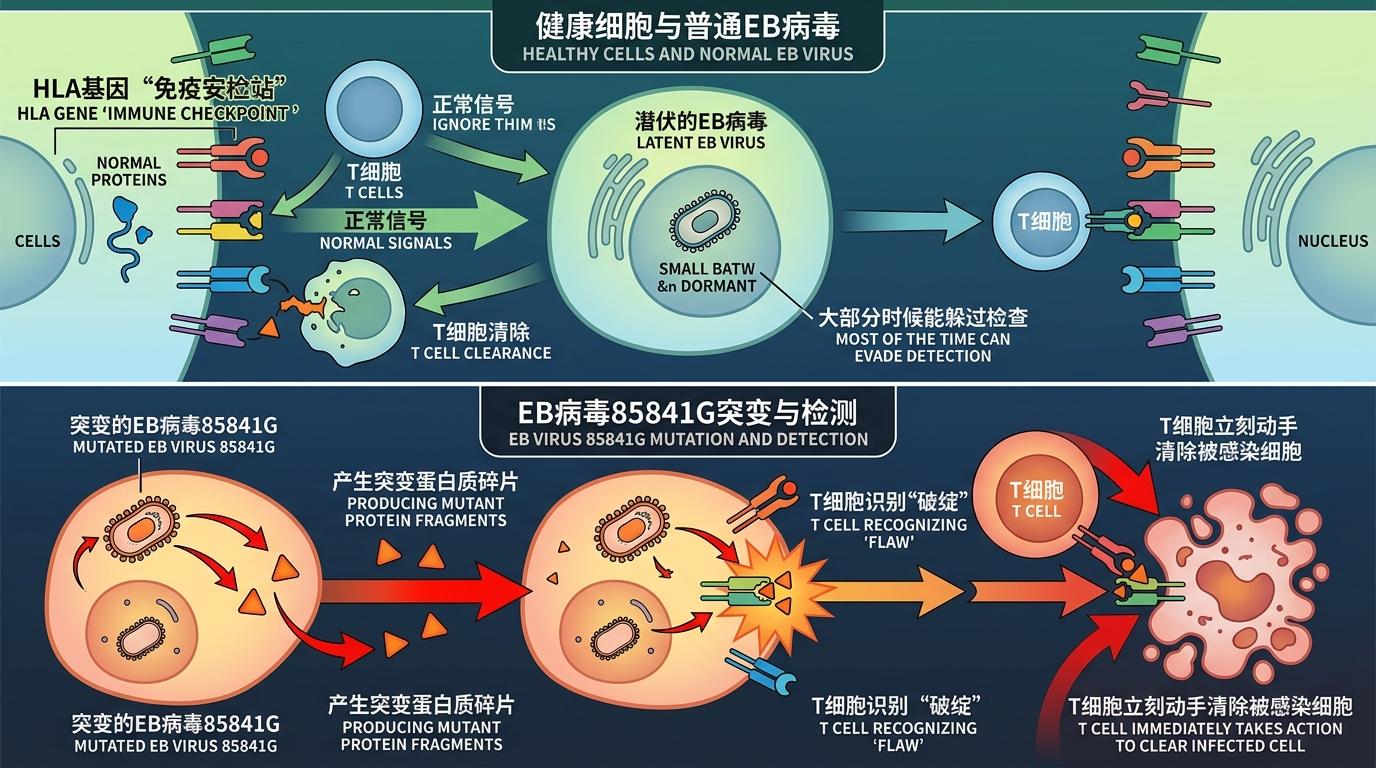
这个破绽刚好能被HLA-A11:01这个“安检员”精准抓住——携带这个基因的人,T细胞能快速识别并清除突变病毒,反而降低患病风险。但如果人体没有HLA-A11:01,又感染了这种突变病毒,安检站就会彻底失效:病毒伪装的蛋白质碎片无法被呈递,T细胞根本不知道敌人已经入侵,任由病毒在鼻咽部悄悄癌变。
研究数据直白得吓人:同时满足“无HLA-A*11:01+感染85841G突变株”的人,仅占总人口的20.5%,却贡献了46.9%的鼻咽癌病例。
这个致命组合不是凭空出现的,而是4000年前一场“病毒联姻”的结果。
通过分子进化分析,研究团队发现,85841G突变株是当时北方和南方的EB病毒谱系重组产生的后代。它在华南地区快速扩散,并非因为它更“凶”,而是因为这里的人群刚好缺少能识别它的HLA-A*11:01基因——或者说,缺少这个基因的人,更容易让这种病毒存活并传播下去。
这是一场漫长的“共进化”:病毒突变出能躲过当地人群免疫的特征,而人群的基因也在筛选着适合生存的病毒毒株。最终,华南地区成了这对组合的“完美温床”:40%的当地人感染了这种高危病毒,同时又有相当比例的人缺乏对应的免疫保护基因。
更关键的是,这种病毒不仅能逃避免疫,还会主动“改造”肿瘤微环境——它的LMP1蛋白会激活多条促癌信号通路,诱导鼻咽上皮细胞无限增殖,还会分泌免疫抑制因子,把肿瘤变成一个“免疫禁区”。
这项研究最直接的价值,是把鼻咽癌的预防从“模糊的地域预警”,变成了“精准的个体画像”。
未来,只需通过简单的基因检测和EB病毒分型,就能快速找出那20.5%的高风险人群——他们不需要像现在这样每年做鼻咽镜筛查,而是可以更早地进行干预:比如注射针对85841G突变株的疫苗,或者定期检测EB病毒载量,一旦发现异常就及时处理。
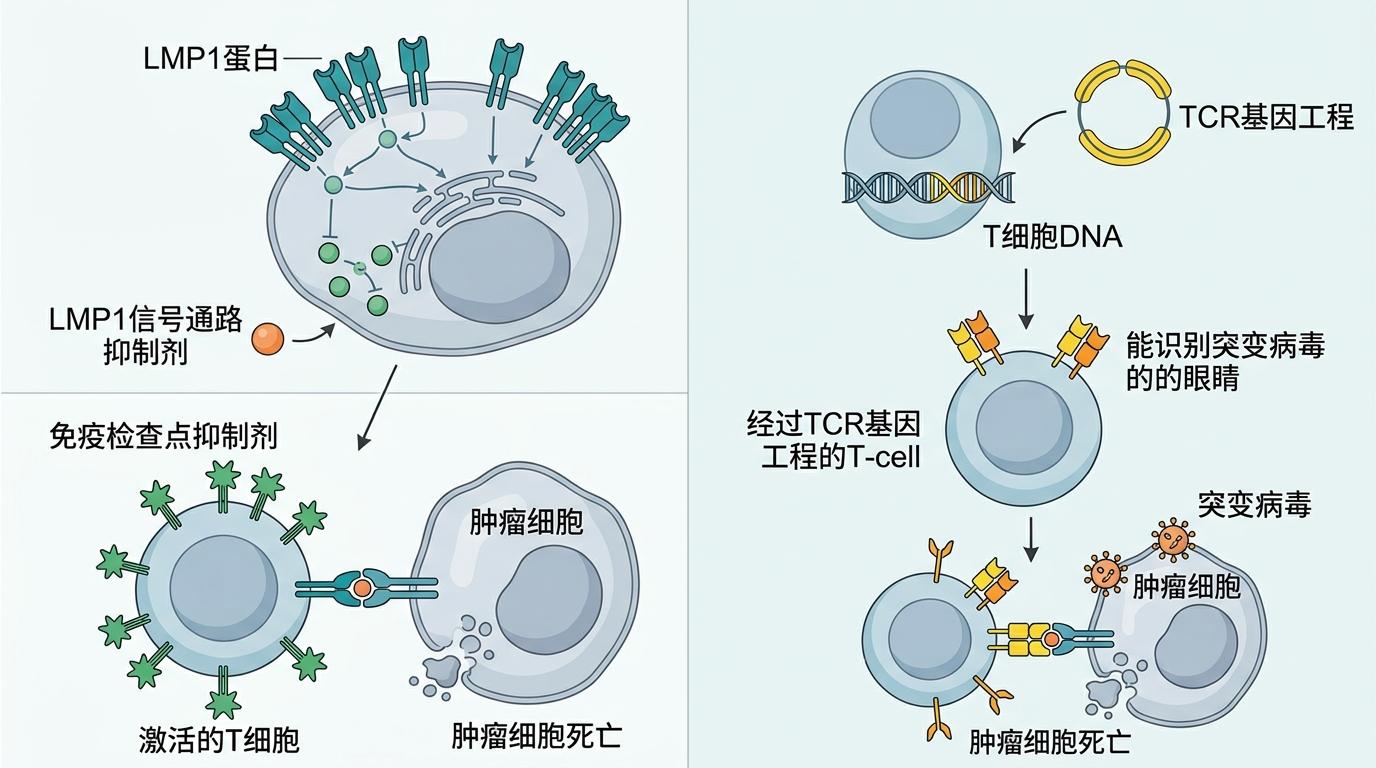
在治疗上,研究也提供了新的方向:针对LMP1蛋白的信号通路抑制剂,或者能激活T细胞的免疫检查点抑制剂,都能精准打击这种病毒驱动的肿瘤。甚至可以通过TCR基因工程,给患者的T细胞装上“能识别突变病毒的眼睛”,让免疫系统重新发挥作用。
当然,目前还有不少未解的问题:比如为什么同样的组合在其他地区没有引发同样的高发?环境因素在其中又扮演了什么角色?但至少,我们终于跳出了“病毒致病”或“基因易感”的单一思路,开始理解疾病背后复杂的“生态系统”。
当我们把鼻咽癌的发病密码拆解到基因与病毒的互动层面,其实也在重新理解所有感染性疾病的本质:从来不是单一的“侵略者”或“受害者”,而是一场持续了千万年的博弈。
病毒与基因共舞,才是疾病的真相。
这项研究不仅解开了华南鼻咽癌的流行之谜,更给了我们一个重要的启示:面对复杂疾病,我们需要的不是“对抗”,而是理解——理解每一个基因的作用,每一种病毒的特征,以及它们在人体这个生态系统里的微妙平衡。毕竟,打破平衡的是自然,但重建平衡的,终将是我们自己。