对抗知识焦虑,从看懂这条开始
App 下载
肝脏的双刃剑:HELZ2如何平衡脂肪肝与血管病?
动脉粥样硬化|血脂调控|脂肪肝|载脂蛋白B|HELZ2|代谢内分泌疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
动脉粥样硬化|血脂调控|脂肪肝|载脂蛋白B|HELZ2|代谢内分泌疾病|医学健康
在健康观念中,“血脂低一点”几乎是一条金科玉律。它意味着更清洁的血管、更低的心血管疾病风险。然而,在我们的身体内部,故事远比这复杂。肝脏,作为人体最繁忙的代谢中枢,时刻面临着一个棘手的权衡:是将脂肪高效“打包”送出,维持自身的清爽,还是减少脂肪的输出,以保护循环系统的通畅?
这个“打包”过程依赖一个关键的装配工——载脂蛋白 B(apoB)。它如同一个勤奋的快递员,将肝脏中的脂肪封装成脂蛋白包裹,发往全身。如果快递员减少,血液中的“包裹”(致动脉粥样硬化的脂蛋白)自然会减少,血管压力骤降。但硬币的另一面是,无法寄出的脂肪只能被迫滞留在肝细胞这个“仓库”里,久而久之,便形成了脂肪肝。肝脏与血管的健康,仿佛成了一个此消彼长的“跷跷板”。那么,肝脏究竟是如何做出决定的?是否存在一个更深层的分子开关,能直接决定快递员apoB的数量,从而在这场健康博弈中扮演最终裁决者的角色?

就在不久前的2025年12月25日,德克萨斯大学西南医学中心的张召博士团队在顶尖期刊《循环》(Circulation)上发表的一项研究,为我们揭开了这个谜底。他们发现了一种名为HELZ2的RNA解旋酶,它正是那个隐藏在幕后,精妙调控肝脏与血管命运的“总开关”。
这项研究的起点颇具戏剧性。团队并未预设任何假说,而是采用了一种“从结果倒推原因”的正向遗传筛选方法。他们在一大群经过随机诱变的小鼠中,寻找那些表现出“肝脂异常”的个体,然后反向追踪导致这一表型的基因线索。这就像在一片广袤的森林里,不预设猎物,而是根据留下的特殊足迹去寻找未知的生物。
最终,他们的目光锁定在一个名为HELZ2的基因上,更精确地说,是该基因上一个极其罕见的功能增强型突变——L1833P点突变,研究者将其命名为 “Colby”。携带Colby突变的小鼠,即便在标准饮食下,也会出现明显的肝脏脂肪堆积,而这一过程竟不依赖于体重的变化。这暗示着,HELZ2可能触及了脂质代谢最核心的调控机制。
深入的机制研究,将故事的核心推向了分子层面。原来,HELZ2的功能就像一把“分子剪刀”,它的工作是识别并降解负责生产apoB的信使RNA(mRNA)。APOB mRNA是制造apoB蛋白的“蓝图”,而HELZ2则通过其解旋酶活性,不断“销毁”这些蓝图,从而控制apoB蛋白的最终产量。
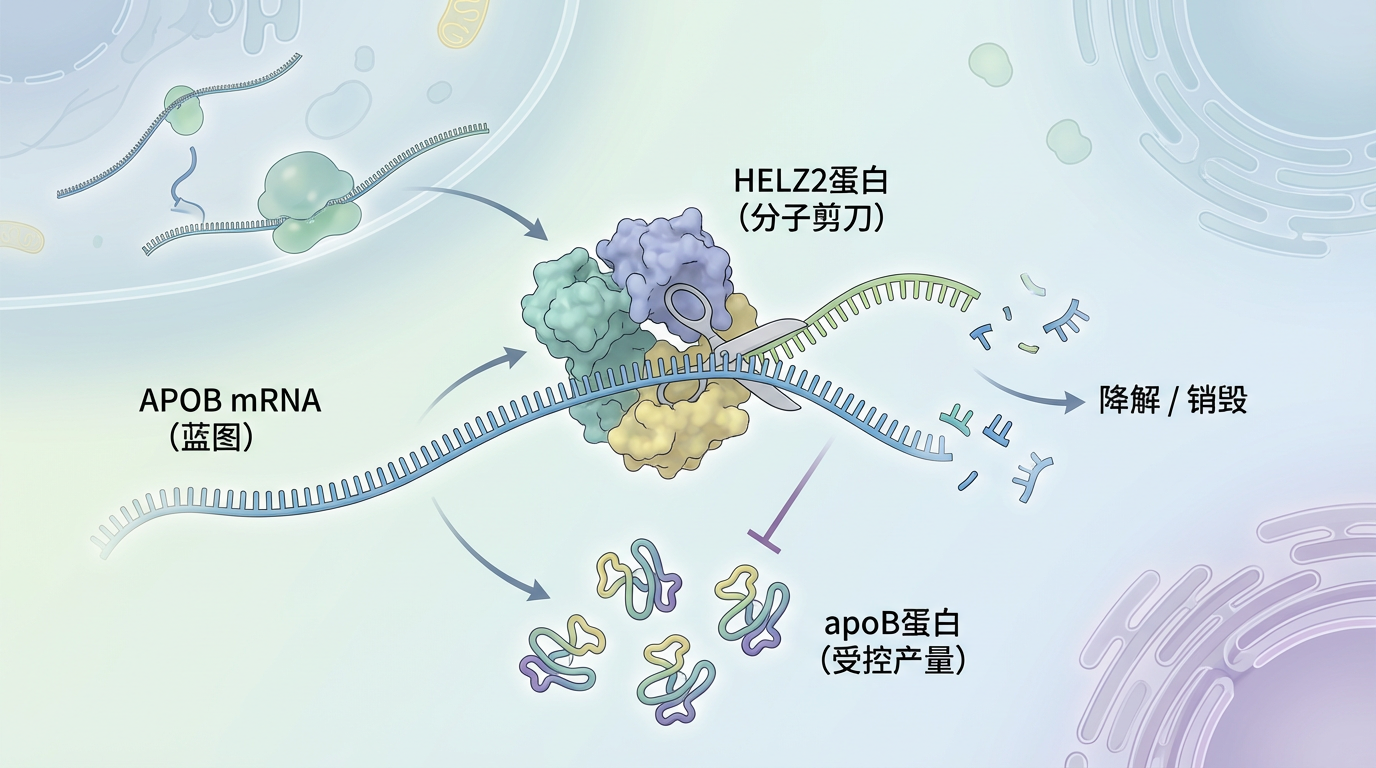
这个发现让一切都豁然开朗:
Colby突变:相当于一把被“磨得更锋利”的剪刀。它增强了HELZ2的活性,导致APOB mRNA被过度降解。蓝图太少,apoB蛋白产量锐减,脂肪运不出去,只能堆积在肝脏,形成脂肪肝。
HELZ2缺失:则像是拿走了剪刀。APOB mRNA的寿命延长,蓝图堆积如山,apoB蛋白被大量生产,肝脏脂肪被高效运出,肝脏自身变得“干净”。
这一正一反的镜像结果,有力地证明了HELZ2在生理状态下,扮演着apoB生产线上一个至关重要的“刹车”或“调速器”角色。它通过决定一段mRNA的“寿命”,直接在源头上掌控了肝脏脂质的去向。
当肝脏中的apoB生产线被HELZ2这把“快剪刀”压制时,血管会发生什么?这正是该研究最具颠覆性的部分。研究团队在两种经典的动脉粥样硬化小鼠模型(Apoe−/− 与Ldlr−/−)中引入了Colby突变。
结果令人震惊:仅仅一份Colby突变基因,就足以对动脉粥样硬化产生显著的保护作用。这意味着,虽然肝脏因为脂肪堆积而“受苦”,但血管却因为循环中的致病脂蛋白减少而“享福”了。HELZ2通过调控APOB mRNA的稳定性,将“肝内脂肪堆积”和“血管硬化风险”这两个看似独立的病理过程,牢牢地拴在了同一根分子轴上。
更重要的是,这一机制并非小鼠独有。通过分析英国生物样本库(UK Biobank)庞大的人群遗传数据,研究者发现,某些人类HELZ2基因的变异,同样与血液中apoB水平的降低显著相关。细胞实验也证实,这些人类变异确实能增强HELZ2降解APOB mRNA的能力。这表明,在人类群体中,大自然也一直在进行着类似的“实验”,HELZ2这个“mRNA寿命开关”同样在悄然影响着我们的代谢健康。
这项发现的意义,远不止于揭示一个新的生物学机制。它为困扰现代医学的两大慢性病——脂肪肝与动脉粥样硬化,提供了一个全新的思考框架,并为药物研发开辟了激动人心的新方向。
传统的降脂策略,如他汀类药物,主要通过抑制胆固醇的合成来起作用。而更新的PCSK9抑制剂,则通过促进脂蛋白的清除来降低血脂。它们都作用于脂质代谢的“下游”环节。而HELZ2的发现则提示了一种全新的“上游”干预策略:直接调控APOB mRNA的稳定性,从根源上控制致病脂蛋白的“生产量”。这为开发“非他汀机制”的降脂新药提供了极具潜力的靶点。
然而,HELZ2的故事也带来了一个深刻的警示:在生命复杂的调控网络中,几乎不存在绝对的“好”与“坏”,更多的是精妙的平衡与取舍。
当我们追求更低的血脂以保护血管时,或许正将负担转移给了肝脏。脂肪肝与动脉粥样硬化,可能并非只是共享相似风险因素的“同路人”,而是被肝细胞内一段mRNA的短暂生命紧紧捆绑的“命运共同体”。当HELZ2这把剪刀挥舞得更快,APOB mRNA的寿命缩短,肝脏与血管便在健康的十字路口,走向了截然不同的分叉点。
未来的治疗或许不再是简单地“降低”某个指标,而是要学会如何“校准”这个系统。如何找到一个最佳的平衡点,既能让血管“轻松”,又不让肝脏“拥挤”?这不仅是留给科学家的巨大挑战,也是对我们理解生命智慧的一次深刻启迪。代谢的真谛,或许就藏在这永恒的动态平衡之中。